1. 서론
콤부차(kombucha)의 정확한 유래는 알려져 있진 않으나 약 기원전 220년경 중국 진나라에서 음용되었다는 기록이 있으며, 찻잎(Camellia sinensis)을 설탕과 혼합하여 Acetobacter, Gluconobacter, Komagataeibacter 종과 같은 아세트산 박테리아와 Saccharomyces, Zygosaccharomyces, Schizosaccharomyces 종과 같은 효모로 발효시킨 약산성 음료이다(De Roos와 De Vuyst, 2018; Lee 등, 2022; Teoh 등, 2004; Villarreal-Soto 등, 2018; Zou 등, 2021). 콤부차의 발효 미생물은 주로 초산균과 효모로 알려져 있으나, 그 외에 유산균도 콤부차 발효 미생물의 최대 30%에 이른다고 보고되었다(Marsh 등, 2014). 콤부차 발효에 관여하는 주요 유산균으로는 Leuconostoc, Lactobacillus, Lactococcus 종이 포함된다(Bogdan 등, 2018). 콤부차의 주요 대사 산물로는 글루콘산, 아세트산, 에탄올이 있으며, 이외에도 비타민, 아미노산, 효소, 폴리페놀, 다양한 유기산 등이 있다(Abaci 등, 2022). 이러한 성분 들은 항산화 작용, 간세포 보호, 항염증 효과, 혈중 콜레스테롤 및 혈당 개선 등 다양한 생리학적 기능과 밀접한 관련이 있다(Woo 등, 2021). 그러나 과량의 설탕 첨가나 장시간의 발효는 미생물의 대사 활성을 과도하게 촉진하여 pH 급하락, 유기산 과생성 및 산도 상승을 초래할 수 있으며, 이는 제품의 관능적 기호성을 저하시킴과 동시에 과발효(over-fermentation) 또는 이상발효(abnormal fermentation)와 같은 비정상적인 발효 현상을 유발하는 주요 요인으로 작용할 수 있다(Chaluvadi 등, 2024; Cohen 등, 2023; Sievers 등, 1995; Sinamo 등, 2022). 최근 이러한 문제점을 개선하기 위해 단순당인 설탕을 대체하여 과일, 채소, 커피, 우유 등 복합 기질을 활용하거나 발효 기간을 단축하는 방식의 다양한 콤부차 제조 전략이 제안되고 있다(Anantachoke 등, 2023; de Melo Pereira 등, 2020; Fabricio 등, 2023; Gangakhedkar 등, 2025; Gustaw 등, 2021; Haug 등, 2007; Verstrepen 등, 2004). 특히 과일을 첨가한 콤부차는 기능성뿐만 아니라 맛과 풍미가 향상되며, 과일의 발효과정을 통해 항산화와 항염 등 다양한 기능성 효과를 얻을 수 있다(Anantachoke 등, 2023; Lee 등, 2022). 이처럼 다양한 기질을 활용한 콤부차에 대한 연구가 진행되고 있으나 복합 원료와 다양한 균주를 동시에 활용한 복합 발효 콤부차의 식품학적 특성 및 생리활성에 관한 연구는 여전히 부족한 실정이다. 또한 기존의 콤부차 연구는 주로 찻잎, 허브류, 과일즙 등을 단독으로 사용한 발효에 집중되어 왔으며, 유산균 기반 발효 ․ 숙성이나 혼합 과실 기질을 적용한 연구는 아직 미흡한 편이다(Su 등, 2023).
토마토는 전 세계에서 가장 널리 소비되는 과일로 다양한 카로티노이드와 폴리페놀이 함유되어 있으며, 항산화 효소의 보조 인자 역할을 하는 셀레늄, 망간, 아연, 구리와 같은 미네랄과 비타민이 풍부하다(Beckles, 2012; Tyssandier 등, 2004). 토마토에 함유되어 있는 다양한 생리활성 물질들로 인해 뛰어난 항산화 활성, 전립선암 예방, 인체 암 증식 억제 효과, 콜레스테롤 수치 완화, 혈압 조절, 심장 질환 예방 효과가 보고되어 있다(Enqelhard 등, 2006; Friedman, 2002; Rao, 2002; Silaste 등, 2007; Yim 등, 2020). 이러한 우수한 영양학적 가치에도 불구하고, 토마토는 당과 수분 함량이 높아 미생물 오염에 취약하고 저장 기간이 짧아 주로 생과 형태로 소비되어 왔다(Lim 등, 2018). 최근에는 식품의 관능적 품질뿐 아니라 기능성을 중시하는 소비자들이 증가함에 따라, 토마토의 다양한 활용 가능성에 대한 관심이 높아지고 있다(Yim 등, 2020). 이에 따라 토마토를 활용한 가공품 개발 연구가 활발히 진행되고 있으며, 현재까지는 주스와 같은 음료류나 퓌레 및 케첩 등 소스류 제품에 주로 집중되어 있는 실정이다(Lim 등, 2018). 한편, 토마토의 발효 가공에 관한 연구들도 일부 보고되어 있다. Kim 등(2010)은 토마토의 알코올 발효 조건에 따른 이화학적 특성 및 토마토 과실주의 품질특성을 조사하였으며, Lim 등(2018)은 토마토 유산발효액의 총페놀 및 플라보노이드 함량 변화와 DPPH 라디칼 소거 활성, 대사산물 분석을 통해 토마토를 이용한 가공품의 개발 가능성을 보고하였다. 또한 Yim 등(2020)은 토마토 고추장을 제조하고 이의 이화학적 분석과 in vitro상의 항산화, α-glucosidase 억제 활성과 지방세포 분화 억제 활성을 확인하였다. Lee 등(2018)은 막걸리 종초를 이용한 토마토 식초의 항산화 활성, 항균 활성 및 3T3-L1 지방전구세포를 이용한 항비만 활성 효과를 보고하였다. 그러나 이러한 연구들은 대부분 단일 발효 형태로 진행되었으며, 혼합 발효는 서로 다른 미생물 간의 상호작용을 통해 대사산물의 다양성과 생리활성을 향상시키는 것으로 알려져 있음에도, 복합 발효 형태인 콤부차에 토마토를 적용한 연구는 아직 보고된 바가 거의 없다(Champagne 등, 2010; Villarreal-Soto 등, 2018).
본 연구에서는 초산발효와 유산발효를 결합한 이중 복합발효형 콤부차 시스템을 구축하여, 기존 콤부차 대비 기능성과 기호성을 동시에 개선할 수 있는 신규 조합 모델을 제시하고자 하였다. 특히 토마토가 지닌 풍부한 카로티노이드와 폴리페놀 성분, 그리고 보조 발효 기질로 사용된 바나나 발효액의 유기산 및 유산균 대사산물이 상호작용함으로써 기존 콤부차에서는 보고되지 않은 새로운 생리활성 발현 가능성이 기대된다(Beckles, 2012; Budiari 등, 2019; Su 등, 2023; Tyssandier 등, 2004). 이에 따라, 본 연구에서는 설탕 대신 과실을 기질로 활용한 토마토 콤부차를 제조한 후 이의 이화학적 특성과 생리활성을 평가함으로써, 토마토 기반 복합발효 콤부차 개발을 위한 기초자료를 제시하고자 한다.
2. 재료 및 방법
본 연구에서 사용된 대저 토마토는 부산광역시 강서구에서 재배된 것을 구매하였고, 70 °Brix 사과 농축액은 ㈜이에스식품원료(Gunpo, Korea)에서 국산 원료로 제조된 제품을 구입하였고, 녹차 가루는 전라남도 보성군에서 재배된 것을 구매하여 4°C에서 냉장 보관하면서 시료로 사용하였다. 바나나 유산 발효원액은 ㈜생생초에서 제공받았다. 3T3-L1 전구지방세포 (CL-173)는 American Type Culture Collection (Manassas, VA, USA)으로부터 분양받아 사용하였다. DMEM, bovine serum, fetal bovine serum은 Gibco BRL (Grand Island, NY, USA)에서 구매하였다. 지방분화유도 시약인 rosiglitazone (ROS), dexamethasone (DEX), 3-isobutyl-methylxanthine (IBMX), Oil Red O solution, formaldehyde, isopropanol 등은 Sigma-Aldrich (St. Louis, MO, USA)에서 구입하여 사용하였다. 생리활성 분석을 위한 L-tyrosine, mushroom tyrosinase, hydrogen peroxide, trichloroacetic acid, K3Fe (CN)6, 2,2’-azino-bis (3-ethylbenzothiazoline-6-sulfonic acid) (ABTS), potassium peroxodisulfate, dibutylated hydroxytoluene, α-tocopherol, α,α’-diphenyl-β-picrylhydrazine (DPPH), peroxidase, quercetin, citric acid, malic acid, succinic acid, lactic acid, acetic acid는 Sigma-Aldrich사(St. Louis, MO, USA) 제품을 사용하였다. Hydrogen peroxide, gallic acid는 Junsei Chemical (Tokyo, Japan)에서 구입하였다.
토마토 식초를 제조하기 위한 균주 효모 Saccharomyces cerevisiae KSH-Y141029와 초산균 Acetobacter pasteurianus DU17-YSAC1은 ㈜생생초(Cheongdo, Korea)에서 위탁받았다. S. cerevisiae KSH-Y141029는 YM broth (BD, Franklin Lakes, NJ, USA)에서 30°C, 정치배양하였다. A. pasteurianus DU17-YSAC1은 0.5% yeast extract (BD), 0.5% glucose (Sigma-Aldrich Co.), 1% glycerin (Daejung, Siheung, Korea), 0.02% MgSO4 (Daejung, Siheung, Korea), and 3% ethanol (Daejung, Siheung, Korea)를 혼합하여 제조한 YEG broth에서 30°C, 120 rpm으로 배양하였다. 바나나 유산발효에 사용된 유산균은 Lactobacillus plantarum KSH-1406으로 MRS broth (BD)에서 37°C에서 정치배양하였다. 모든 균주는 각 배지에 활성화시켜 종균으로 접종하였다.
토마토 식초는 선행 연구(Lee 등, 2013)에 보고된 제조 방법에 따라 제조하였으며, 본 연구에서는 추가로 녹차 가루를 첨가하여 발효를 수행하였다. 우선, 토마토는 세척한 후 꼭지를 제거하고 분쇄한 뒤 30% (w/v) 함량이 되도록 정제수로 희석하고 사과 농축액을 첨가하여 13 °Brix (w/v)로 보당하였다. 그 후 녹차 가루 0.5% (w/v)를 혼합하였다. 1차 알코올 발효 단계에서 S. cerevisiae (5%, v/v)를 토마토 혼합물에 스타터로 접종한 후 30°C에서 4일간 정치발효하였다. 알코올 발효가 끝나면 토마토 혼합물을 80 mesh로 여과하고 2차 초산 발효 단계에서 A. pasteurianus (10%, v/v)를 접종하여 30°C, 120 rpm에서 14일간 배양하였다. 초산 발효가 끝난 후 80 mesh로 여과하였다. ㈜생생초에서 구매한 바나나 유산 발효원액은 65 °Brix 바나나 농축액(Comax International Co., Seoul, Korea)을 5 °Brix (w/v)로 희석한 후 녹차 가루를 0.5% (w/v) 첨가한 다음 ㈜생생초 유산균 L. plantarum KSH-1406 (10%, v/v)를 접종하여 37°C에서 24시간 배양하여 제조하였다. 토마토 콤부차는 토마토 식초의 총산도를 5%로 조정한 후 유산 발효원액과 31:69 비율로 혼합하여 실온에서 3일 동안 발효숙성하여 토마토 콤부차 원액을 제조하였다. 토마토 식초와 바나나 유산 발효원액의 혼합 비율은 식품과 관련된 전공자(대학생 및 대학원생) 20명을 관능평가원으로 선정하여 전체적인 기호성이 가장 높은 혼합액을 채택하여 개발하였으며 녹차의 첨가량은 산업적인 측면을 고려하여 콤부차 제조 시 일반적으로 사용되는 수준을 참고하여 설정하였다. 이후 실험은 토마토 콤부차 원액(KL), 31% 함량 토마토 발효액(FT) 및 69% 함량 바나나 유산 발효액(FD)을 시료로 사용하였다.
당도는 각 시료 300 μL를 당도계(Atago Pocket PAL-3, Atago Co., Tokyo, Japan)에 취해서 측정하여 °Brix로 표기하였다. pH는 pH meter (pH-200L, iSTEK Co., Seoul, Korea)로 측정하였으며, 총산도는 0.1 N NaOH 용액을 이용하여 pH가 8.3이 될 때까지 적정하고, acetic acid의 양으로 계산하였다.
DPPH radical 소거 활성은 Blois(1958) 방법을 이용하였다. 각 시료 1 mL를 4 mM DPPH solution 3 mL와 혼합하고 30분간 암소에서 반응시켜 UV/Vis-spectrophotometer (SpectraMax Plus 384, Molecular Device, San Jose, CA, USA)로 517 nm에서 흡광도를 측정하였다. Positive control로 0.1% butylated hydroxytoluene (BHT)와 0.1% α-tocopherol를 사용하였다. 대조군은 시료 대신 에탄올 1 mL를 이용하였고 DPPH radical 소거 활성능은 대조군에 대한 흡광도의 감소비율로 표시하였다.
ABTS∙+ radical 소거 활성은 Biglari 등(2008)의 방법을 변형하여 측정하였다. 7.4 mM ABTS와 2.6 mM potassium peroxodisulfate와 혼합한 후 실온 암실에서 16시간 동안 반응시켰다. 이후 ABTS 용액을 734 nm에서 0.70±0.01의 흡광도가 되도록 증류수로 조정하였다. ABTS 용액 3.9 mL과 각 시료 0.1 mL를 vortexing 후 실온에서 암실에서 10분간 반응시켰다. 반응이 끝난 후 UV/Vis-spectrophotometer에서 734 nm로 측정하였다. 대조군은 시료 대신 증류수를 이용하여 대조군에 대한 흡광도의 감소비율로 나타냈다.
환원력은 Yildirim 등(2001)의 방법을 변형하였다. 각 시료 1 mL과 0.2 M phosphate buffer (pH 6.6) 2.5 mL와 1% K3Fe (CN)6 (w/v) 2.5 mL를 혼합한 후, 50°C에서 30분간 반응시켰다. 이후 반응액과 10% trichloroacetic acid (w/v) 2.5 mL를 첨가하고 3,000 rpm, 10분간 원심분리하였다. 1 mL의 상층액에 증류수 1 mL과 0.1% FeCl3 (w/v) 2 mL를 첨가하여 700 nm에서 흡광도를 측정하였다.
H2O2 소거 활성은 Műler (1958)의 방법에 따라 측정하였다. 각 시료 100 μL에 35% hydrogen peroxide 20 μL를 첨가하여 37°C에서 5분간 반응시켰다. 반응 후 1.25 mM ABTS 시약과 1 unit/mL peroxidase을 각각 30 μL를 혼합하여 37°C에서 10분간 반응시켰다. 반응이 끝난 후 UV/Vis-spectrophotometer를 이용하여 405 nm로 흡광도를 측정하였다.
Tyrosinase 저해 활성은 Chen과 Kubo (2002)의 방법을 변형하여 측정하였다. 각 시료 20 μL와 50 mM phosphate buffer (pH 6.5) 230 μL와 220 unit/mL mushroom tyrosinase 10 μL, 2.5 mM L-tyrosine 40 μL를 혼합하여 37°C에서 30분간 반응시킨다. 그 후 UV/Vis-spectrophotometer를 이용하여 450 nm로 흡광도를 측정하였다. Positive control로 0.1% kojic acid (w/v)을 사용하였다. 대조군은 시료 대신 증류수를 이용하여 대조군에 대한 흡광도의 감소비율로 나타냈다.
총폴리페놀 함량은 Folin-Ciocalteu 방법에 따라 측정하였다(Gao 등, 2000). 각 시료 0.1 mL와 증류수 8.4 mL, 2 N Folin-Ciocalteu 용액 0.5 mL를 혼합하고 20% Na2CO3 1 mL를 첨가하여 2시간 반응시킨다. 반응이 끝난 후 UV/Vis-spectrophotometer에서 725 nm로 측정하였다. 표준곡선은 gallic acid를 이용하여 mg GAE/L로 계산하였다.
총플라보노이드 함량은 Abdel-Hameed (2009)의 방법을 변형하여 측정하였다. 각 시료 0.5 mL와 10% diethylene glycol 5 mL과 혼합 후 1 N NaOH 0.5 mL를 첨가하였다. 이후 37°C에서 1시간 동안 반응시켰다. 반응이 끝난 후 UV/Vis-spectrophotometer로 420 nm에서 흡광도를 측정하였다. 표준곡선은 quercetin을 이용하여 mg QE/L로 환산하였다.
유기산 분석은 각 시료를 0.45 μm membrane filter로 필터하여 사용하였다. 유기산 조성은 high-performance liquid chromatography (Shimadzu Co. Model Prominence, Kyoto, Japan)를 이용하여 측정하였다. 유기산 분리는 PL Hi-Plex H column (7.7 × 300 mm, Agilent Co., Santa Clara, CA, USA)을 사용하여 65°C에서 수행하였다. 이동상은 5 mM H2SO4를 사용하였고 주입량은 20 μL, 유속은 0.6 mL/min으로 일정하게 유지하였다. Detector는 SPD-20A UV/VIS Detector를 사용하였고, 각 유기산(citric acid, malic acid, succinic acid, lactic acid, acetic acid)과 일치하는 피크는 각 표준물질의 머무름시간과 비교하여 확인하였다.
3T3-L1 전구지방세포는 10% bovine serum을 함유한 DMEM를 사용하여 37°C, 5% CO2 incubator (SCA-165DS, ASTEC Co., Ltd., Fukuoka, Japan)에서 2일마다 계대 배양하였다. 전구지방세포는 100% confluence에 도달할 때까지 배양한 후 2 μM ROS, 1 μM DEX 0.5 mM IBMX, 10 μg/mL 및 10% fetal bovine serum (FBS)을 포함하는 DMEM인 분화 유도 배지를 2일간 처리하고 10% FBS 10 μg/mL을 포함하는 DMEM으로 교체한 후 2일 간 배양하였다. 이후 10% FBS를 포함하는 DMEM을 처리하여 분화 유도를 진행하였으며 2일마다 배지를 교체하였다. 지방세포의 분화 억제 효과를 확인하기 위해 지방 분화 유도 기간 동안 각 시료를 처리하였다. 시료는 동결건조를 통해 분말화 한 후 증류수에 용해하여 농도별로 제조하였다.
토마토 콤부차의 세포독성은 SRB assay를 사용하여 평가하였다(Vichai과 Kirtikara, 2006). 3T3-L1 전구지방세포를 2×104 cells/well이 되도록 96 well plate에 분주한 다음 24시간 동안 37°C, 5% CO2 incubator (SCA-165DS, ASTEC Co., Ltd.)에서 배양하였다. 이후 시료를 농도별로 처리하여 48시간 동안 배양하였다. 반응이 끝난 후 배지를 제거하고 12% TCA를 첨가하여 4°C에서 1시간 동안 세포를 고정시키고 각 well을 세척하였다. 각 well에 0.4% SRB 용액을 첨가하고 암실에서 1시간 염색하였다. 1% acetic acid로 염색이 끝난 well을 세척한 후 10 mM Tris buffer로 세포내 염색된 SRB를 녹여내어 상등액을 96 well plate에 옮기고 UV/Vis-spectrophotometer로 540 nm에서 흡광도를 측정하였다. Control 군의 값을 기준으로 백분율로 계산하였다.
3T3-L1 전구지방세포는 6-well plate에 배양하여 시료 처리 및 분화 유도가 완료된 뒤 phosphate-buffered saline (PBS)로 세척 후 4% formaldehyde 용액으로 1시간 동안 반응하여 고정하고 증류수로 세척하였다. 고정된 세포는 60% isopropanol을 이용해 제조한 0.5% Oil Red O 용액으로 염색시킨 뒤 증류수로 3회 세척하고 광학 현미경(BX53, Olympus Optical Co., Ltd., Tokyo, Japan)을 사용하여 200배의 배율로 관찰했다. 이후 세포 내 지질을 정량하기 위해 염색된 세포에 60% isopropanol 시약을 첨가하여 세포 내 염색된 Oil Red O를 용해시킨 뒤 UV/Vis-spectrophotometer를 이용하여 540 nm 파장에서 흡광도를 측정하였다.
지방세포 분화 유도 및 각 시료를 처리한 후 triglyceride kit (Abcam Inc., Cambridge, UK)를 이용하여 중성 지방 함량을 측정하였다. 우선 지방 분화 유도 기간 동안 각 시료를 처리한 지방세포를 채취하고 PBS로 세척하였다. 5% NP-40 용액 1 mL에 세포를 재현탁하고 균질화하였다. 그 후 water bath에서 100°C, 5분간 천천히 가열한 후 실온에서 냉각시켰다. 이 과정을 반복하여 세포 내 중성지방을 완전히 용해시킨 후 용해된 시료를 원심분리기(Micro 17TR, Hanil Science Industrial Co., Ltd., Incheon, Korea)를 이용하여 17,000 rpm으로 2분 동안 원심분리하여 불용성 물질을 제거하고 상등액을 채취하여 시료로 사용하였다. 96-well plate에 시료와 농도별 표준 용액을 각각 50 μL씩 분주하고 cholesterol esterase 2 μL를 첨가하여 실온에서 20분간 반응시켰다. 반응 혼합액에 triglyceride reaction mix 50 μL씩 혼합한 후 실온에서 1시간 반응시켰다. 반응이 끝난 후 흡광도 570 nm에서 측정하여 흡광도 값을 kit 프로토콜에 따라 mmol/L로 계산하였다.
3. 결과 및 고찰
토마토를 이용한 콤부차의 당도, pH 및 총산도를 분석한 결과는 Table 1에 나타냈다. FT, FD 및 KL의 당도는 각각 4.0 °Brix, 4.2 °Brix 및 4.5 °Brix로 나타났다. 그러나 각 군 간의 유의적인 변화는 확인되지 않았다. pH의 경우 각각 3.05, 3.51 및 3.12로 확인되었고 FD에서 유의적으로 높은 수치를 보였다(p<0.05). FT, FD 및 KL의 총산도는 각각 2.93%, 0.85% 및 3.02%로 FD에서 현저한 차이를 보였다(p<0.05). FD는 발효 전부터 바나나 농축액을 5 °Brix로 희석하여 발효 기질로 사용함으로써, 초기 이화학적인 조성 차이에서 영향이 있는 것으로 판단된다. Wu 등(2023)은 Fu-brick tea kombucha의 발효 과정에서 pH가 감소하고 환원당 함량은 전반적으로 증가하였으나 일부 기간에서는 일시적으로 감소하였으며, 일부 유기산은 일정 시간까지 증가한 후 감소하는 양상을 보여 이러한 변화가 발효 중 미생물의 대사활동에 기인한 것으로 설명하였다. 따라서, KL은 FT와 FD를 혼합하여 숙성한 것으로 숙성과정에서 일부 미생물들의 대사가 일어났거나 혼합가공을 통해 이화학적 변화가 일어난 것으로 사료된다.
| Sample | Sugar content (°Brix) | pH | Total acidity (%) |
|---|---|---|---|
| FT1) | 4.00±0.302)a3) | 3.05±0.25b | 2.93±0.11a |
| FD | 4.20±0.20a | 3.51±0.15a | 0.85±0.02b |
| KL | 4.50±0.30a | 3.12±0.03b | 3.02±0.06a |
토마토 콤부차의 유기산 분석 결과는 Table 2와 같다. FT의 유기산 함량은 구연산 89.86 mg%, 숙신산 19.52 mg%, 아세트산 941.53 mg%로 확인되었다. FD는 구연산(83.81 mg%), 숙신산(28.99 mg%), 젖산(332.80 mg%), 아세트산(1.91 mg%)을 함유하는 것으로 나타났다. KL의 구연산, 숙신산, 젖산 및 아세트산은 각각 205.31 mg%, 11.22 mg%, 362.26 mg% 및 1,279.66 mg%로 나타났다. 이전 연구에서 매실을 효모와 초산균으로 2단 발효할 때 초산과 숙신산이 증가하며, 발효 과정의 상호전환으로 유기산 조성이 재구성될 수 있음을 보고하였다(Chidi 등, 2018; Kim 등, 2021). 또한 유산균은 당을 기질로 이용해 젖산과 초산 등 대사산물을 생성한다(Mazzoli 등, 2014). 더 나아가 젖산은 피루브산을 거치는 알코올 발효의 부산물로 형성될 수 있으며, 사과산은 유산균에 의해 젖산으로 전환될 수 있다(Masino 등, 2008). Chen 등(2013)은 Shanxi aged vinegar는 숙성 단계에서 구연산, 아세트산, 젖산이 증가하는 것으로 확인되었으며, 이러한 변화는 발효 및 숙성 과정에서 미생물의 대사활동에 의해 형성된 것으로 보고하였다. Acetobacter의 대사활성 중 숙신산은 TCA 회로로 재편입되어 산화적 대사에 이용되어 숙신산이 감소할 수 있고 반대로 구연산이 증가할 수 있다(Feng 등, 2023; Wei 등, 2023). 본 연구 결과에서 숙신산을 제외하고 모든 유기산은 대체적으로 KL에서 증가한 것으로 확인되었는데, 이는 효모, 초산균 및 유산균의 혼합 숙성 단계에서 미생물들의 복합적인 대사활동과 TCA 회로 연계 반응에 의해 유기산 대사 균형이 변화한 결과로 판단된다.
폴리페놀과 플라보노이드는 식물에 존재하는 주요 2차 대사산물로서, 인체 내에서 직 ․ 간접적으로 생리활성에 영향을 미치는 것으로 알려져 있다(Rudrapal 등, 2024). 토마토 콤부차의 총폴리페놀 및 총플라보노이드 함량을 측정한 결과는 Table 3에 나타냈다. FT의 총폴리페놀 및 플라보노이드 함량은 각각 429.22 mg GAE/L 및 355.03 mg QE/L로 확인되었으며, FD는 각각 368.11 mg GAE/L 및 351.52 mg QE/L였다. KL의 총폴리페놀 및 플라보노이드 함량은 각각 456.89 mg GAE/L, 341.51 mg QE/L으로 나타났으며, 총폴리페놀의 경우 FT와 FD보다 유의적으로 높은 함량을 보였다(p<0.05). 이전 연구에서 감귤 와인은 초산발효를 통해 페놀성 화합물 함량이 유의미하게 증가한 것을 확인하였으며, 파인애플 유산균 발효물은 발효에 의해 총폴리페놀 함량이 증가한 것으로 나타났다(Jung과 Oh, 2022; Won 등, 2024). Lee과 Yi (2023)는 과일 껍질을 첨가한 콤부차가 발효 중 폴리페놀과 플라보노이드 함량이 증가한다고 보고하였다. 구기자를 이용한 혼합 발효물의 총폴리페놀 및 플라보노이드 함량은 단일 발효물의 함량보다 유의적으로 증가하였고, 이는 발효 중 과일 주스 내 배당체 형태의 페놀성 화합물이 더 많이 분해되어 단순한 형태의 자유 페놀 화합물로 전환되었다고 보고하였다(Qiang 등, 2025; Wang 등, 2024). Hur 등(2014)은 미생물의 종류에 따라 발효를 통해 식물의 페놀 함량을 증가시킬 수 있다고 보고하였다. 반대로 일부 발효액에서는 플라보노이드의 일종인 카테킨과 에피카테킨 농도가 숙성 중 감소하는 것으로 나타났으며, 발효 과정에서 카테킨류는 효소 및 산화 작용 때문에 구조적 변화와 가수분해가 일어나면서 플라보노이드 함량이 감소할 수 있다고 보고하였다(Barrio-Galán 등, 2015; Liu 등, 2022). 본 연구에서 KL의 총폴리페놀 함량은 유의적으로 증가한 반면, 총플라보노이드 함량은 큰 변화를 보이지 않았다. 이러한 결과는 숙성 과정에서 다양한 미생물이 공생적으로 작용하여 폴리페놀 화합물의 생성 및 전환을 촉진하는 동시에, 플라보노이드의 산화적 ․ 효소적 분해를 일정 수준 억제한 데 기인한 것으로 판단된다.
| Sample | Contents (mg%) | |
|---|---|---|
| Total polyphenol contents (GAE1)) | Total flavonoid contents (QE2)) | |
| FT1) | 429.22±10.872)b3) | 355.03±17.40a |
| FD | 368.11±18.15c | 351.52±11.20a |
| KL | 456.89±6.54a | 341.51±14.06a |
토마토 콤부차의 DPPH radical 소거 활성을 Fig. 1A에 나타냈다. DPPH 시약은 보라색을 띄는데, 항산화 물질과 반응하여 황색으로 변화하는 반응을 이용한 방법이다(Ahn 등, 2015). α-Tocopherol과 BHT은 강력한 항산화제로서, DPPH radical, ABTS∙+ radical 및 hydrogen peroxide 소거 활성 측정 시 대표적인 양성대조군(positive control)으로 0.1% 농도 수준에서 in vitro 항산화 활성 실험의 기준물질로 널리 사용되며, 라디칼 소거능과 환원력에서 높은 항산화 활성을 나타낸다(Min 등, 2023; Park 등, 2023). 0.1% α-tocopherol과 0.1% BHT의 DPPH radical 소거 활성능은 각각 85.58% 및 89.94%로 유의적으로 가장 높은 수치를 보였다(p<0.05). FT, FD 및 KL은 각각 78.34%, 68.43% 및 79.33%의 DPPH radical 소거 활성을 나타냈으며, positive control군을 제외하고 KL에서 가장 높은 소거능이 확인되었다.
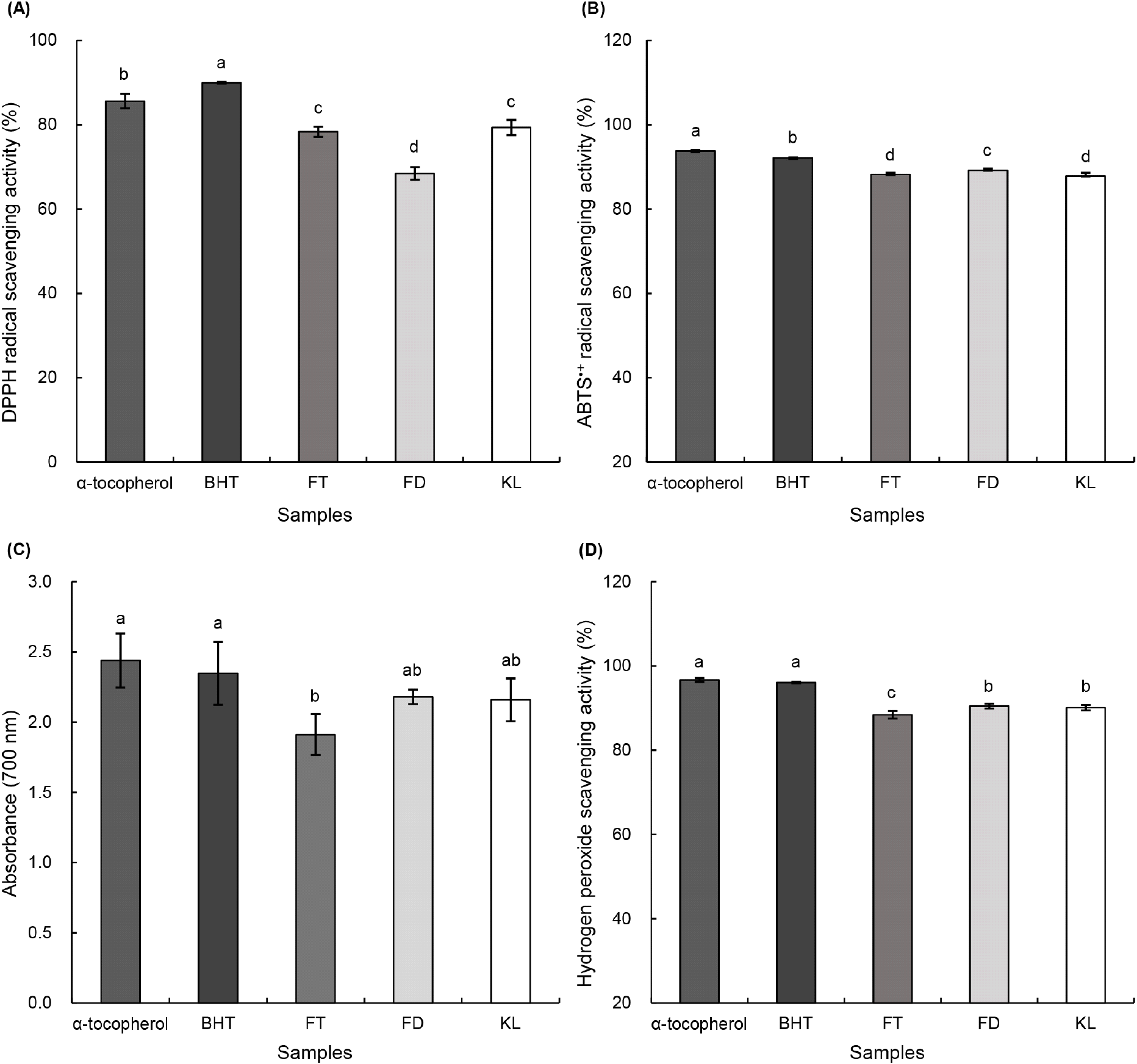
ABTS∙+ radical 소거 활성 측정은 항산화제가 radical에 수소 원자를 제공하여 안정화시키는 과정에서 청색이 탈색되는 원리를 기반으로 하며, 이를 통해 시료의 항산화 활성을 평가할 수 있다(Re 등, 1999). 토마토 콤부차의 ABTS∙+ radical 소거 활성 결과는 Fig. 1B와 같다. FT, FD 및 KL의 ABTS∙+ radical 소거 활성은 각각 88.22%, 89.15% 및 87.81%로 FD가 유의적으로 높은 소거능을 보였지만, 모든 군에서 80% 이상의 높은 수치로 확인되었다.
토마토 콤부차의 환원력은 Fig. 1C에 나타내었다. 환원력은 700 nm에서 흡광도를 측정하는 방법으로, 이는 Fe3+ 이온이 항산화제의 수소 공여에 의해 안정화되면서 Fe2+로 환원되는 과정을 이용한 원리이다(Sa 등, 2010). 0.1% α-tocopherol과 0.1% BHT의 환원력은 각각 2.44, 2.35로 높은 수치를 보였다. KL의 환원력은 2.16으로 FT (1.91), FD (2.18)와 유사한 값으로 나타났다. 또한 KL의 환원력 수치는 positive control군들과 비슷한 활성을 보여 뛰어난 환원력을 보유한 것으로 확인되었다.
Hydrogen peroxide 자체는 비교적 독성이 낮으나, 체내에서 효소 작용에 의해 쉽게 다른 형태의 활성산소로 전환될 수 있고 이 과정에서 생성된 활성산소는 금속 이온과 반응하여 hydroxyl radical을 형성하고, 이는 강한 독성을 나타내어 DNA 손상 및 노화와 같은 생리적 변화를 유발하는 것으로 알려져 있다(Kang 등, 2002). 토마토 콤부차의 hydrogen peroxide 소거 활성 결과는 Fig. 1D와 같다. 0.1% α-tocopherol과 0.1% BHT의 hydrogen peroxide 소거 활성은 각각 96.67% 및 96.05%를 보였다. FT, FD 및 KL의 hydrogen peroxide 소거 활성은 각각 88.42%, 90.48% 및 90.09%로 확인되었으며, KL은 숙성 후에도 높은 hydrogen peroxide 소거 활성을 유지하였다. 폴리페놀과 플라보노이드는 대표적인 페놀성 화합물로, 과일을 비롯한 다양한 식물에 다량 존재하며, 분자 내 하이드록실기를 통해 항산화 활성을 나타내는 것으로 알려져 있다(Bastida 등, 2022; Jung과 Oh 등, 2022). Platzer 등(2022)은 폴리페놀과 플라보노이드가 DPPH radical, ABTS∙+ radical 및 oxygen radical absorbance capacity (ORAC) 등의 라디칼 소거에 관여하며, 특히 플라보노이드류가 전반적으로 높은 항산화 활성을 보였다고 보고하였다. Flavonoids는 폴리페놀의 중요한 하위군으로서 phytochemical 중 가장 큰 계열에 속하며 채소와 과일에서 가장 광범위하게 존재하고, 자유라디칼과 활성산소종(ROS)을 제거하며 금속이온을 킬레이션함으로써 우수한 항산화 활성을 나타낸다(Hassanpourt과 Doroudi, 2023). 본 연구에서 FT, FD 및 KL 간의 항산화 활성은 유의적인 차이를 보이지 않았으나, KL의 높은 항산화능이 숙성 후에도 안정적으로 유지되었다. 이러한 결과는 플라보노이드가 폴리페놀 중 항산화 활성에 주요하게 기여하는 화합물군임을 고려할 때, 이전 연구에서 시료 간 총플라보노이드 함량이 유사한 수준을 보인 점과 관련이 있는 것으로 판단된다.
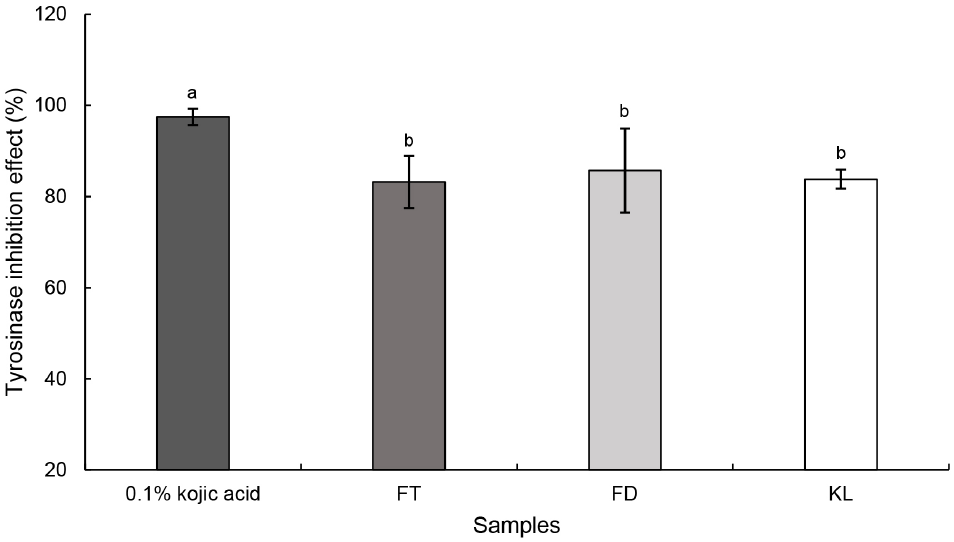
Tyrosinase는 멜라닌 합성 경로에서 핵심적인 효소로, L-tyrosine을 L-DOPA로 전환시키고 L-DOPA를 산화시켜 dopachrome을 형성하는 역할을 한다. 특히 버섯 유래 tyrosinase는 멜라닌 생합성 억제제의 잠재적 후보 물질을 탐색하기 위한 표적 효소로 널리 활용되고 있다(Lawrence 등, 2002). Positive control인 0.1% kojic acid의 tyrosinase 억제능은 97.48%로 가장 높은 활성을 보였고 FT, FD 및 KL은 각각 83.18%, 85.70% 및 83.79%로 나타났다(Fig. 2). 모든 군에서 tyrosinase 저해능은 80% 이상으로 확인되었다. Tyrosinase 저해 활성은 quercetin, kaempferol과 같은 플라보노이드류와 catechin같은 폴리페놀류와 관련이 있다(Jeong 등, 2010). Stewart 등(2000)은 토마토가 주로 quercetin 및 kaempferol 배당체와 같은 플라보노이드를 풍부하게 함유하고 있음을 보고하였다. Musial 등(2020)은 녹차의 주요 생리활성 화합물이 catechin임을 보고하였다. 또한 Kim과 Lee (2003)는 팽이, 느타리 및 표고버섯 발효액의 tyrosinase 저해 활성은 발효 ․ 숙성 기간 동안 큰 변화를 보이지 않았다고 보고하였다. 또한 Lang 등(2021) Traditional fermented Rosa 발효액의 농도별 tyrosinase 억제 활성 측정 결과, 발효 ․ 숙성 7일 이후부터 활성이 점차 증가하였고 30일 시료에서 유의적인 차이가 나타났다고 보고하였다. 본 연구에서 KL의 tyrosinase 저해 활성은 FT 및 FD와 유의적인 차이는 없었으나, 높은 억제 활성을 유지하였다. 이는 상대적으로 짧은 발효 ․ 숙성 기간으로 인해 시료 간 유의적인 차이가 나타나지 않은 것으로 판단되며, 이러한 높은 tyrosinase 저해 활성은 토마토 및 녹차가 함유한 quercetin, kaempferol, catechin 등의 다양한 생리활성 물질이 복합적으로 작용한 결과로 사료된다. 추후에 세포 수준의 심도 있는 미백 관련 실험을 통해 KL의 효소 억제 활성이 실제 멜라닌 생성 억제 효과로 이어지는지를 검증할 필요가 있을 것으로 판단된다.
3T3-L1 전구지방세포를 이용한 실험은 유기산과 총폴리페놀 함량이 가장 높은 토마토 콤부차로 진행하였다. 3T3-L1 세포에 대한 토마토 콤부차의 세포독성을 확인하기 위해 SRB assay를 수행하였고, 그 결과는 Fig. 3A와 같다. 토마토 콤부차 추출물 200, 300, 400, 500 μg/mL의 처리 농도에서 세포 사멸률에 유의한 차이가 확인되지 않았다. 따라서 세포독성이 나타나지 않는 농도 범위 내에서 3T3-L1 지방전구세포를 이용한 지질 축적 억제 실험을 수행하였다.
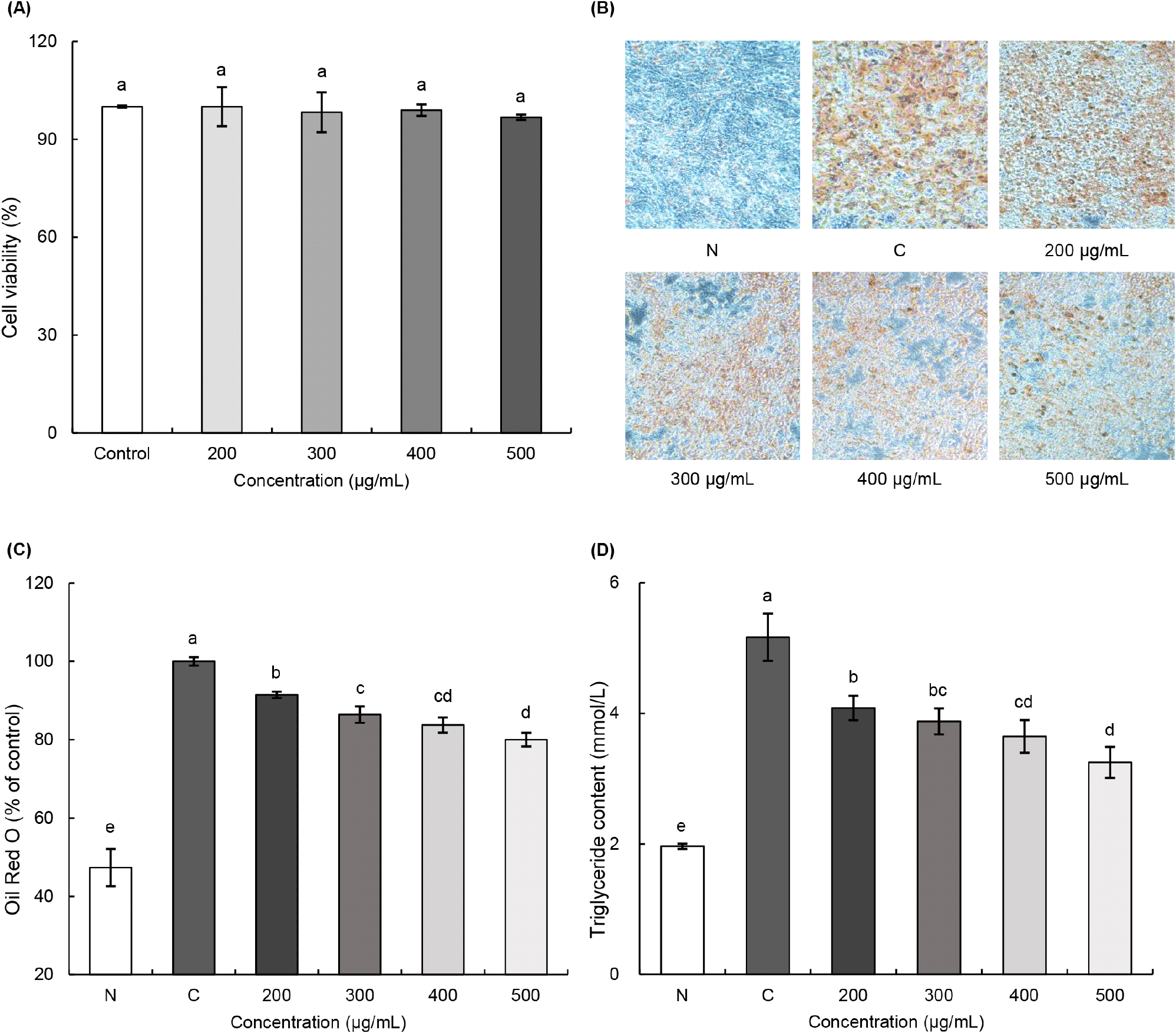
Oil Red O 염색을 통해 분화가 유도된 지방세포의 지질을 특이적으로 염색시켰다(Fig. 3B and 3C). 미분화인 N군과 비교하여 분화를 유도한 C군에서 붉게 염색된 지방세포의 수가 두드러지게 증가하였다. 반면 토마토 콤부차의 처리 농도가 높아질수록 지질 축적은 점차 감소하는 경향을 보였다. 토마토 콤부차 처리 농도별(200, 300, 400, 500 μg/mL)로 각각 8.54%, 13.59%, 16.26%, 19.99%의 지질축적 억제 효과를 보여, 농도 의존적으로 유의적인 감소가 확인되었다(p<0.05). 또한 중성지방 함량 측정 결과에서도 N군에 비해 C군에서 현저하게 증가한 것으로 나타났다(Fig. 3D). 토마토 콤부차의 처리를 통해 농도 의존적으로 중성지방 함량이 감소하는 것으로 확인되었다. 특히 토마토 콤부차 500 μg/mL 농도의 중성지방 수치는 C군에 비해 37.14% 감소하였다. 선행 연구에 따르면, 폴리페놀 화합물과 같은 생리활성을 함유한 토마토 식초는 Oil Red O 염색과 중성지방 함량 분석에서 우수한 지질 축적 억제 효과가 확인되었다(Lee 등, 2013). Oh 등(2024)은 모시잎 에탄올 추출물을 첨가한 산업용 배지에서 배양한 Lactobacillus plantarum 발효액이 발효 전보다 지질 축적을 감소시켜 항비만 효과를 높일 수 있다고 보고하였다. Pyo 등(2022)은 아세트산만을 함유한 식초가 3T3-L1 전구지방세포에서 지방세포의 분화와 분화 과정 중 지질 축적을 억제하는 효과가 있음을 확인하였다. Rocha 등(2016)은 catechin 및 quercetin 등 폴리페놀을 함유한 녹차 추출물을 섭취한 비만 유도 생쥐에서 AMPK 경로가 활성화되어 p-AMPK와 지방산 합성의 속도 조절 효소인 acetyl-CoA carboxylase (ACC)의 인산화가 증가함으로써 지방 합성이 억제되고, 지방 분해 효소인 hormone-sensitive lipase (HSL)와 지방산 산화 효소인 carnitine palmitoyltransferase-1β (CPT1β)의 발현이 증가하며, 지방세포 분화 관련 전사인자인 peroxisome proliferator-activated receptor-γ (PPAR-γ)의 발현이 억제되어 결과적으로 지질 축적이 감소하고 항비만 효과가 나타났다고 보고하였다. 종합적으로, 토마토 콤부차에 함유된 아세트산 등 유기산, catechin과 quercetin을 포함한 폴리페놀 성분, 그리고 Lactobacillus plantarum에 의한 발효 과정이 복합적으로 작용하여 지방세포 분화와 지질 합성을 억제한 것으로 판단된다. 또한 토마토 콤부차 역시 유사한 기전을 통해 AMPK 경로를 활성화하고, 지방합성 억제(ACC 억제), 지방산 산화 촉진(CPT1β 활성화), adipogenic transcription factor 억제(PPAR-γ 억제) 등을 유도하여 항비만 효과를 나타냈을 가능성이 있다. 향후에는 이러한 세포 수준의 결과를 분자생물학적 분석을 통해 확인함으로써, 토마토 콤부차의 항비만 기전을 보다 명확히 규명할 필요가 있다.
4. 요약
본 연구는 토마토를 기반으로 한 발효음료의 기능성 소재화를 목적으로, 녹차를 함유한 토마토 발효액과 바나나를 기질로 한 유산 발효액을 혼합하여 발효 ․ 숙성시킨 토마토 콤부차의 품질특성과 생리활성을 평가하였다. 토마토 콤부차의 이화학적 특성 분석 결과, 당도는 4.5 °Brix, pH는 3.12, 총산도는 3.02%로 확인되었으며, 유기산 및 총폴리페놀 함량은 토마토 발효액과 바나나 유산 발효액보다 높은 수준을 나타냈다. DPPH radical 소거능은 다른 발효군보다 높게 측정되었으며, ABTS∙+ radical 소거능은 85% 이상으로 확인되었다. 환원력은 positive control군과 유사한 수준을 보였고, hydrogen peroxide 소거 활성에서도 90% 이상의 높은 활성을 유지하였다. 또한 토마토 콤부차의 tyrosinase 억제 활성은 83% 이상으로 나타났으며, 발효 ․ 숙성 후에도 높은 활성을 유지하였고, 3T3-L1 전구지방세포에서 세포독성이 나타나지 않는 농도 범위 내에서 처리 시 분화 과정 중 지질 축적이 유의적으로 억제되었다. 이상의 결과를 종합하면, 풍부한 유기산 및 폴리페놀, 플라보노이드를 함유한 토마토 콤부차는 항산화, tyrosinase 억제, 지질 축적 억제 효과를 나타내는 기능성 발효음료로 평가되며, 이는 기능성 식품 소재로 활용될 수 있는 가능성을 제시한다.










