1. 서론
코로나19 팬데믹 이후 전 세계적인 사회구조 변화는 식품 소비 패턴에도 큰 영향을 미쳤으며, 대표적 변화의 하나로 가공식품 소비의 급증을 꼽을 수 있다. 외식 물가의 지속적인 상승과 건강에 대한 관심 증대는 ‘집밥’ 수요 증가로 이어졌고, 이로 인해 국내 가공식품 시장은 빠르게 성장하고 있다. 가공식품은 다양성, 편의성, 맛, 건강 등 여러 측면에서 제품 개선이 이루어지고 있으며, 그 시장 규모 또한 지속적으로 확대되고 있다(Lee, 2017). 북미는 전 세계 HMR 식품 소비의 38% 이상을 차지하며 최대 시장으로 평가된다. 아시아-태평양 지역은 약 30%의 점유율을 보이고 있으며, 그중 한국은 연간 280만 톤 이상의 HMR 제품을 소비하는 주요 국가로 알려져 있다(Market Growth Reports, 2025). 이에 따라 다양한 형태의 HMR 제품이 개발되고 있으며, ready to eat (RTE), ready to heat (RTH), ready to cook (RTC), ready to serve (cooked food for delivery, RTS)의 세분화된 제품군이 출시되고 있다(Costa 등, 2001).
가공식품 소비 증가에 따라 제품의 영양성분 정보에 대한 수요 또한 증가하고 있으며, 이에 따라 여러 국가에서는 가공식품 영양표시 의무화 제도를 시행하고 있다. 미국, 일본, EU 등 36개국에서는 국민 건강 보호를 목적으로 영양표시를 의무화하고 있으며, 우리나라도 2026년부터 단계적으로 이를 도입할 예정이다(Ministry of Food and Drug Safety, 2024). 그러나 현재까지의 영양표시는 열량, 나트륨, 탄수화물, 당류, 지방, 단백질, 콜레스테롤 등 다량 영양소(macronitrients) 중심으로만 이루어지고 있으며, 비타민이나 무기질 등 미량 영양소(micronutrients)에 관한 정보는 부족한 실정이다. 특히 가공식품 시장의 급속한 성장에도 불구하고, 이러한 제품에 대한 미량영양소에 대한 정보 구축은 매우 미흡한 실정이다.
우리나라의 대표적인 식품성분 정보 제공 시스템인 국가표준식품성분표는 1970년 농촌진흥청에서 초판이 발행된 이후 5년 주기로 개정되고 있으며, 농수산자원 및 가공식품의 영양성분 정보가 지속적으로 갱신되고 있다(Kim 등, 2011). 그러나 최신판인 제9개정판 기준으로 수록된 성분의 약 83%는 미국, 일본 등의 국외 자료를 인용하고 있어 국내 실정에 맞는 데이터베이스 구축의 필요성이 제기되고 있다(Park 등, 2018).
엽산은 수용성 비타민 B군 중 하나로, 녹색 채소나 두류에 풍부하게 함유되어 있으며, 포유류의 필수 섭취 성분으로 알려져 있다(Nazki 등, 2014). 한국 식단은 채소 섭취가 풍부하기 때문에 일반적으로 성인의 엽산 섭취가 큰 문제로 여겨지지 않지만, 임산부나 수유부의 경우 엽산 결핍이 빈혈 및 태아 신경관 결손 등의 건강 위험을 초래할 수 있어 보충 섭취의 필요성이 강조되고 있으며, DNA 합성과 메틸화 반응에 관여하는 필수 보조인자로 알려져 있다(Bertuzzi 등, 2019; Chang 등, 1993; Han과 Hyun, 2022; Kennedy 등, 2010).
식품 잔존율(retention)은 원재료(raw food)를 가공 및 조리 하였을 때 보존되는 영양소를 비율로 나타내며, 원재료의 조리방법, 수분, 저장조건 등 다양한 외부요건들이 영양소 잔존률에 큰 영향을 주는 것으로 알려져 있다. 개인 및 집단의 영양소 섭취량을 정확하게 파악하기 위해선 조리된 음식의 영양소 함량에 대한 정보가 필요하나 대부분 원재료를 기준으로 영양소 섭취량이 계산되어진다. 따라서 조리 과정에서 발생하는 영양소 손실이나 변화를 보정하기 위해 원재료 무게에 적용할 수 있는 보정계수가 필요하다(Murphy 등, 1975).
본 연구는 시판 중인 국내 가공식품 중 즉석섭취식품(ready-to-serve, RTS) 15종과 즉석조리식품(ready-to-cook, RTC) 26종을 선정하여 이들의 식품 엽산 및 첨가 엽산 함량을 분석하고, 이를 국가식품영양성분 데이터베이스로 구축 및 활용하기 위해 수행되었다. 신뢰성 있는 데이터 확보를 위해 분석법의 유효성을 평가하고, 분석품질관리를 수행함으로써 국가식품영양성분 데이터베이스로서의 신뢰도 확보 및 소비자 활용도 제고에 기여하고자 한다.
2. 재료 및 방법
본 연구에 사용된 41종의 가공식품 시료는 2023년부터 2024년 사이 농촌진흥청으로부터 제공받았다. 시료는 다소비되는 국내 프랜차이즈 즉석섭취식품 및 시판되는 즉석조리식품을 선정하였으며, 균질화된 상태로 냉동 보관되어 배송되었다. 구매 후 조리가 필요한 시료는 다음의 네 조건에 따라 조리 후 균질화하였다. 1) 굽기: 팬에 소량의 기름을 두르고 중불에서 조리, 2) 찌기: 물이 끓은 후 시료를 넣고 뚜껑을 덮은 상태로 5분간 조리, 3) 에어프라이어 조리: 기름을 분사한 후 앞뒷면을 뒤집어가며 조리, 4) 튀기기: 175-190°C의 온도에서 조리. 프랜차이즈 제품은 조리된 상태로 제공되었으며, 모두 동일하게 균질화하여 실험에 사용하였다. 모든 시료는 수령 즉시 냉동 상태(−18°C 이하)로 보관하였고, 분석 직전에 실온에서 해동하여 사용하였다.
엽산 분석을 위한 folic acid 표준품은 Sigma-Aldrich (St. Louis, MO, USA)에서 구입하였다. 엽산 추출에 사용된 효소 중 α-amylase 및 protease는 Sigma-Aldrich에서, conjugase는 Pel-Freeze Biologicals (Rogers, AR, USA)에서 구입하였다. 엽산 정량 분석에 사용된 Lactobacillus casei subsp. rhamnosus (ATCC 7469)는 American Type Culture Collection (Manassas, VA, USA)에서 구입하였다. 배지로는 folic acid casei medium (HiMedia Laboratories Pvt. Ltd., Dindori, Nashik, India), Lactobacilli broth AOAC, Lactobacilli agar AOAC (Difco, Becton-Dickinson, Sparks, MD, USA)를 사용하였으며, 냉장 보관하여 실험에 사용하였다. 실험에 사용된 증류수는 Power Max 정제 시스템(Human Science, Hanam, Korea)을 통해 생산된 초순수 증류수를 사용하였다. 이외 사용된 모든 시약은 GR 등급 이상의 고순도 시약을 사용하였다.
엽산은 자연형 folate (polyglutamate 형태) 및 합성형 folic acid (monoglutamate 형태)에 따라 추출 방법이 달라진다. 자연형 folate는 여러 vitamer가 polyglutamate 사슬로 존재하여 trienzyme(3가지 효소 사용)처리를 통해 monoglutamate 형태로 전환한 후 추출한다. 그러나 합성형 folic acid의 경우 monoglutamate로 단순하게 존재하고 있어 folate conjugase를 제외한 효소 추출을 할 수 있다는 차이점이 있다(Arcot과 Shrestha, 2005). 본 연구에서는 식품의 자연형 엽산을 추출하여 분석에 사용하였다. 엽산 추출은 3가지 효소[protease, α-amylase 및 folate conjugase (chicken pancreas)]를 처리한 trienzyme 추출법을 이용하였다(Chun, 2006). 시료 0.5-1.0 g을 삼각플라스크에 칭량하였으며, 지방이 5% 이상 함유된 시료는 n-hexane을 사용하여 지방을 제거하였다. 이후 시료가 들어있는 삼각플라스크에 phosphate buffer (pH 7.8) 20 mL와 증류수 30 mL를 가한 후 15분간 100°C 항온수조(HB-205WM, 22 L, Hanbaek Scientific, Seoul, Korea)에서 열탕처리 후 실온으로 냉각하였다. 플라스크에 phosphate buffer 10 mL와 2 mg/mL의 농도로 제조한 protease 용액 1 mL를 가한 후 3시간 동안 37°C의 shaking incubator에서 반응시켰다. 반응이 끝난 시료는 100°C의 항온수조에서 10분간 열처리하여 protease 활성을 종료하였다. 삼각플라스크를 냉각시킨 후 toluene 0.5 mL와 α-amylase (20 mg/mL) 1 mL를 가한 후 2시간 동안 37°C의 shaking incubator에서 반응시켰다. 이후 conjugase [5 mg/mL, phosphate buffer (pH7.8)] 용액 4 mL를 가하고 최대 16시간 동안 37°C의 shaking incubator에서 반응시킨 후 100°C 항온수조에서 10분간 가열하여 모든 효소의 활성을 종료하였다. 실온으로 냉각한 추출액은 pH를 4.5로 조정 후 100 mL로 정용하였으며, 여과지(Whatman No. 1, GE Healthcare, Amersham, UK)로 여과하여 추출액으로 사용하였다.
엽산의 정량 분석은 엽산 농도에 따른 Lactobacillus casei의 생육 반응을 기반으로 하는 미생물학적 방법을 이용하여 수행하였다(Park 등, 2017). 엽산에 대한 생육의존성을 갖는 L. casei subsp. rhamnosus (ATCC 7469)는 분석 당일, depletion media (Lactobacilli broth : folic acid casei medium = 1:1, v/v)에 접종한 후 37°C에서 약 6시간 전배양하여 활성화시켜 사용하였다. 시료 추출액 및 L-ascorbic acid 용액(1 mg/mL), 엽산 표준용액(2 ng/mL)은 0.45 μm membrane filter를 이용해 여과한 후 분석에 사용하였으며, 분석에 사용되는 증류수 및 실험 기구는 모두 멸균 상태로 준비하였다. 각 시료 추출액은 멸균 증류수로 희석하여 총 부피가 150 μL가 되도록 6단계로 희석하였으며, 이를 96-well plate에 분주하였다. 이후 각 well에 다음의 배지 혼합액을 추가하였다: folic acid casei medium 15 mL, L-ascorbic acid 용액 150 μL, depletion media 75 μL. 배지 혼합액 150 μL를 각 microplate 96-well에 첨가하여 총 300 μL로 구성하였으며, 37°C 인큐베이터에서 20시간 동안 배양하였다. 배양이 완료된 후 각 well의 균 배양액을 고르게 혼합한 뒤, microplate spectrophotometer (Thermo Fisher Scientific, Vantaa, Finland)를 이용하여 595 nm 파장에서 흡광도를 측정하였다. 정량 분석의 정확도 확보를 위해, 모든 시료는 시료 자체 및 효소 유래 내인성 엽산을 보정하기 위해 공시험(blank)을 병행하여 분석하였다.
분석법 검증은 AOAC (2016)에서 제시된 가이드라인에 따라 수행되었으며, 검증 방법은 다음과 같다. 정밀성(precision) 검증은 QC 시료를 하루에 5회 3반복으로 추출 및 분석하는 repeatability (inter-day precision, RSDr)와 5일간 하루에 한 번씩 3반복으로 추출 및 분석한 reproducibility (intra-day precision, RSDR)를 계산하여 평가하였다. 정확성(accuracy) 검증을 나타내기 위해 표준인증물질(certified reference materials, CRM)인 SRM-3290 (National Institute of Standards and Technology, Gaithersburg, MD, USA)과 BCR-487 (Resource Technology, Laramie, WY, USA)을 분석하였으며, 제시된 인증값에 분석값을 비교하여 정확성을 나타내었다.
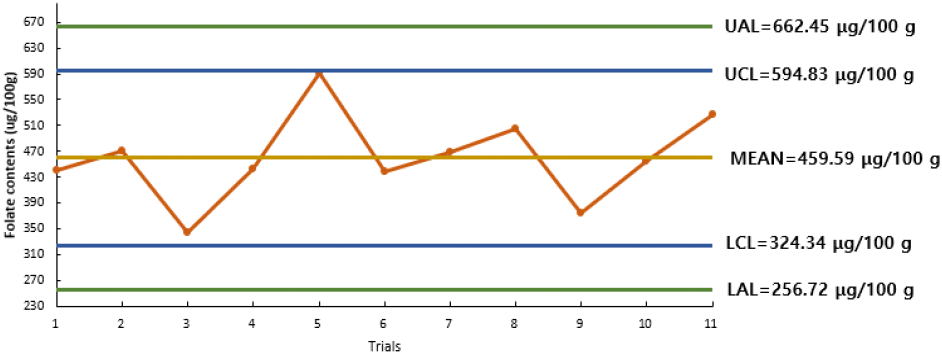
L. casei를 이용한 미생물학적 엽산 정량법에 대한 분석품질관리는 시료의 엽산 함량을 분석 시 품질관리(quality control, QC) 시료를 함께 분석하고 QC chart의 관리선을 이용하여 분석 품질을 평가 관리하였다. QC chart 기준선은 상대표준편차가 5% 이내인 10개의 QC 분석데이터를 기반하여 설정하였으며, 관리 상 · 하한선(upper and lower control line, UCL & LCL)과 조치 상 · 하한선(upper and lower action line, UAL & LAL)을 설정하여 분석데이터의 품질관리에 적용하였다. 관리에 사용된 기준선 설정식은 다음과 같다.
3. 결과 및 고찰
본 연구에서는 L. casei를 이용한 미생물학적 방법을 통해 가공식품의 엽산 함량을 정량하였으며, 분석법의 정밀성 평가를 위해 반복 측정 시 변동계수(coefficient of variation, CV)를 산출하였다. 그 결과, 실험 내 반복 정밀성을 나타내는 RSDr은 2.63%, 실험 간 반복 정밀성을 나타내는 RSDR은 9.66%를 나타내었다(Table 1). 이는 AOAC (2016) Guideline에서 제시한 기준(RSDr≤16%, RSDR≤8% 수준)과 비교할 때 수용 가능한 범위 내에 있으며, 특히 RSDr의 값은 3% 미만으로 매우 양호한 정밀성을 나타내었다. 이러한 결과는 미생물학적 분석법의 한계로 지적되어 온 정밀도 문제를 숙련된 분석 프로토콜을 통해 극복할 수 있음을 보여준다 하겠다.
| Analytes | Repeatability (RSDr)1) (μg/100 g) | Reproducibility (RSDR)2) (μg/100 g) | ||
|---|---|---|---|---|
| Mean±SD3) | CV4) (%) | Mean±SD | CV (%) | |
| Folate | 448.90±11.79 | 2.63 | 445.17±43.01 | 9.66 |
이와 유사하게 Ndaw 등(2001)은 엽산과 같은 미량 영양소 분석에서 미생물학적 분석법이 기기 분석법에 비해 정밀성이 낮을 수 있으나, 균주의 품질관리와 표준화된 전처리 과정이 이를 보완할 수 있다고 보고하였다. 본 연구는 L. casei 배양 조건, 시료 희석 단계, 배양 시간 등 주요 변수들을 표준화하여 적용하였으며, 반복성과 재현성이 확보되었음을 확인하였다.
L. casei를 이용한 엽산 분석법의 정확성 검증을 위해 표준인증물질(standard reference materials, SRMs)을 분석하였으며, 그 결과는 Table 2와 같다. SRM 3290의 엽산 분석 값은 579.11 μg/100 g, BCR-487의 분석값은 1,282.76 μg/100 g을 나타내어, 해당 인증값 대비 96.5%의 회수율을 보였다. AOAC (2016) Guideline에서는 분석 대상 성분의 함량이 1 μg/100 g 수준일 경우 수용 가능한 회수율 범위를 70-125%로 제시하고 있으며, 본 연구의 회수율은 그 범위 내에서도 높은 수준(>95%)의 정확성을 나타냈다.
| Samples | Reference value3) (μg/100 g) | Analysis value4) (μg/100 g) | Recovery5) (%) |
|---|---|---|---|
| Mean±SD | |||
| SRM 32901) | 600.00±100.00 | 579.11±10.51 | 96.52 |
| BCR-4872) | 1,330.00±130.00 | 1,282.76±11.52 | 96.45 |
정확성에 대한 이와 유사한 결과는 Aiso와 Tamura (1998)의 연구에서도 확인되었다. 해당 연구에서는 소고기, 빵, 우유, 시금치에 amylase와 protease의 효소처리를 통해 엽산 함량의 회수율이 50% 이상 증가하였다고 보고하였으며, 이는 엽산 분석 시 전처리 단계의 효소 사용이 회수율 향상에 중요한 요소인 것으로 나타났다. 본 연구에서도 동일한 전처리 효소 과정을 적용하였는데, 이것이 높은 정확성 확보에 기여한 것으로 판단된다.
엽산은 식품 중 다양한 형태로 존재하고 생물학적 활성도와 분석 감도가 낮아 정량 분석이 어려운 비타민으로 분류된다. 특히 자연 식품에서의 엽산은 식물세포 구조 내에 존재하거나 다른 영양소와 결합되어 있기 때문에 정확한 추출 및 정량을 위해서는 효소 처리, 적절한 추출 조건, 생물학적 반응 기반의 분석법이 요구되며, 다양한 식품 매트릭스에 존재하는 엽산 분석법으로 미생물학적 정량법이 권장되고 있다(DeVries 등, 2005). AOAC에서도 엽산 분석의 표준법으로 미생물학적 분석법(L. casei assay)을 권장하고 있는데, 이는 L. casei가 다양한 엽산 유도체에 모두 반응할 수 있다는 장점을 가지기 때문에 정확한 정량에 적합하기 때문이다. 그러나 균주의 생육 상태, 배지 조건, 배양 시간 등의 변수는 분석 데이터의 오차를 키울 수 있는 요인이 되므로 정밀한 분석품질 관리 및 분석 숙련도가 요구된다. 이러한 특성으로 인해 일반적으로 미생물학적 분석법은 기기 정량법에 비해 정밀성 및 정확성이 부족할 수 있다. 그러나 본 연구에서는 분석 전 품질관리 항목(표준곡선 작성, 공시험 포함, 배양조건 모니터링)을 체계적으로 수행함으로써, 기기 분석법에 비견될 수 있는 수준의 정밀성과 정확성을 확보하였다. 이는 국내 가공식품의 엽산 함량 분석 및 이에 대한 국가식품영양성분 데이터베이스 구축에 있어, 미생물학적 분석법의 활용이 충분한 신뢰성을 확보할 수 있음을 나타낸다 하겠다.
본 연구에서는 L. casei를 이용한 엽산 정량 분석의 신뢰성을 지속적으로 확보하기 위해 분석품질관리 지표로 QC chart를 활용하였다. QC chart는 분석 수행 과정에서 발생할 수 있는 내부적(기기 상태, 시약 안정성 등) 및 외부적 요인(온도, 배양 조건 등)에 의한 변동을 모니터링함으로써, 분석 시스템의 이상 여부를 조기에 식별하고 데이터를 신뢰성 있게 유지하는 도구로 사용된다. 본 연구에 사용된 엽산 분석의 QC chart는 Fig. 1에 제시하였다. QC 시료는 각 분석 시점마다 함께 측정되었으며, 해당 값이 사전에 설정된 조치 상한선(UCL) 또는 조치 하한선(LCL)을 초과하는 경우에는 분석 시스템 점검 및 검체 시료에 대한 재분석을 실시하였다. 이러한 조치는 잘못된 분석 결과의 국가데이터베이스로의 사용을 방지하고, 분석 결과의 품질과 정확도를 보장하기 위한 중요한 검증 절차라 할 수 있다. Jung 등(2019)은 미생물학적 방법을 이용한 엽산 분석에서 QC 관리를 수행하였고, 분석 기간 중 1회를 제외한 모든 QC 값이 UCL과 LCL 내에 분포하였다고 보고하였다. 또한 기준선을 초과한 경우, 해당 결괏값을 배제하고 전처리 및 분석 과정을 재정비한 후 재측정을 수행하였다고 하였다. 이는 미생물 기반 정량 분석에서 QC chart의 효과적 활용 사례로 볼 수 있으며, 본 연구의 분석품질관리 방법과 유사한 접근법임을 알 수 있다. 본 연구에서는 총 11회에 걸친 QC 분석을 수행하였으며, 모든 분석 결과가 설정된 UCL 및 LCL 범위 내에 포함되는 것으로 나타났다. 이는 국가식품영양성분 데이터베이스 구축과 같이 장기간 동안 다종류 및 다수의 시료를 수거 및 분석하는 방식의 실험 디자인을 적용해야 하는 구조적 특수성에서도 일관된 분석품질을 유지할 수 있도록 관리할 수 있는 효과적인 도구가 될 수 있으며, 본 연구에서는 전 분석 기간 동안 분석 조건의 재현성이 확보되었음을 객관적으로 나타낼 수 있는 자료라 하겠다. 이는 본 연구에서 분석된 모든 시료의 엽산 정량 데이터가 신뢰할 수 있는 환경과 조건 하에서 분석되었으며, 분석된 시료의 엽산 함량은 국가식품영양성분 데이터베이스로 활용하기에 충분한 신뢰성을 확보하고 있음을 입증한다 하겠다.
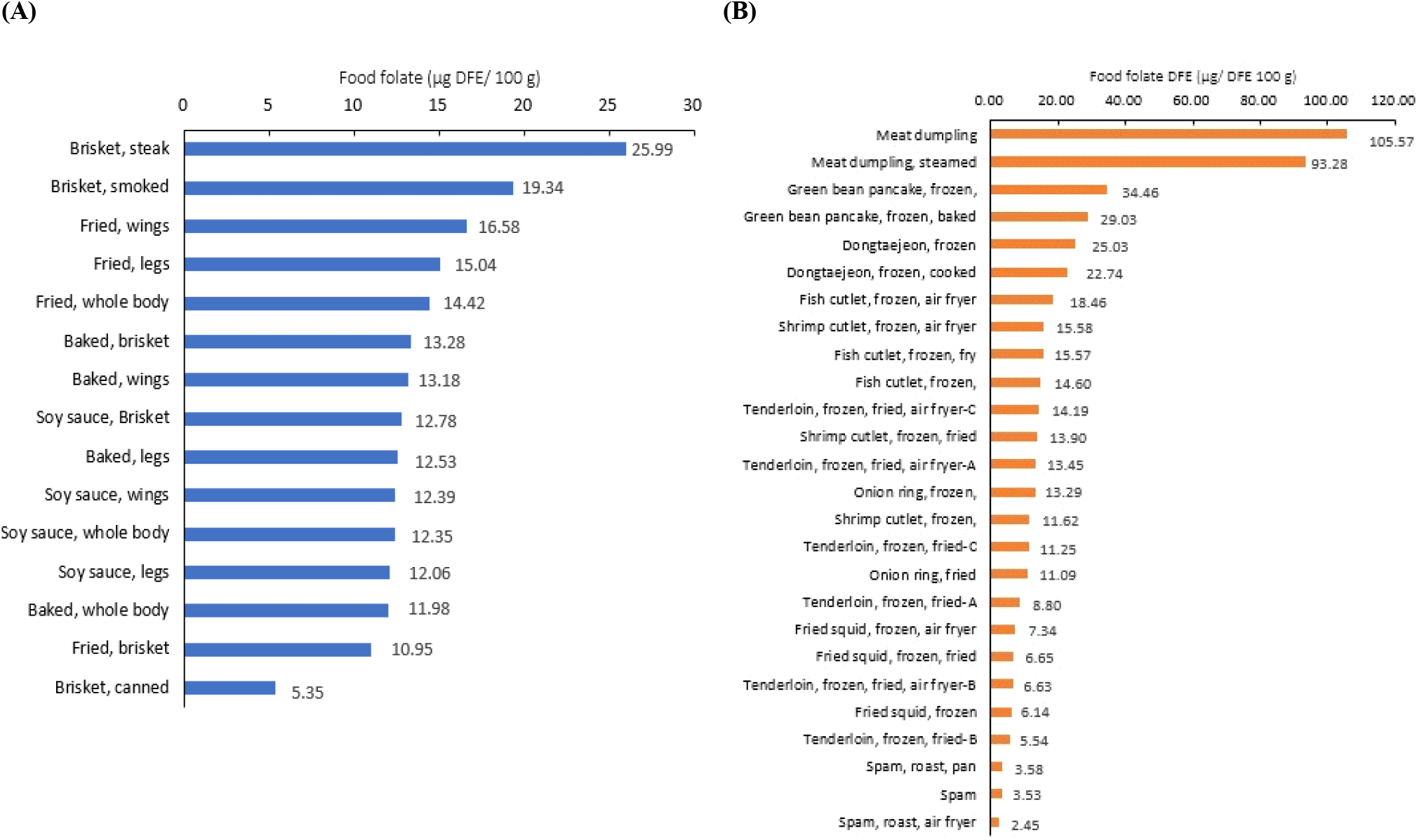
본 연구에서는 국내 시판중인 RTC 즉석 가공식품 26종을 대상으로 식품 엽산(food folate) 및 첨가 엽산(folic acid) 함량을 분석하고, 조리방법에 따른 함량 변화 및 processing factor를 산출하였다. 시료의 엽산 함량은 최소 2.45 μg/100 g(스팸, 구운 것, 에어프라이어 조리)에서 최대 45.37 μg/100 g(만두, 생것)의 범위를 보여 약 19배 차이를 나타내었는데(Table 3), 이는 가공식품의 원재료, 조리 상태, 첨가물 유무 등에 따라 엽산 함량이 크게 달라질 수 있음을 보여준다. 흥미롭게도, 만두(생것 및 찐 것)에서는 첨가 엽산이 각각 35.14 μg/100 g 및 33.51 μg/100 g 수준으로 검출되었으며, 나머지 시료에서는 첨가 엽산이 검출되지 않았다. 이는 만두 제조 시 사용된 수입산 강화밀가루의 영향으로 해석되며, 미국과 호주 등지의 엽산 강화 정책과 관련이 있다. 미국과 캐나다를 비롯한 여러 국가에서는 신경관 결손증 예방을 목적으로 곡류 가공식품에 엽산 첨가(fortification)를 법적으로 의무화하고 있다. 미국 FDA는 1996년부터 곡물 기반 식품(밀가루, 시리얼 등)에 엽산을 강화하도록 규정하였으며, 이러한 조치는 실제로 신경관 결손증의 발생률을 현저히 낮추는 데 기여하였다(Crider 등, 2011; De Wals 등, 2007). Boen 등(2009)은 미국 내에서 판매되는 강화 밀가루 기반 가공식품(피자, 마카로니, 빵 등)의 첨가 엽산 함량이 34-200 μg/100 g 수준임을 보고하였으며, 피자 10종의 평균 엽산 함량은 34 μg/100 g으로 나타났다. 이는 본 연구에서 확인된 만두 시료의 첨가 엽산 함량(33-35 μg/100 g)과 유사한 수준이다. 분석에 사용된 만두 제품은 호주산 및 미국산 밀가루 사용이 명시되어 있었으며, 이는 엽산이 강화된 밀가루의 사용 가능성을 시사하며, 국내 시판 가공식품에서도 강화 엽산의 존재를 일부 확인할 수 있었다.
닭고기의 안심, 튀긴 것은 에어프라이어 조리에 따른 유의적 차이를 나타냈으며(p<0.05, p<0.001), 에어프라이어 조리 후의 시료에서 식품 엽산 함량이 증가하였고, processing factor가 1.20-1.53으로 함량이 높아지는 경향을 보였다(Table 3). 이는 수분 증발에 따른 농축 효과 또는 기름 사용량 감소에 따른 영양소 보존 가능성을 시사한다. 예를 들어, “Tenderloin, frozen, fried-A”는 wet basis에서 8.80 μg/100 g, dry basis에서 20.89 μg/100 g의 엽산 함량을 보였으나, 동일 시료의 에어프라이어 조리 후에는 13.45 μg/100 g, 25.76 μg/100 g으로 증가하였다. 일부 시료는 반복 측정 시에도 1.00을 초과한 processing factor를 보였으며, 이는 조리 손실보다 수분 증발로 인한 상대적 농축이 우세한 경우로 해석된다.
한편, 해산물류(seafood) 시료는 조리 전·후 식품 엽산 함량 차이가 더 명확하게 나타났다(Table 3). 동태전(dongtaejeon)의 경우, 생 시료 대비 조리 후 함량이 감소하였으며, processing factor는 0.91로 나타나 조리 중 엽산 손실이 확인되었다. 반면, 오징어튀김, 새우커틀릿 및 생선까스는 조리 후 엽산 함량이 증가하였으며, 튀기기와 에어프라이어 조리에 따른 함량 변화가 유의적인 차이를 나타내었다(p<0.05). 이는 조리 시 사용된 기름의 양, 조리 시간, 온도 등에 따라 영향을 받을 수 있으며, 해산물의 지방함량과 수분함량이 결과에 영향을 미쳤을 것이라 사료된다.
스팸과 같은 통조림 햄류 제품은 전체적으로 가장 낮은 식품 엽산 함량(2.45-3.58 μg/100 g)을 보였으며, 조리 후 processing factor는 0.69-1.01로 조리 시 엽산 손실이 가장 큰 편이었다. 이는 고지방 식품의 가열에 따른 엽산의 분해와 유실 가능성을 시사한다.
식품군 전반적으로 조리 전후 식품 엽산 함량은, 조리 방법(굽기, 찌기, 튀기기, 에어프라이어)에 따라 일정한 증감 경향은 확인되지 않았다. 예를 들어, 동태전의 경우 생것(25.03 μg/100 g)이 조리 후(22.74 μg/100 g)보다 높았으나, 닭고기 안심-A은 생것(8.80 μg/100 g)보다 에어프라이어 조리 후(13.45 μg/100 g) 식품 엽산 함량이 오히려 증가하였다. 이러한 결과는 선행 연구 결과와도 일치한다. Park 등(2017)은 조리법에 따라 버섯의 엽산 잔존율이 달라질 수 있으며, 일부 시료에서는 오히려 조리 후 엽산 함량이 증가하는 현상을 보고하였다. 또한 Johansson 등 (2008)은 냉동 채소 제품을 다양한 조리 방식(가스레인지, 전자레인지, 오븐 등)으로 처리한 후 엽산 함량을 분석하였으나, 조리 방법에 따른 명확한 패턴은 확인되지 않았다고 보고하였다. 본 연구에서도 생것의 시료를 조리 및 가열하였을 때 검출되는 엽산 패턴이 일정하지 않았으며, 이는 가공식품이 조리됨에 따라 엽산 함량이 파괴되는 시료가 있는 반면, 오히려 엽산 함량이 높아지는 시료도 있는데 이는 식품 내 엽산의 분포 형태, 수분 증발, 농축 효과 등의 복합적 요인에 의해 함량 변화가 발생함을 시사한다 하겠다.
본 연구에서 사용한 15종의 즉석섭취식품(ready to serve, RTS) 가공식품의 엽산 함량 및 processing factor는 Table 4에 나타내었다. 조리되어 배달되는 치킨과 같은 RTS 식품류는 즉석편의 식품류로 분류되고 있으며, ready to eat (RTE)과 같이 가열과 같은 사전 조리과정이 필요하지 않고 식품을 구매하여 바로 소비가 가능한 식품이다(Costa 등, 2001). RTS 가공식품의 식품 엽산은 5.35-25.99 μg/100 g을 나타냈으며, 최소 함량(닭가슴살, 통조림)과 최대 함량(닭가슴살, 스테이크)은 약 4.8배의 차이를 나타냈다. 또한 시료 중 첨가 엽산(folic acid)은 검출되지 않았다. 국가표준식품성분표(RDA, 2020)에 따르면 닭 부위별 식품 엽산의 함량은 가슴, 생것은 10 μg/100 g, 다리, 생것은 23 μg/100 g으로 보고되어있다. 본 연구에서 분석한 프랜차이즈 치킨의 엽산 함량은 11.98-16.58 μg/100 g을 나타내며, 국가표준식품성분표에서 제시된 생것 함량의 범위와 비슷한 엽산 함량을 나타내어 가공 시에도 큰 차이를 나타내지 않는 것으로 사료된다. Ji 등(2019)은 패스트푸드와 가공식품의 엽산 함량을 분석하였으며, 이 중 프랜차이즈 치킨은 43.4-58.2 μg/100 g의 함량을 나타내는 것을 확인하였다. Lee 등(2008)은 사료 단백질 및 에너지 수준에 따라 닭의 혈중 단백질, 포도당, 총 콜레스테롤의 변화가 있다고 보고하였으며, Lee 등(2021)은 닭의 품질 특성이 생산 단계에 따라 다르게 나타난다고 하였다. 이는 사육 환경, 섭취 사료 영양성분 등과 같은 많은 요인의 따라 닭의 영양성분이 달라질 수 있음을 나타내며, 선행연구와의 엽산 함량 차이가 나는 것 또한 위의 이유로 인한 것이라 사료된다.
식이 엽산 당량(dietary folate equivalent, DFE)은 자연적으로 존재하는 식품 속 엽산과 생체이용률이 더 높은 합성 엽산 간의 흡수율 차이를 반영하여 나타내는 수치로, 엽산 섭취량의 평가 시 DFE 기준의 사용이 권장되고 있다(Suitor, 2000). 본 연구에서 사용한 41종의 가공식품의 식이 엽산 당량은 Fig. 2에 나타냈으며, 식품 중 식품 엽산(folate)과 첨가 엽산(folic acid)의 생체이용률을 고려하여 계산하였다(Han과 Hyun, 2022). 먼저 15종의 RTS 중 닭가슴살, 스테이크에서 가장 높은 DFE를 나타냈으며(25.99 μg DFE/100 g), 제일 낮은 DFE를 나타낸 닭가슴살, 캔은 5.35 μg DFE/100 g으로 약 5배의 차이를 나타냈다. 조리가 필요한 RTE에선 식품 엽산과 첨가 엽산이 검출된 만두(생것, 찐 것)에서 제일 높은 DFE를 나타냈으며(105.57 μg DFE/100 g, 93.28 μg DFE/100 g), 제일 낮은 당량을 나타낸 스팸(생것, 굽기, 에어프라이어)과 비교하였을 때 약 31배의 차이를 나타냈다. 2020년 한국인 영양소 섭취기준(MOHW and KNS, 2020)에 따르면 성인 남녀의 엽산 권장섭취량은 400 μg DFE/100 g, 임산부 및 수유부는 520-620 μg DFE/100 g으로 권장하고 있다. 식사 시 가공식품 위주의 식단만으로는 일일 권장섭취량을 충족하기 어려울 수 있으며, 다양한 식품군이 포함된 균형 잡힌 식단을 구성하여 섭취하는 것이 일일 엽산 권장섭취량을 충족할 수 있을 것으로 보인다.
국가식품영양성분 데이터베이스에서 제공하는 데이터는 일반적으로 섭취 시 식품의 형태, 즉 습중량 기준(wet basis, w/w)으로 산출된 100 g 중의 엽산 함량 수준이다. 일반적으로 엽산은 열과 수분에 민감하여 조리 중 손실이 발생할 수 있으며, 조리로 인한 수분 변화는 잔존하는 엽산 함량의 해석에 중요한 영향을 미칠 수 있다. 실제로 원재료를 조리하였을 때 엽산 잔존율이 감소한다는 몇몇 연구결과들이 나와있으며(Maharaj 등, 2015; McKillop 등, 2002), 이는 즉석식품을 가공할 때 나타나는 엽산 잔존율과도 연관이 있을 것으로 사료된다. Table 3과 4는 실제 섭취하는 식품 상태에서의 엽산 함량을 나타내는 습중량 기준 산출값으로 조리 후 시료 매트릭스의 특성에 따라 잔존 수분 함량에 따른 변동을 반영하기 어려우므로, 조리 후 잔존하는 실제 엽산 잔존율 평가를 위해서는 건조중량(dry basis) 기준에서의 함량 비교 평가가 필요하다. Table 5는 건조중량으로 환산된 엽산 함량으로, 일부 시료에서는 습중량 기준과 달리 조리 후 엽산 손실이 두드러지게 나타나는 것을 볼 수 있다. 예를 들어, 생선까스(냉동) 시료의 습중량 기준 엽산 함량은 14.60 μg/100 g이었으나, 조리 후 에어프라이어 처리 시 18.46 μg/100 g으로 증가하였다. 그러나 건조중량 기준으로 환산한 결과, 에어프라이어 조리 시의 processing factor는 0.82, 튀기기 조리 시에는 0.71로, 실질적인 엽산 손실이 발생했음을 확인할 수 있었다. 이러한 결과는 조리 시 수분 변화가 엽산 농도 해석에 중대한 영향을 미친다는 점을 보여준다. 일반적으로 식품성분 데이터는 소비자가 섭취하는 상태로의 식품 상태에서의 정보를 반영하기 때문에 습중량 기준으로 제공되지만, 건조중량 기준은 식품 간 성분 비교 시 수분의 영향을 배제할 수 있어 정밀한 비교 및 식품가공 연구에서 널리 활용된다. 국가 식품영양성분 데이터베이스는 일반인 뿐만 아니라 전문가들도 활용하는 다양한 수요자에게 정보가 제공되므로 데이터를 제공 시 습중량 정보와 함께 건조중량 데이터 정보를 병행 수록하고, 이에 대한 용어와 사용 가이드를 함께 제공하는 방법에 대한 고려도 필요할 것으로 보여진다.
4. 요약
본 연구는 코로나19 이후 증가하고 있는 국내 가공식품 소비에 대응하여, 시판 중인 즉석섭취식품 및 즉석조리식품(ready-to-serve, ready-to-cook) 41종의 엽산 함량을 분석하고, 해당 데이터를 국가 식품영양성분 데이터베이스 구축에 활용하고자 수행되었다. 엽산은 체내 세포 대사의 기능에 관여하는 필수적인 보조 인자로 결핍 시 여러 건강 문제를 초래하고, 태아의 경우 신경 결손을 일으킬 수 있어 임산부에게 특히 높은 수준으로 요구되는 수용성 비타민이다. 본 연구에서 적용한 미생물학적 분석법을 검증하여 데이터의 신뢰성을 확보하고, 이를 기반으로 국내에서 시판되는 즉석섭취식품 및 즉석조리식품 41종의 엽산 함량을 분석하였다. Trienzyme 추출 및 L. casei 활용 미생물학적 분석법에 대한 검증 결과, 정밀성(RSDr 2.63%, RSDR 9.66%)과 정확성(recovery 96.5%)이 모두 AOAC 가이드라인 기준을 충족하였다. QC chart 기반 분석품질관리를 통해 모든 시료 분석 회차에서 분석값이 UCL 및 LCL 수준 이내를 유지하여 시료 분석이 검증된 수준으로 관리되어 수행되었음이 확인되었다. 분석 결과, 41종 모든 시료에서 엽산이 검출되었으며, 함량 범위는 2.45-45.37 μg/100 g로, 식품 간 최대 19배의 차이를 나타냈다. 특히 만두(생것, 찐 것)에서 첨가 엽산이 검출되었으며, 이는 해당 제품이 강화 엽산이 함유된 수입 밀가루를 사용했을 가능성을 시사한다. 조리 방법별 엽산 변화는 일정한 경향을 보이지 않았으며, 일부 시료에서는 조리 후 엽산 함량이 오히려 증가하는 현상도 관찰되었다. 또한 습중량(wet basis) 기준과 건조중량(dry basis) 기준 비교 결과, 조리 후 수분 변화에 따라 엽산 함량 해석이 달라질 수 있음을 확인하였으며, 연구 및 가공 목적의 영양 비교에는 dry basis 기준의 병행 제시 필요성도 확인되었다. 본 연구는 국내 다소비 가공식품의 엽산 함량 데이터를 제시함과 동시에, 신뢰성 있는 미생물학적 분석법의 검증과 활용 사례를 제공하였으며, 향후 국가식품성분 데이터베이스의 고도화 및 영양정책 수립에 기초 자료로 활용될 수 있을 것이라 사료된다.










