1. 서론
활성산소종(reactive oxygen species)은 superoxide radical (O2•−), hydroxyl radical (•OH), singlet oxygen (1O2), hydrogen peroxide (H2O2) 등을 포함하며, 불완전한 전자 구조로 인해 핵산, 단백질, 지질을 산화시켜 세포 기능 이상과 만성 염증을 유발시킨다(Van den Ende 등, 2011). 정상적인 미토콘드리아 호흡 과정 중 최대 5%가 활성산소종으로 전환되는 것으로 추정되며(Zwart 등, 1999), 흡연, 과도한 음주, 자외선, 스트레스 등 외인성 요인 또한 활성산소종의 생성을 촉진시킨다(Crack과 Taylor, 2005). 인체는 superoxide dismutase (SOD), catalase, glutathione peroxidase 등 내인성 항산화 효소와 glutathione 같은 비효소적 항산화 시스템이 활성산소종을 제거, 해독하지만 노화와 환경적인 스트레스에 따라 이러한 방어 체계가 약화되면 암, 심혈관계 질환, 신경퇴행성 질환 등 다양한 질환이 촉발될 수 있다(Xiao 등, 2017). 이러한 산화적 스트레스로 인한 활성산소종을 억제하고 산화적 손상을 예방하기 위해 hydroxyanisole (BHA)와 butylated hydroxytoluene (BHT)같은 합성 항산화제가 사용되어 왔지만, 장기간 섭취 시 독성과 잠재적 발암성 등이 보고되면서(Jun 등, 2001), 보다 안전성이 확보된 천연 항산화제 탐색이 요구되고 있다. 식물 유래 polyphenol과 flavonoid는 전자 공여, 금속 이온 킬레이션, 항산화 효소 발현 조절 등을 통해 활성산소종을 직접 제거하거나 내인성 방어 체계를 강화하여 활성산소종에 대한 방어 효과를 나타내는 것으로 알려져 있어(Shomali 등, 2022), 천연 항산화 소재로서 주목받고 있다.
센티페드그라스[Eremochloa ophiuroides (Munro) Hack.]는 중국을 기원지로 하는 다년생 C4 잔디로, 주로 동남아시아와 남미에 널리 분포하며 곤충 · 병원균 저항성과 내열 · 내답압성이 뛰어나 사료용과 스포츠 터프용 잔디로 활용되어 왔다(Hanna, 1995; Hanna와 Burton, 1978; Islam과 Hirata, 2005). 최근 식물화학 연구에 따르면, 센티페드그라스 잎에는 maysin, isoorientin, orientin, luteolin 유도체 등 C-glycosyl flavone이 고농도로 축적되어 있는 것으로 보고되었다(Badaboina 등, 2013). 이 가운데 maysin (6-C-glucosyl-2"-O-α-L-rhamnosyl apigenin)은 면역 증진, 지방 축적 억제, 항산화, 항암 활성을 나타내는 핵심 성분으로 알려져 있다(Choi 등, 2014; Lee 등, 2014; Maksimović 등, 2005; Waiss 등, 1979). 더 나아가 γ선 조사 처리 시 maysin 함량이 유의적으로 증가하고(Lee 등, 2011), DPPH radical 및 ABTS radical 소거능이 향상된다는 결과가 보고되었으며(Lee 등, 2011), 고염 스트레스 조건에서도 항산화 효소 활성 및 polyphenol 축적이 유지되어 내염성과 항산화성이 밀접하게 연관됨이 제시된바 있다(Maeda 등, 2011). 현재까지 다양한 천연물의 항산화 활성에 대한 연구가 이루어져 왔지만, C-glycosyl flavone 계열의 생리활성 물질을 고농도로 함유하고 있음에도 불구하고 센티페드그라스의 항산화 소재로서의 기능성 평가는 제한적으로 이루어져 왔다. 특히, 저활용 식물 자원으로서 새로운 기능성 소재 개발 가능성이 매우 높음에도 용매별 화학 조성과 항산화 활성을 체계적으로 비교한 연구는 미흡한 실정이다. 따라서, 본 연구에서는 센티페드그라스에 대한 식품, 의약 또는 기능성 소재로서의 활용 연구를 기존에 보고된 항산화 소재들과 비교하여 차별성과 우수성을 바탕으로 잠재적 기능성 소재로서의 가능성을 평가하고자 하였다.
이에 본 연구에서는, 물, 열수(90°C), 80% 에탄올, 80% 메탄올, 80% 아세톤을 용매로 침지 추출을 수행한 뒤, 각 추출물의 총 polyphenol 및 총 flavonoid 함량과 maysin 함량을 HPLC로 정량하였다. 또한, DPPH radical 및 ABTS radical 소거능과 xanthine 유래 superoxide 소거능을 평가하여, 추출 용매-화학 조성-항산화 효능 간 상관 구조를 규명하고자 하였다. 본 연구 결과는 센티페드그라스 유래 천연 항산화 소재의 최적 추출 조건을 제시함으로써, 기능성 식 · 의약 및 화장품 원료 개발에 과학적 근거를 제공할 것으로 기대된다.
2. 재료 및 방법
본 연구에 사용된 센티페드그라스[Eremochloa ophiuroides (Munro) Hack.]는 ㈜바이오메이신 전용 재배 농지(전북특별자치도 익산시 소재)에서 수확하여 사용하였으며, 수확된 센티페드그라스는 흐르는 물에 세척 후 자연 건조하여 건초로 사용하였다. 센티페드그라스 건초 20 g을 80% 에탄올, 80% 메탄올, 80% 아세톤, 물, 열수(90°C) 400 mL를 용매로 1일간 침지 추출하였으며, 이 과정을 3회 반복하였다. 추출액은 여과지로 여과한 후 50°C 수욕상에서 감압 농축하였으며, 물 추출물의 경우 소량의 에탄올을 단계적으로 첨가하여 농축 효율을 높여주었다. 농축된 시료는 밀봉하고 보관하여 실험에 필요한 시료로 사용하였다.
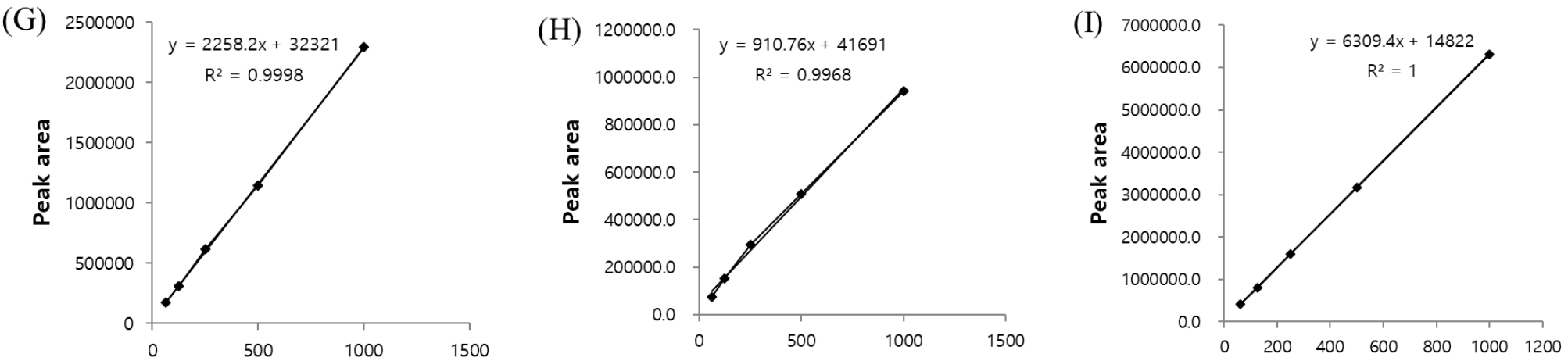
용매별 센티페드그라스 추출물 내 polyphenol 함량은 추출물 5 mg을 1 mL의 추출 용매로 용해하여 분석에 필요한 시료로 사용하였다. Cicco 등(2009)의 방법에 따라 각 시료와 Folin & Ciocalteu 시약을 정확히 동량 혼합한 후 0.1 M의 sodium carbonate 용액 800 μL를 가하여 40°C에서 20분 동안 반응시키고, 10분 동안 냉각시킨 뒤 700 nm에서 흡광도를 측정하였으며, gallic acid를 표준물질로 농도에 따른 일차방정식(y = 0.0009x + 0.0355, R2=0.9988)을 이용하여 총 페놀 함량[mg gallic acid equivalent (GAE)/g]으로 계산하였다. flavonoid 함량 측정은 용매별 센티페드그라스 추출물 시료 1 mL과 5%의 sodium nitrite 용액 30 μL를 혼합하여 정확히 5분 반응시킨 후 10%의 aluminum chloride 용액 30 μL와 1 M의 sodium hydroxide 용액 200 μL를 가하여 510 nm에서 흡광도를 측정하였다(Lee 등, 2012). Flavonoid 함량은 quercetin을 표준물질로 농도에 따른 일차방정식(y = 0.0011x + 0.0836, R2=0.9951)을 이용하여 총 flavonoid 함량[mg quercetin equivalent (QE)/g]으로 계산하여 나타내었다.
Maysin 표준물질은 ㈜바이오메이신에서 센티페드그라스로부터 반복적인 칼럼크로마토그래피를 수행하여 순수한 단일 물질로 분리 정제하고 NMR 및 high-resolution electrospray ionization mass spectrometry 등 분광학적 분석을 수행하여 화합물의 구조를 동정하였다. 용매별 센티페드그라스 추출물 내 maysin의 함량을 분석하기 위해 시료 5 mg을 정밀히 달아 50% 메탄올 1 mL를 첨가한 뒤, 10분간 초음파를 가하여 시료를 용해하였다. 이후 원심분리(10,770 × g, 5 min)하여 상등액을 취해 분석에 필요한 시료로 사용하였다. 분석에 사용된 HPLC는 SPD prominence UV/VIS detector가 장착된 HPLC (LC-20AD, Shimadzu, Kyoto, Japan)를 사용하였으며, 컬럼은 YMC-Pack C18 column (4.6 mm I.D. × 150 mm; particle size 5 μm; YMC Co., Ltd., Kyoto, Japan)을 사용하였다. 컬럼의 온도는 40°C를 유지하였으며 mobile phase는 용매 A (0.1% formic acid가 포함된 물)와 용매 B (acetonitrile)를 분당 1 mL의 유속으로 흘려주었다(Table 1).
용매별 센티페드그라스 추출물의 DPPH radical 소거 활성을 측정하기 위해 시료 50 μL와 에탄올을 용매로 제조한 0.2 mM의 DPPH 용액 200 μL를 96-well plate에 가하여 실온의 암소에서 정확히 30분간 반응시킨 후 microplate reader를 이용하여 517 nm에서 흡광도를 측정하였다(Yoshida 등, 1989). 용매별 센티페드그라스 추출물의 ABTS radical 소거 활성을 평가하기 위해 7.4 mM의 ABTS 용액과 2.6 mM의 potassium persulfate 용액을 혼합하여 실온의 암소에서 24시간 동안 반응시켜 radical을 형성시켰으며, 흡광도의 값이 0.70±0.03이 되도록 phosphate buffered saline (pH 7.4)을 이용하여 적절히 희석하여 사용하였다. 이후, 희석된 ABTS 용액 190 μL와 시료 10 μL를 96-well plate에 가한 후 실온의 암소에서 10분간 반응시키고 microplate reader를 이용하여 732 nm에서 흡광도를 측정하였으며, 대조물질로 catechin을 사용하였다(Re 등, 1999).
용매별 센티페드그라스 추출물의 xanthine과 xanthine oxidase에 의해 생성되는 superoxide radical의 소거 활성을 측정하기 위해 시료 10 μL와 100 μM nitro blue tetrazolium (NBT)와 xanthine (250 μM)을 포함하는 phosphate buffer (pH 7.8, 20 mM)를 혼합하여 5분간 반응시켰다. 이후, xanthine oxidase (0.05 U/mL) 100 μL를 가하여 37°C에서 20분간 반응시킨 후 69 mM의 sodium dodecyl sulfate (SDS)를 가하여 반응을 멈춘 뒤 570 nm에서 흡광도를 측정하였다. Superoxide radical 소거 활성에 대한 측정은 시료와 대조군이 NBT를 환원시키는 정도로 비교하였다(Thuong 등, 2007).
3. 결과 및 고찰
용매별 센티페드그라스 추출물 내 polyphenol 함량을 분석한 결과, 80% 에탄올 추출물이 0.46±0.01 mg GAE/g으로 가장 높았고, 이어 80% 메탄올(0.42±0.01 mg GAE/g), 열수(0.32±0.02 mg GAE/g), 물(0.30±0.01 mg GAE/g), 80% 아세톤(0.28±0.02 mg GAE/g) 순으로 나타났다(p<0.05). Flavonoid 함량 역시 에탄올 추출물이 0.26±0.02 mg QE/g으로 가장 높았으며, 메탄올(0.25±0.02 mg QE/g), 열수(0.17±0.02 mg QE/g), 물(0.17±0.02 mg QE/g), 아세톤(0.12±0.00 mg QE/g) 순으로 유의적 차이를 나타내었다(p<0.05; Table 2). 70-80% 에탄올은 중간 정도의 극성을 가지기 때문에 친수성인 페놀성 수산기와 소수성인 benzopyran 골격을 모두 지닌 polyphenol 및 flavonoid를 효과적으로 용출시키는 용매로 알려져 있으며(Kähkönen 등, 1999), 본 연구 결과도 이와 동일한 경향을 나타내었음을 확인하였다. Kim 등(2018)이 보고한 대나무 잎 추출물, Anokwuru 등(2011)이 보고한 님나무(Azadirachta indica) 추출물 연구에서도 70-80% 에탄올이 물 또는 메탄올, 아세톤 대비 높은 phenolic flavonoids 회수율을 나타낸 바 있어, 에탄올의 용출 효율이 다양한 식물 종에 걸쳐 재현됨을 시사한다. 종합하면, 센티페드그라스의 항산화 성분 추출에는 80% 에탄올이 가장 적합한 용매라고 판단되며, 해당 용매 조건에서 얻은 추출물이 다른 용매보다 높은 polyphenol 및 flavonoid 함량을 나타내는 만큼 radical 소거 활성 및 세포 기반 항산화 활성에서도 우수한 효과를 나타낼 것으로 기대된다.
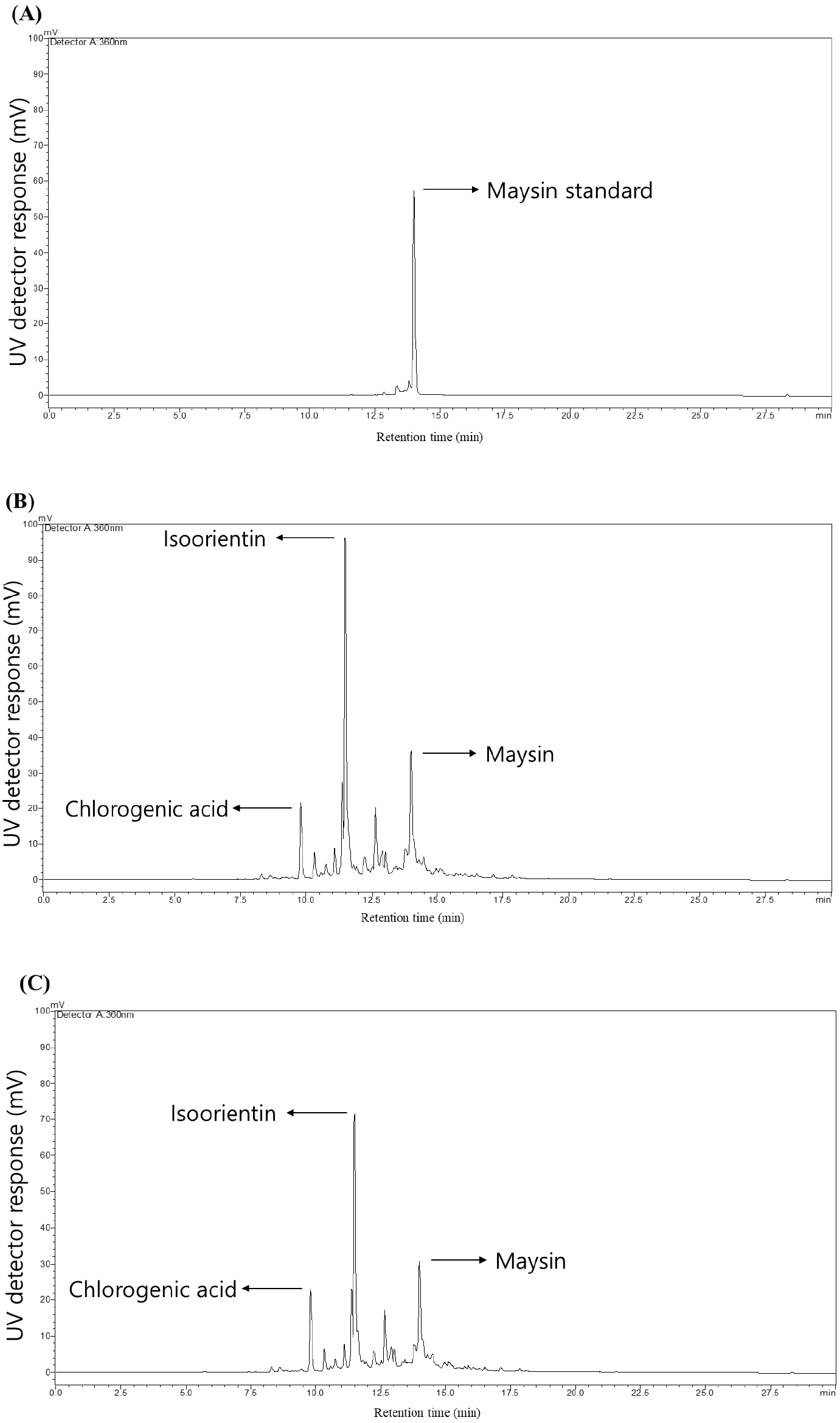
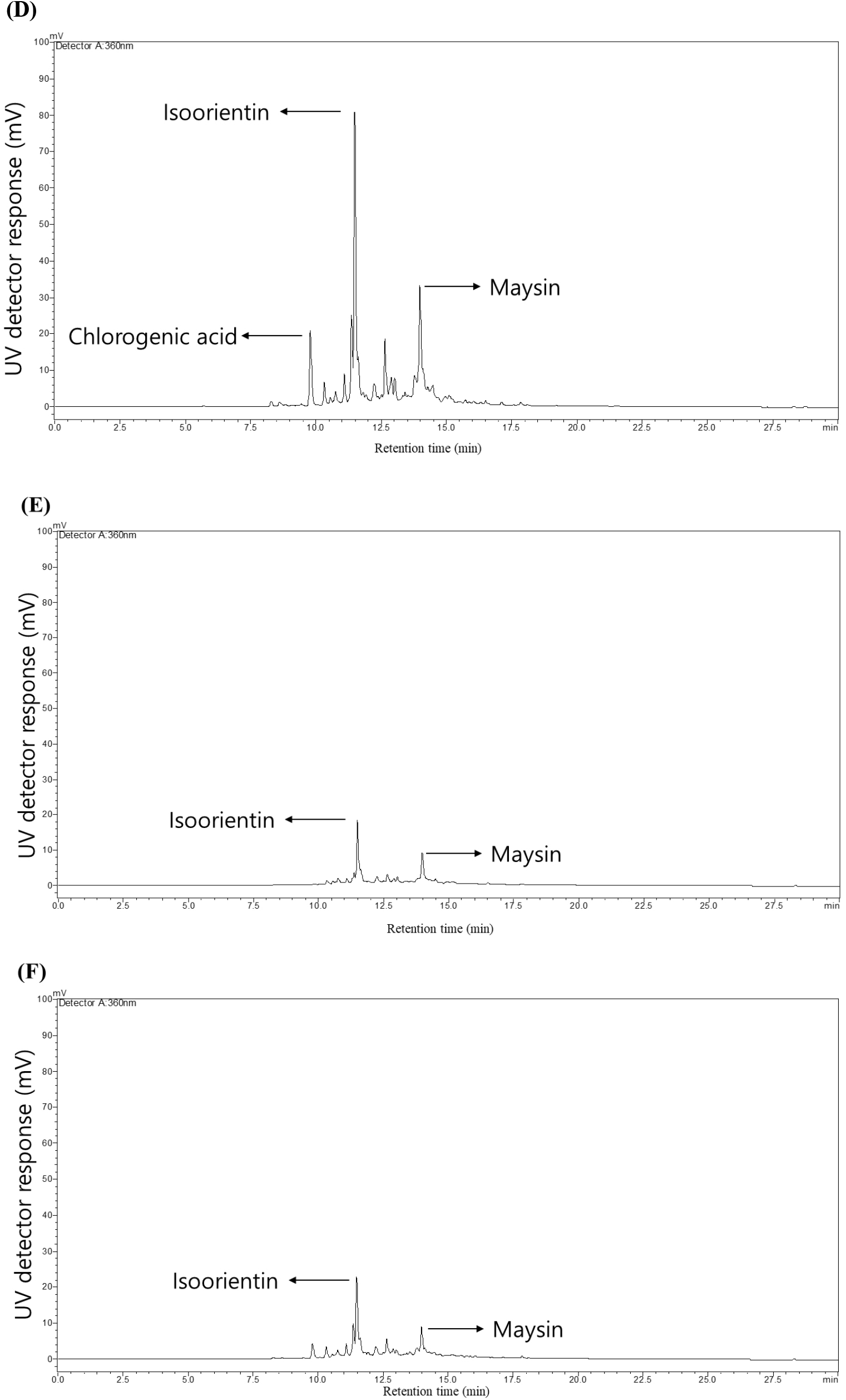
센티페드그라스 추출물의 maysin 함량을 추출 용매별로 비교하기 위해 HPLC 분석을 수행하였으며, 각 추출물의 주요성분에 대한 크로마토그램은 Fig. 1에 제시하였다. 정량 결과, 80% 에탄올 추출물이 21.9±0.2 mg/g으로 가장 높은 maysin 농도를 나타내었고, 80% 아세톤(20.0±0.1 mg/g)과 80% 메탄올(17.8±0.2 mg/g)이 그 뒤를 이었다. 반면, 물 추출물과 열수 추출물은 각각 5.9±0.1 mg/g, 3.45±0.3 mg/g로 유의적으로 낮았다. Chlorogenic acid와 isoorientin 또한 80% 에탄올에서 각각 20.6±0.3 mg/g, 20.6±0.2 mg/g으로 다른 용매 추출물보다 우수한 함량을 나타내었다(p<0.05; Table 3). Maysin은 C-glycosyl flavone 계열로서 친수성(C-glucoside)과 지용성 특성을 갖는 benzopyran 고리 구조를 동시에 지니고 있어, 극성과 비극성 상호작용이 모두 가능한 특성을 나타낸다. Chlorogenic acid와 isoorientin 또한, 극성과 비극성 특성을 동시에 갖는 중간 극성의 화합물로써 중간 극성의 수용성 유기용매인 80% 에탄올에서 용해도가 높아 용출 효능이 극대화되는 경향을 보인다. 페놀계 화합물 및 플라보노이드 배당체는 70-80% 에탄올과 같은 중간 극성의 용매에서 가장 잘 용해되는 특성을 가지며(Sultana 등, 2009), 실제로 Moringa oleifera 잎(Wang 등, 2017), Hylocereus polyrhizus 종자(Zulkifli 등, 2020)에서도 70-80% 에탄올이 flavonoid 회수율을 극대화한 바 있다. Flavonoid는 대표적인 2차 대사산물로 전자 공여 및 금속 이온 킬레이션을 통해 강력한 활성산소종 소거 활성을 나타낸다(Pietta, 2000). 따라서, maysin과 chlorogenic acid, isoorientin이 고농도로 함유된 에탄올 추출물은 다른 용매 추출물보다 우수한 항산화 활성을 나타낼 것으로 기대된다.
DPPH radical과 ABTS radical 소거 활성법은 시료의 항산화능에 의해 radical이 제거 및 탈색되는 원리를 이용한 방법으로 항산화 활성을 평가하는데 널리 이용된다(Moreno 등, 2000). 본 연구에서는 각 추출물의 radical 소거능을 50% 저해농도인 IC50 값으로 비교하였다(Fig. 2, Table 4). 센티페드그라스 추출물의 DPPH radical 소거 활성은 80% 에탄올 추출물 53.8 μg/mL, 80% 메탄올 추출물 53.1 μg/mL, 80% 아세톤 추출물 55.4 μg/mL, 물 추출물 208.9 μg/mL, 열수 추출물 175.7 μg/mL로 측정되었으며, 에탄올과 메탄올 추출물의 IC50 값은 물, 열수 추출물에 비해 약 3-4배 낮아(p<0.05) 우수한 소거 활성을 나타내었다. ABTS radical 소거 활성 역시 80% 에탄올(34.2 μg/mL)과 80% 메탄올(33.5 μg/mL) 추출물이 가장 뛰어난 활성을 나타내었으며, 80% 아세톤(38.4 μg/mL), 열수(62.6 μg/mL), 물(88.0 μg/mL)이 뒤를 이었다. DPPH radical과 ABTS radical 두 모델에서 얻은 IC50 값은 매우 높은 양의 상관계수(r=0.97, p<0.01)를 나타내어 두 라디칼 시스템이 동일한 항산화 성분군에 의해 일관되게 영향을 받음을 시사하였다. 개별 성분과의 상관 분석 결과, maysin 함량은 평균 IC50 값과 강한 음의 상관을 보였다(r=−0.93), 반면 총 flavonoid 함량은 중등도 수준의 음의 상관(r=−0.39)을 나타내었다. 이는 maysin이 센티페드그라스 추출물의 라디칼 소거 활성에 핵심 기여 인자임을 뒷받침한다. 80% 에탄올 계열 용매가 flavonoid를 가장 효율적으로 회수한다는 점은 화살나무 잎(Min 등, 2023)과 님나무 잎(Anokwuru 등, 2011) 등 선행 연구와 일치한다. 또한 옥수수 수염 유래 순수 maysin은 DPPH radical 소거능이 양성 대조인 rutin을 능가하였으며(Kim 등, 2003), 본 실험에서 에탄올 추출물의 maysin 함량이 최고치(21.9 mg/g)였다는 점을 고려하면 maysin이 추출물의 항산화력 향상에 크게 기여한 것으로 판단된다. 자료 전반은 80% 에탄올 · 메탄올 추출 조건이 센티페드그라스의 항산화 유효 성분을 최적으로 농축함을 시사하며, 해당 추출물이 천연 항산화제 후보로서의 가치를 뒷받침한다.
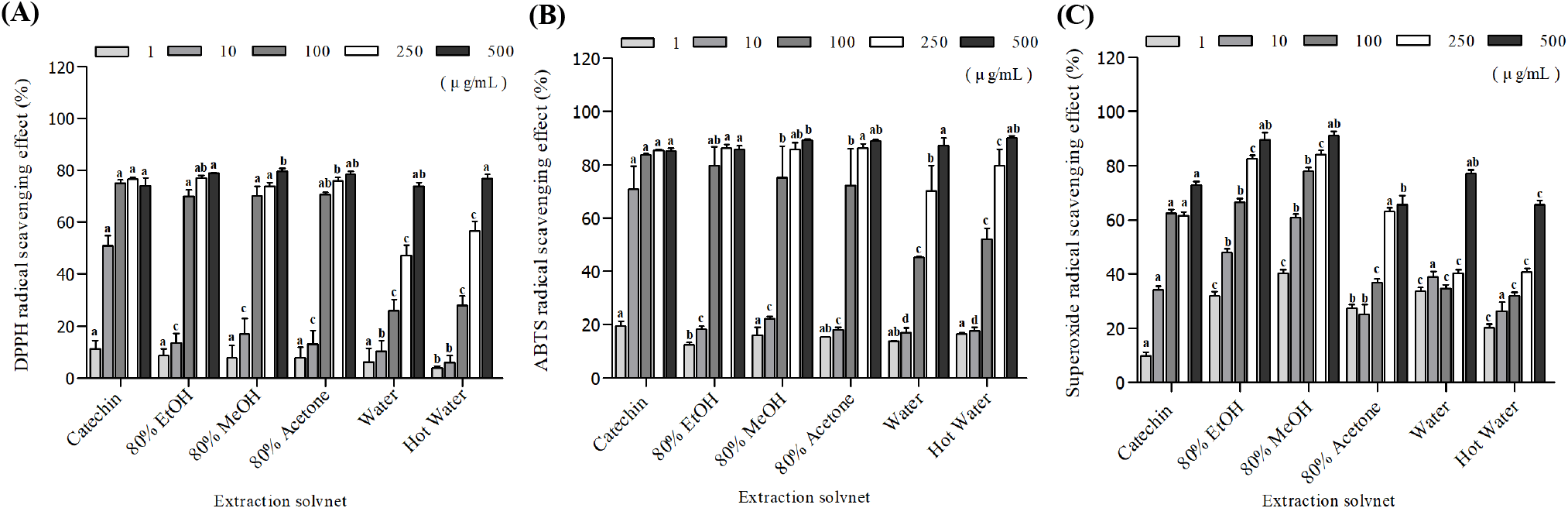
Xanthine oxidase (XO)는 xanthine을 기질로 하여 uric acid를 생성하는 과정에서 superoxide radical을 생성하고 hydrogen peroxide 등의 산화제로 작용하여 통풍을 유발하게 된다(Hatano 등, 1989; Ziegler 등, 1971). Superoxide radical은 NBT와 반응하면 blue formazan을 생성하게 되는데 이때 시료의 항산화 활성과 반응하게 되면 청색의 blue formazan이 superoxide anion radical-NBT-complex 작용으로 인해 탈색되고, 페놀성 화합물에 의해 radical이 소거된다고 보고되어 있다(Gülçin, 2006). 본 연구에서는 센티페드그라스를 용매별로 추출하였을 때 xanthine oxidase와 xanthine으로 인해 생성된 superoxide radical 소거 활성에 미치는 영향을 확인하였으며, 80% 메탄올 추출물이 가장 뛰어난 소거 활성을 나타내었고 그 뒤로 80% 에탄올 추출물이 우수한 소거 활성을 나타내었다(p<0.01; Fig. 2, Table 4). 비극성 비율이 높은 아세톤과 물, 열수 추출물은 IC50 값이 120-335 μg/mL로 현저히 높게 분석되었으며, 메탄올은 제조, 식품의 적용에 독성을 나타내어 대체 용매로 부적합하기 때문에(Roopashree과 Naik, 2019), 80% 에탄올이 산업적 측면에서 항산화 소재를 개발하는 최적의 용매라고 판단된다. 본 연구 결과는 앞서 도출된 polyphenol, flavonoid 및 maysin 함량의 분포와 매우 일관되는 경향을 나타내는데 특히, 에탄올과 메탄올 추출물의 maysin (21.9 mg/g, 17.8 mg/g)은 페놀성 전자공여체로 superoxide radical을 소거하여 formazan의 형성을 억제한 것으로 사료된다.
센티페드그라스 80% 에탄올 추출물의 영양성분 분석 결과, 비타민 C는 883.3 mg/100 g, 칼륨은 6,608.5 mg/100 g로 매우 높은 함량을 나타내었다(Table 5). 비타민 C는 수용성 항산화제로서 활성산소종을 제거하고 산화된 tocopherol을 재생하는 역할을 하며(Davey 등, 2007), 칼륨은 신경과 근육의 정상적인 기능을 돕는 필수적인 전해질이다(Youn과 McDonough, 2009). 본 추출물에는 이들 미량 영양소 외에도 maysin (21.9 mg/g)을 포함한 C-glycosyl flavone이 고농도로 존재하여, 이전의 연구에서 보고된 항산화, 항염 효과(Lee 등, 2011)를 상호보완적으로 증진시킬 수 있을 것으로 판단된다. 센티페드그라스 추출물은 우수한 항산화 활성뿐만 아니라, 영양학적 가치 또한 뛰어나 기능성 및 식품 원료로서 우수한 잠재력이 있음이 확인되었다. 즉, 비타민과 미네랄, polyphenol 복합 성분을 포함하는 센티페드그라스 에탄올 추출물은 식의약 및 화장품 분야에서 다양한 항산화 소재로서의 활용 가치가 높음을 시사한다.
4. 요약
본 연구에서는 서로 다른 극성을 지닌 용매를 이용하여 센티페드그라스를 추출한 후 각 추출물의 화학 조성과 항산화 활성을 체계적으로 비교 분석하였다. 추출 용매와 추출 시간은 자사에서 반복적인 추출 과정을 통해 확립된 결과를 토대로 진행하였으며, 그 결과 80% 에탄올 추출물에서 maysin과 polyphenol, flavonoid 함량이 가장 높게 검출되었다. 또한, DPPH radical 및 ABTS radical 소거 활성과 xanthine 유래 superoxide radical 소거 활성에서 모두 높은 항산화 활성을 나타내었다. 두 라디칼 모델에서 얻은 IC50 값은 강한 양의 상관을 보여 동일한 항산화 인자가 작용함을 시사했고, 특히 maysin의 농도와 IC50 값 간의 뚜렷한 음의 상관을 나타내어 maysin이 항산화 활성에 핵심 성분임을 확인하였다. 또한, 80% 에탄올 추출물은 비타민 C와 칼륨을 포함한 필수 영양소를 풍부하게 함유하고 있어, 항산화 활성을 나타내는 물질과 상호 보완적으로 작용할 가능성을 제시하였다. 이러한 결과는 센티페드그라스 80% 에탄올 추출물이 강력한 항산화 효능과 뛰어난 영양학적 가치를 지닌 천연 소재임을 입증하며, 향후 기능성 식품, 건강 보조제 등 다양한 분야에서 활용될 수 있는 과학적인 근거를 제공한다.










