1. 서론
현대 사회에서 피부는 자외선, 미세먼지, 정신적 스트레스 등 다양한 환경적 요인에 지속적으로 노출되어 피부 항상성 유지에 어려움을 겪고 있다(Krutmann 등, 2017). 이러한 외부 자극은 피부 내 활성산소종(reactive oxygen species, ROS)의 생성을 유도하여 세포 손상을 일으키며 지질과 단백질 등 주요 생체 분자의 산화를 초래한다(Gonzaga, 2009; Rawlings와 Harding, 2004). 그 결과 피부는 민감하게 반응하거나 가려움, 홍반 등의 피부염 노출이 증가하고, 장기적으로는 피부 노화 및 염증성 피부질환의 위험이 높아진다(Sandilands 등, 2009). 활성산소 및 자유 라디칼의 과도한 생성은 체내 항산화 방어체계를 약화시켜 염증 매개체의 과도한 분비를 촉진한다(Pillai 등, 2005). 이로 인해 염증 방어를 담당하는 대식세포가 손상 및 괴사에 이르게 되며, 이는 선천 면역 조절의 기능 저하로 나타난다(Ghasemian 등, 2016). 대식세포는 항원을 제거하고 염증성 사이토카인을 분비하여 면역 반응을 조절하는 데 핵심적인 역할을 한다(Park 등, 2023). 특히 lipopolysaccharide (LPS) 자극에 의해 유도된 대식세포는 산화질소(nitric oxide, NO)와 프로스타글라딘 E2 (PGE2)를 생성하여 염증 반응을 유도한다(Huang 등, 2024; Kim 등, 2007). 이러한 염증 반응은 피부 장벽 손상에도 관여한다. 천연보습인자(natural moisturizing factors, NMF)의 감소는 각질세포 간 응집력을 저하시켜 피부의 수분 유지 능력을 약화시키고, 결과적으로 장벽 기능 저하로 이어진다(Liang 등, 2016). 특히 피부 보습 인자인 히알루론산(hyaluronic acid, HA)은 세포외기질(extracellular matrix, ECM)의 주요 구성 성분으로 세포막 주변에 분포하여 수분을 저장하고 피부 구조를 안정화하는 역할을 수행한다(Kang 등, 2024). 따라서 피부 장벽 유지와 염증 조절은 피부 항상성 유지의 핵심 요소로 작용하며, 피부 보습력과 면역 조절 능력은 건강한 피부의 지표가 된다.
제주 용암해수는 현무암질 화산암층을 통과한 후 자연적으로 여과된 지하 해수로, 유기물과 병원균이 대부분 제거된 순도 높은 해수로 알려져 있다(Miyamura 등, 2004). 칼슘, 마그네슘, 셀레늄, 아연 등 풍부한 미네랄과 영양염류를 포함하고 있으며, 식품 및 화장품 산업에서 기능성 원료로 주목받고 있다(Ding 등, 2019; Kang 등, 2023). 용암해수의 미네랄 성분은 피부 보습에 관여하는 유전자 발현을 증가시켜 보습 기능을 강화하고(Lee 등, 2016), 특히 염화칼슘과 염화마그네슘과 같은 무기염은 피부 장벽 회복에 기여하는 것으로 보고되었다(Denda 등, 1999).
오미자과(Schisandraceae)에 속하는 오미자(Schisandra chinensis Baillon)는 낙엽성 덩굴식물로 붉은 열매는 다섯 가지 맛이 난다고 알려져 있다(Kopustinskiene과 Bernatoniene, 2021). 오미자는 아시아에서 다양한 연구가 진행되는 약초 중 하나로 간 보호(Wang 등, 2014), 진정(Hu 등, 2014), 항산화(Lee 등, 2014), 항암(Zhou 등, 2016) 등의 약리 효과로 잘 알려져 있다. 오미자의 약리효능은 주로 dibenzocyclooctadiene 골격을 가진 다수의 리그난 성분들에 기인하며, schizandrin (schizndrol A), schizandrol B (gomisin A) 등이 다수 함유되어 있고, 이외에 flavonoids의 quercetin, rutin과 triterpenoid 화합물의 lactone등이 확인되었다(Kim 등, 2024). 이러한 성분들의 함량 증진을 위한 발효 등 다양한 추출 기술 연구도 진행 중이다(Park 등, 2021).
따라서 본 연구는 제주 용암해수를 이용하여 오미자 열매 추출물을 제조한 후, 리그난 성분들 중 schisandrol A와 schisandrol B의 성분 변화를 확인 후 피부세포의 생리활성 변화를 관찰하고자 하였다.
2. 재료 및 방법
오미자 에탄올 추출물 및 오미자 용암해수 추출물 제조에 사용된 오미자 열매는 충북 제천에서 구입(Tojongherb, Jecheon, Korea)하여 사용하였다. 건조된 오미자 열매를 분쇄 후 시료에 70% 에탄올을 넣고 60°C에서 20시간 동안 가온 추출 후, 감압 농축(EYELA, Tokyo, Japan)하여 얻어진 수득물을 오미자 추출물로 사용하였다. 오미자 용암해수 추출물에 사용된 용암해수는 ㈜두래 제주바이오센터에서 구입하였으며 최적의 배양을 위해 경도를 500으로 맞추어 사용하였다. 분쇄된 오미자 열매를 원물 대비 20배의 경도를 500으로 맞춘 제주용암해수를 넣고 밀봉한 다음 4°C에서 7일간 정치 배양을 통해 숙성을 진행하였다. 물을 제거한 후 60°C에서 5시간 동안 가온 추출 후 10% NaHCO3 용액을 같은 비율로 첨가한 후 감압 농축 후 고온에서 교반하여 수득하였다. 이후 추출물들은 여과지(Whatman No. 2; Cytiva, Marlborough, MA, USA)를 이용하여 여과한 후 동결 건조하여 -20°C에 보관하여 본 실험의 시료로 사용하였다.
오미자 에탄올 추출물과 용암해수를 이용한 오미자 추출물의 성분 변화를 확인하기 위해 고성능 액체 크로마토그래피 분석방법을 사용하였다. 표준 용액은 schisandrol A와 schisandrol B 표준물질(Sigma-Aldrich, St. Louis, MO, USA) 0.1 g을 정밀 측정하여 메탄올 1 mL를 이용하여 녹인 후, PTFE syringe filter (0.45 μm; Merck Millipore, Burlington, MA, USA)로 여과한 후 표준용액으로 하였다. 시험 용액의 경우, 오미자 에탄올 추출물과 오미자 용암해수 추출물을 각각 0.1 g을 정밀하게 측정해 이를 메탄올 10 mL를 이용하여 녹인 후 PTFE syringe 0.45 μm 필터로 여과하여 제조하였다. 지표성분을 분석하기 위해 Photodiode array (PDA)가 달린 HPLC system (Shimadzu, Kyoto, Japan)을 이용하였으며, 컬럼은 shim-pack GIS C18 (4.6 mm×250 mm, 5 μm; Shimadzu, Kyoto, Japan)을 사용하였다. 이동상 용매는 아세토니트릴(Acetonitrile, ThermoFisher, Waltham, MA, USA)과 0.1% 트리플루오로아세트산(trifluoroacetic acid, ThermoFisher, Waltham, MA, USA)이 함유된 초순수(water)를 사용하였으며 모든 용매는 사용 전 탈기 및 필터 여과 후 사용하였다. 분석 시간은 0에서 40분까지 이동상을 조절하였으며 분석 시료는 10 μL를 주입하였다. 컬럼의 유속은 1.0 mL/min, 온도는 40°C였으며 UV는 251 nm에서 측정하였다.
1,1-Diphenyl-2-picrylhydrazyl (DPPH, Thermo Scientific, Waltham, MA, USA)은 Blois의 방법을 변형하여 측정하였다. 180 μM DPPH를 희석하여 조제한 시약과 시료를 농도별로 희석하여 각각의 well에 넣고 혼합한 후 15분간 배양한다. 반응 후 517 nm에서 microplate reader (BMG LABTECH, Allmendgrun, Ortenberg, Germany)를 이용하여 흡광도를 측정하였다. 소거능 측정은 시료 용액의 첨가군과 무첨가군의 흡광도 감소율로 표현하였다.
인체각질형성세포(human keratinocyte)인 HaCaT 세포와 대식세포인 RAW 264.7 세포는 ATCC (Manassas, VA, USA)에서 분양받아 실험에 사용하였으며 100 U/mL penicillin/streptomycin (Thermo Scientific, Waltham, MA, USA)과 10% fetal bovine serum (Thermo Scientific, Waltham, MA, USA)를 함유하는 Dulbecco’s Modified Eagle’s Medium (DMEM) (Thermo Scientific, Waltham, MA, USA)배지에 넣고 37°C, 5% 이산화탄소를 포함하는 배양기 내에서 배양하였다.
각질형성세포와 대식세포에 대한 세포 생존율은 3-[4,5-dimethylthiazol-2-yl]-2,5-diphenyltetrazolium bromide (MTT, Sigma Chemical Co., St. Louis, MO, USA) 측정을 통한 세포독성을 확인하였다. 각각의 세포를 96 well plate에 1×104 cells/well을 분주하여 24시간 동안 배양 후 오미자 추출물 및 오미자 용암해수 추출물을 각각 첨가 후 배양액과 함께 배양 후 2.5 mg/mL MTT 시약을 각각의 well에 첨가한 후 3시간 동안 반응시켰다. 이후 MTT 시약을 제거하고 DMSO 용매를 첨가하여 10분간 반응시킨 후 540 nm에서 microplate reader를 사용하여 흡광도를 측정하여 세포생존율을 측정하였다.
각질형성세포 1×105 cells/mL의 농도로 96-well plate에 seeding 후 각 well에 배양배지를 제거하고 PBS로 세척한 다음 FBS를 함유하지 않은 DMEM 배지를 사용하여 세포를 기아상태로 만들어주었다. SLS 30 μg/mL와 함께 일정 농도의 오미자 에탄올 추출물과 오미자 용암해수 추출물을 처리하여 24시간 배양하였다. 이후 MTT 시약을 이용하여 자극에 의해 반응한 세포들을 540 nm에서 microplate reader를 사용하여 흡광도를 측정하여 확인하였다.
NO 생성 저해 활성은 대식세포를 이용하여 Green 등(1982)의 방법을 변형하여 수행하였다. 6-well plate에 세포를 3×105 cells/well씩 분주한 후, 18시간 37°C, 5% CO2 배양기에서 배양한 후, 자극제인 10 μg/mL의 LPS 농도로 처리 후 2시간 뒤 시료를 농도별로 추가한다. 다음날 세포 배양액과 Griess reagent (Sigma Chemical Co., St. Louis, MO, USA)를 1:1로 반응시켜 540nm에서 흡광도를 측정을 통해 NO 생성능을 관찰하였다. NO 측정은 무첨가군과 첨가군을 비교하여 백분율로 계산 하였다.
HaCaT 세포를 1.5×104 cells/well씩 96-well plate에 seeding 후 24시간 동안 배양하였다. 배양액을 버리고 PBS로 세척한 다음 FBS를 함유하지 않은 DMEM 배지를 사용하여 세포를 기아 상태로 만들어주었다. 24시간 배양 후 샘플을 다양한 농도로 처리하여 배양 후 HA Elisa kit (R&D system, Minneapolis, MN, USA)를 이용하여 제조사에서 제공한 방법으로 실험을 수행하였다. 이후, HA양을 측정하기 위해 microplate reader로 흡광도 450 nm에서 측정하여 나타내었다. 최종 HA의 양은 단백질 당 HA의 양으로 변환하여 음성대조군과 확인하였다.
3. 결과 및 고찰
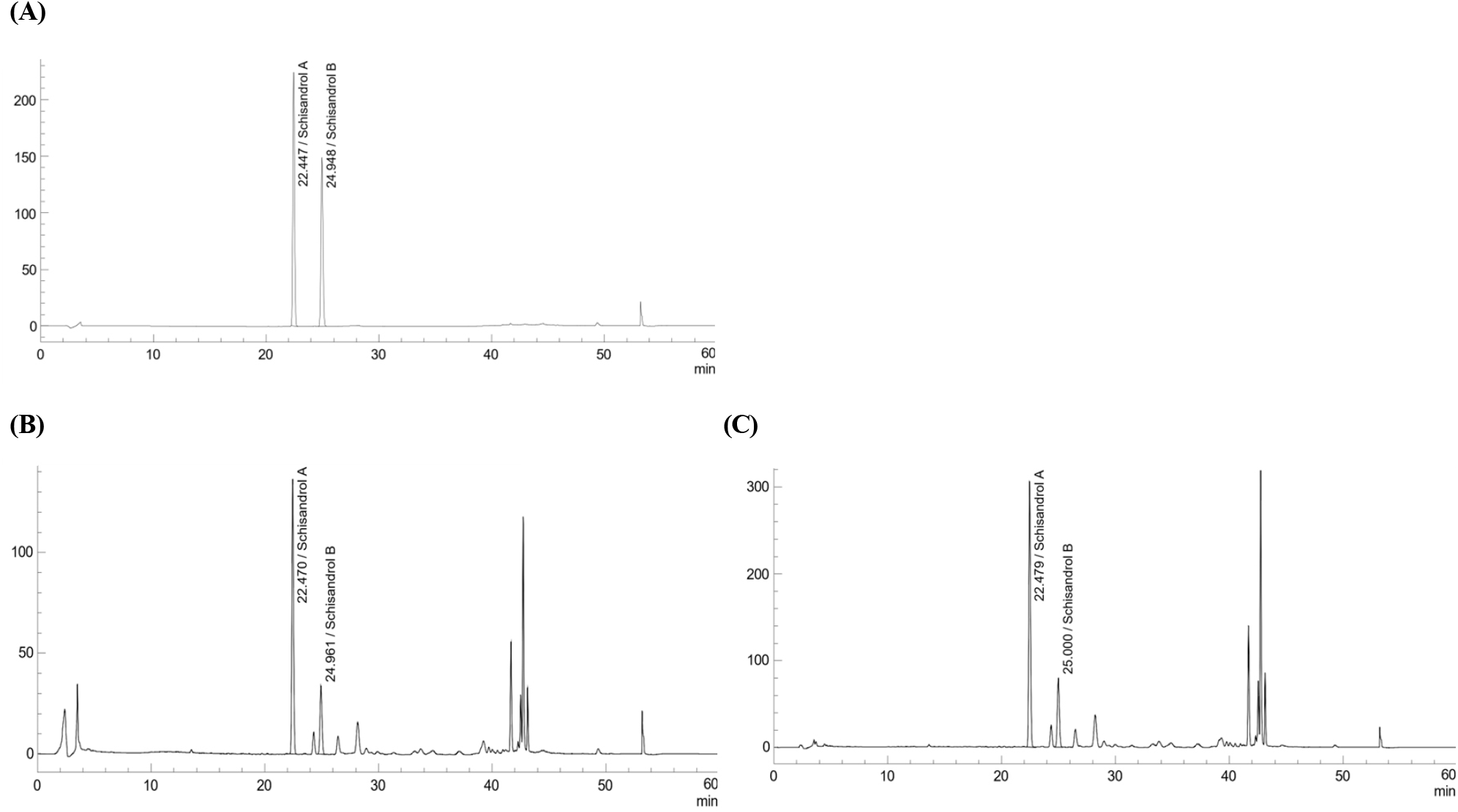
용암해수 처리에 따른 오미자 에탄올 추출물의 주요 지표성분인 schisandrol A, schisandrol B의 함량 변화를 분석하였다. 오미자 추출물은 대표적인 생리활성 물질인 리그난 화합물을 포함하며, 트리테르페노이드 성분도 보고된 바 있다(Kim 등, 2019). 특히 오미자에 함유된 주요 성분 중 schisandrol A과 schisandrol B의 성분이 가장 많이 함유되어 있다고 알려져 있어 본 연구에서도 이들의 함량 변화를 관찰하였다. 오미자 에탄올 추출물의 schisandrol A와 schisandrol B의 함량을 확인한 결과, 약 44,721.67±413.69 ppm과 19,485.33±222.87 ppm 함량이었으나 용암해수 전처리를 통해 수득한 오미자 용암해수 추출물의 함량은 약 137,776.00±54.51 ppm과 53,450.33±43.50 ppm으로 약 3배 이상 증가하였다(Fig. 1, Table 1). 선행연구에 따르면, 이러한 리그난 성분인 schisandrol A와 schisandrol B 함량 증가는 항산화 활성의 증가와 연관되며, 염증매개인자 발현 억제를 통해 항염 효과도 유도하는 것으로 보고되었다(Jeong 등, 2024; Szopa 등, 2017; Kopustinskiene과 Bernatoniene, 2021). 용암해수는 현무암층을 통과하면서 여과되어 칼슘, 마그네슘, 셀레늄, 아연 등 다양한 미네랄을 풍부하게 함유하고 있으며, 일반 해수나 해양심층수보다 나트륨, 철, 망간 등의 함량이 높다고 알려져 있다(Lee 등, 2016). 특히 철 성분은 산화전이의 촉매역할을 통하여 유기물의 대사물질 성분 변화에 관여할 수 있다(Prousek 등, 2007). 미네랄은 피부 장벽에 활성에 도움을 주며 염화칼슘 및 마그네슘 성분이 장벽 회복 가속화를 통해 피부수분 함량을 증가시킨다고 보고되었다(Denda 등, 1999). 또한 미네랄이 풍부한 해양심층수를 활용하여 토마토의 lycopene 함량 및 가용성 고형물 함량을 증가시킨 연구와 보리 발아 과정에 용암해수를 사용하여 procyanidin과 prodelphinidin 대사산물의 함량을 증대시켜 주름 개선 소재로서의 가능성을 제시한 연구 등, 미네랄 성분에 의한 숙성과 이에 따른 성분 변화에 관한 연구들이 지속적으로 보고되고 있다(Park 등, 2021; Woo 등, 2006). 결과적으로, 용암해수 전처리는 schisandrol A와 B의 생합성 또는 추출 효율에 긍정적인 영향을 미쳤으며, 이러한 작용은 미네랄 조성과 산화환원 환경의 복합 효과로 해석된다.
| Compounds | Contents | |
|---|---|---|
| SE | SLE | |
| Schisandrol A (ppm) | 44,721.67±413.691) | 137,776.00±54.5*2) |
| Schisandrol B (ppm) | 19,485.33±222.87 | 53,450.33±43.50* |
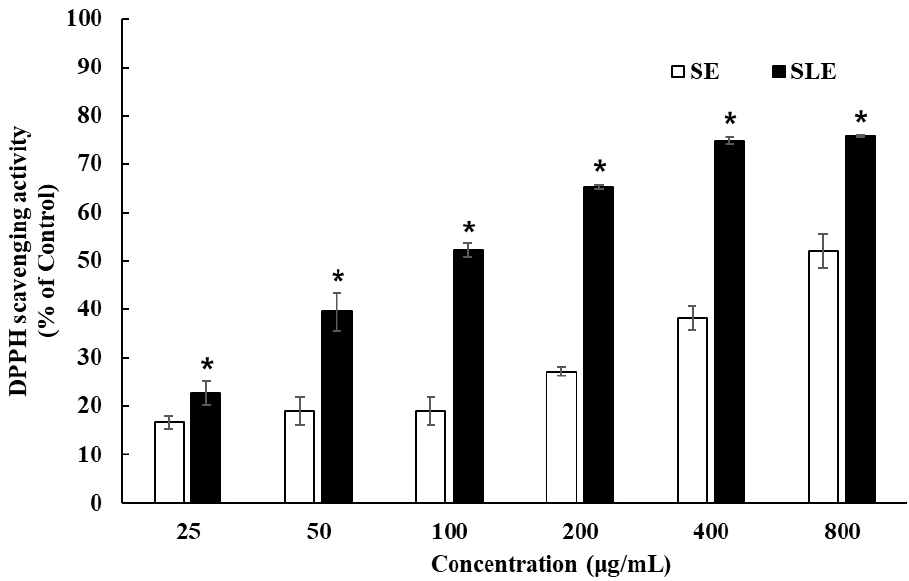
오미자 에탄올 추출물과 오미자 용암해수 추출물의 항산화 활성의 변화를 확인하고자 DPPH 라디칼 소거 활성능을 측정하였다. 오미자 에탄올 추출물과 오미자 용암해수 추출물 모두 농도 의존적으로 라디칼 소거활성이 증가하였으며(Fig. 2), 특히 용암해수를 이용한 추출물에서 더 높은 소거 활성이 나타났다. 200 μg/mL 농도에서 오미자 용암해수 추출물은 에탄올 추출물에 비해 약 38.1% 높은 소거 활성을 보였다. 선행연구에 따르면 용매별 오미자 추출물의 과산화물가 분석을 통해 천연 항산화제로서의 활용 가능성이 제시되었으며, 특히 항온저장 조건에서 에탄올 추출물이 가장 높은 항산화 활성을 나타내는 것으로 보고되었다(Jang 등, 1996). 또한, 전처리 조건을 건조방법, 분쇄 방법 및 용매 조성에 따라 달리한 오미자 추출물 분석 결과, 에탄올 추출물에서 리그난 화합물(schisandrol A, gomisin A, gomisin N)의 함량과 DPPH 라디칼 소거 활성도 가장 높게 나타났다(Jung 등, 2025). 이는 오미자에 함유된 지용성 성분들의 에탄올에 대한 용해도와 밀접한 연관성을 나타내며 전처리 조건에 따라 항산화 활성 변화에 중요한 역할을 담당하는 것으로 사료된다. 본 연구에서도 용암해수 전처리를 통한 추출 시 지표성분의 증가가 라디칼 소거 활성 증가에 영향을 미친 것으로 판단된다.
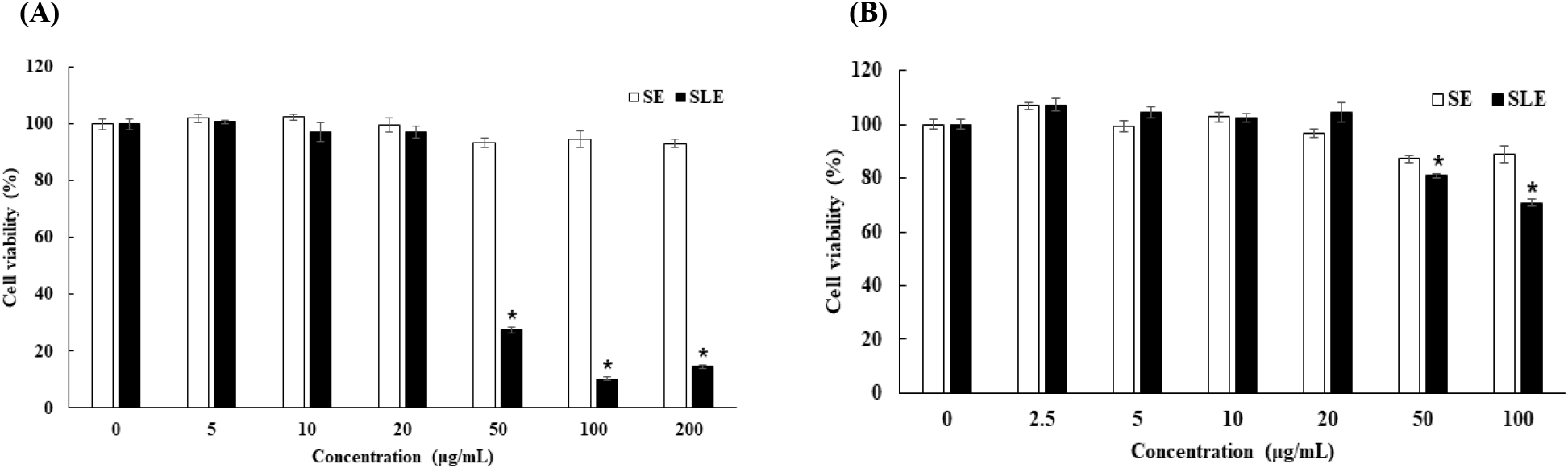
오미자 에탄올 추출물과 오미자 용암해수 추출물의 세포 독성을 알아보기 위해 각질형성세포와 대식세포의 생존에 미치는 영향을 확인하였다. 살아있는 세포 내 미토콘드리아의 탈수소효소에 의해 환원반응의 결과로 formazan 색소로 변환되는 원리를 이용한 실험법으로 오미자 에탄올 추출물과 오미자 용암해수 추출물을 농도별로 처리하여 확인하였다(Madesh과 Balasubramanian, 1998). 각질형성세포에서 오미자 에탄올 추출물과 오미자 용암해수 추출물을 2.5-100 μg/mL의 농도로 처리하여 확인한 결과, 10 μg/mL 이하의 농도에서 각각의 시료가 95% 이상의 세포 생존율을 나타났다. 대식세포에서 샘플을 5-200 μg/mL의 농도로 처리하여 확인한 결과, 20 μg/mL 이하의 농도에서 모든 시료가 95% 이상의 세포 생존율을 확인하였다(Fig. 3). 이후의 생리활성 비교실험은 해당 범위 내에서 수행되었다.
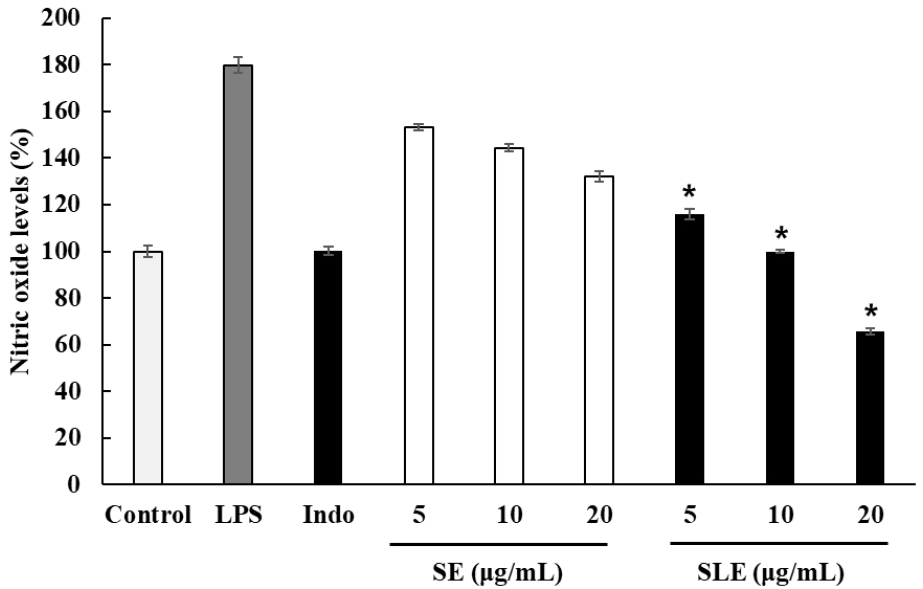
LPS 자극에 의해 활성화된 대식세포에서 생성되는 염증 매개 인자인 nitric oxide (NO)의 변화를 확인하기 위해, 오미자 에탄올 추출물과 오미자 용암해수 추출물을 농도별로 처리 후 NO 생성 억제 효과를 측정하였다. 그 결과 모두 LPS 자극에 의해 유도된 NO 생성을 저해하는 것으로 확인하였다. 특히 오미자 용암해수 추출물은 기존 추출물보다 유의적으로 우수한 활성을 나타내었으며 최대 20 μg/mL 농도에서는 약 66% 정도 저해 효과가 확인되었으며 양성대조군으로 사용한 indomethacin (2.5 μg/mL)은 약 79% 정도 저해능이 관찰되었다(Fig. 4). LPS는 세포질과 조직 내 사이토카인 발현을 유도하여 다량의 NO 생성을 유발하며, 생성된 NO는 대식세포 유래 염증 매개체로 작용하여 염증 반응에 관여한다고 보고되었다(Dilshara 등, 2013). 또한, 오미자 열수 추출물 역시 NO, PGE2와 TNF-α 등의 염증 매개 인자의 발현을 억제함으로써 항염 효과가 나타내는 것으로 알려졌으며 리그난 화합물인 schisandrol A의 함량이 증가할수록 유의한 것으로 보고되었다(Han 등, 2021). 결국, 오미자 용암해수 추출물은 기존 추출물보다 NO 억제 활성이 증가하였으며 이는 리그난 성분 변화에 기인한 것으로 사료된다.
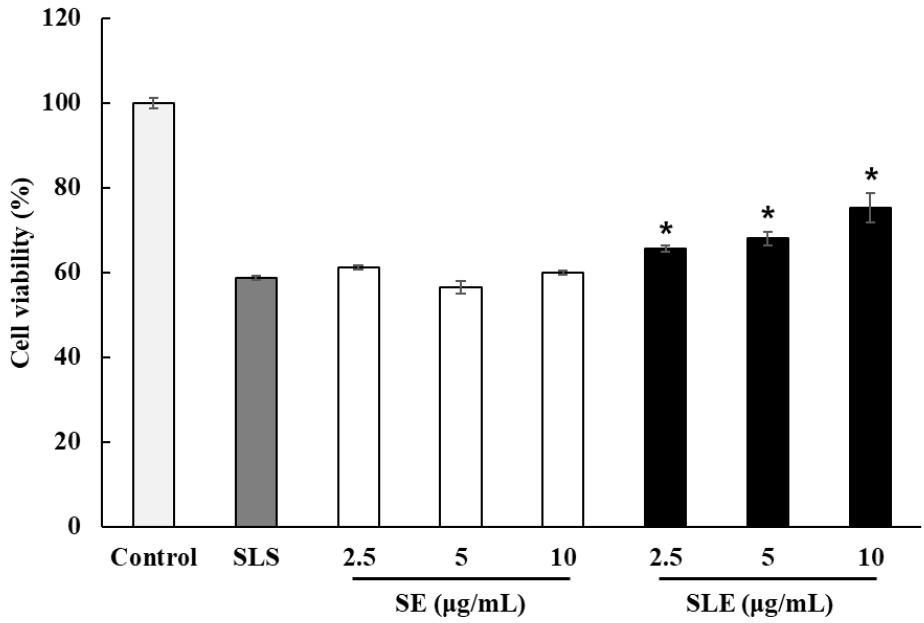
Sodium lauryl sulfate (SLS)는 피부 장벽 기능을 손상시키고 염증을 유발하는 대표적인 자극성 계면활성제이다(Leoty-Okombi 등, 2021). 이러한 자극성 물질로부터 피부를 보호해 주는 자극 완화 천연물들은 안전성을 확인할 수 있는 지표로 활용되고 있다(Kim 등, 2004). 이에 각질형성세포에 SLS 자극을 유도 후 오미자 에탄올 추출물과 오미자 용암해수 추출물의 자극 완화 효과를 확인하였다. 그 결과 SLS 자극에 의해 감소된 세포 생존율이 오미자 추출물은 변화가 나타나지 않았으나, 오미자 용암해수 추출물의 세포 생존율은 최대 10 μg/mL 농도에서 약 16% 증가된 세포 생존율을 확인하였다(Fig. 5). SLS 자극에 의해 유도된 표피 반응은 사이토카인 등의 염증 매개체의 생성을 유발한다(Kobiela 등, 2013). 이로 인한 면역 반응의 교란으로 피부에 항상성 유지가 어려워지고 피부 노화가 촉진된다(Pillai 등, 2005). 이에 따라, 용암해수로 전처리한 오미자 추출물은 기존 에탄올 추출물에 비해 자극 완화 효능이 향상되었으며 미네랄 성분 및 NO 억제 효과에 기인한 것으로 판단된다.
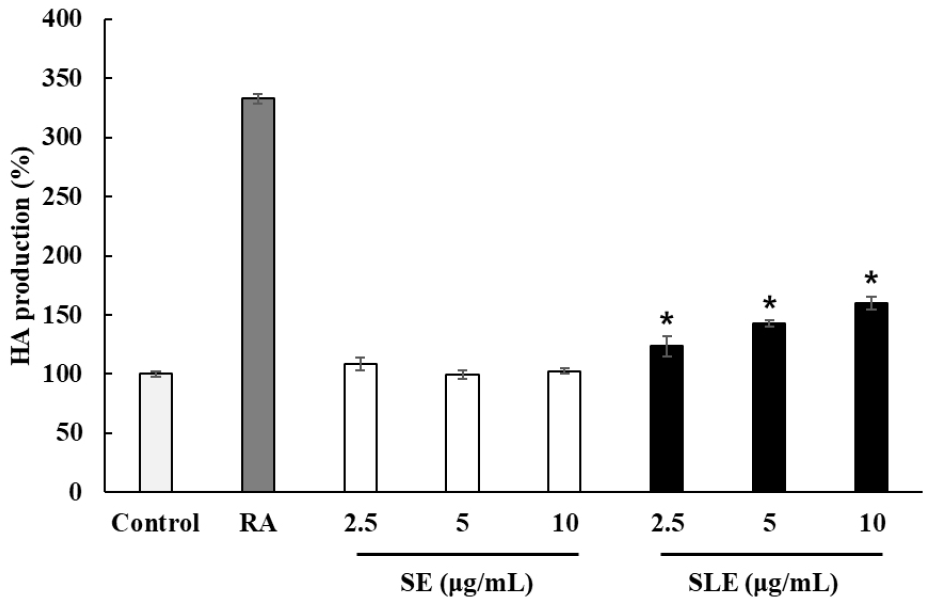
오미자 에탄올 추출물과 오미자 용암해수 추출물의 보습장벽 인자인 HA 생성에 미치는 변화를 평가하였다. 그 결과 오미자 에탄올 추출물에서는 HA 생성 효과가 관찰되지 않았으나 용암해수를 이용한 추출물에서는 농도가 증가할수록 HA 생성량이 증가한 것을 확인하였다(Fig. 6). 특히 최대 10 μg/mL 농도에서 약 60% HA 생성 증가를 확인하였다. Retinoic acid는 비타민 A의 활성물질로 각질층의 HA 합성 효소의 발현 증가를 통한 HA 합성에 관여하는 것으로 보고되어 양성대조군으로 확인하였다(Han과 Ha, 2019; Szymanski 등, 2020). 선행연구에서 용암해수에 풍부하게 함유된 영양염류와 미네랄이 수분 함유량을 증가시키는 특성을 통해 용암해수와 홍삼을 혼합하여 추출한 경우 피부 장벽 보호 효과가 보고되었다(Jo 등, 2021). 따라서 기존 오미자 추출물에서 활성이 나타나지 않았던 HA 생성 효과가 용암해수 전처리에 의해 유의하게 증가하였으며 이는 용암해수에 포함된 성분들이 활성이 기여했을 것으로 사료된다. 향후 추가 분석을 통해 지표성분 활성에 관여하는 미네랄 성분의 규명이 필요하다.
4. 요약
본 연구는 제주 용암해수를 활용하여 오미자 에탄올 추출물의 기능성 성분 오미자 에탄올 추출물의 지표성분 및 생리활성에 미치는 영향을 조사하였다. 오미자에 함유된 지표성분인 schisandrol A와 schisandrol B의 함량 변화를 확인한 결과 오미자 용암해수 추출물에서 약 3배 정도 함량이 증가한 것을 확인하였다. 생리활성 변화를 확인하고자 라디칼 소거 활성을 비교한 결과 오미자 용암해수 추출물이 기존 에탄올 추출물 대비 우수한 활성을 나타내었다. 대식 세포와 각질형성세포를 이용하여 NO 생성 억제 및 SLS 자극 완화 효과 시험을 진행하였을 때 용암해수를 이용한 오미자 추출물에서 향상된 억제 활성을 나타냈다. 또한, 오미자 용암해수 추출물에서 HA 생성능 증가 효능을 확인을 통해 피부 보습 효능에도 유의미한 결과를 확인하였다. 이러한 결과는 용암해수의 미네랄 조성이 기능성 성분의 함량 및 효능 증진에 기여한 것으로 판단된다. 본 연구 결과는 오미자 용암해수 추출물은 화장품 및 기능성 소재로서의 활용 가능성을 제시하는 것으로 사료된다.










