1. 서론
일반적으로 수심 200 m 이상의 해수를 해양심층수(deep sea water, DSW)라 하며, 표층수와 달리 햇빛이 도달하지 않아 광합성이 이루어지지 않는다. 이로 인해 영양염류는 풍부하지만 유기물 함량이 낮아, 미생물의 밀도는 표층수에 비해 상대적으로 낮은 수준을 보인다. 이러한 극한 환경에 적응한 미생물들은 독특한 대사 능력과 생리적 특성을 지니며, 산업적 활용 가능성이 높아 높은 부가가치를 가진다(Moon 등, 2004). 해양심층수는 특히 풍부한 미네랄 함량과 높은 청정성이 특징으로, 자원으로 개발할 경우 환경에 미치는 영향이 적은 거의 무한한 자원으로 평가된다. 국내 연안에서 산업적 ․ 학술적으로 활용 가치가 높은 해양심층수는 지형과 수심 특성상 동해에만 존재한다(Choi 등, 2015). 동해는 수천 미터에 달하는 심해 분지와 겨울철 표층 냉각으로 형성되는 고밀도수 덕분에 안정적인 심층수가 발달하며, 연안에서도 취수가 가능하다. 이러한 특성으로 인해 강원특별자치도 고성군을 중심으로 해양심층수 개발이 활발히 이루어지고 있다. 이에 따라 설립된 해양심층수산업 고성진흥원은 지역 기업들과 협력하여 해양심층수의 산업적 활용 방안을 모색하고 있으며, 특히 미생물 유래 물질을 이용한 기능성 식품 분야에서의 응용 가능성이 주목받고 있다. 해양심층수는 낮은 온도, 높은 수압, 낮은 광도 등 극한 조건에서 형성되기 때문에, 이로부터 유래한 미생물은 극한 환경에 대한 적응력이 우수하고 안정적인 생육 특성을 보인다(Horikoshi, 1998). 이러한 특성은 발효 공정의 안정성을 높이고 품질의 일관성을 유지하는 데 기여할 수 있다.
김치는 우리나라를 대표하는 발효식품으로, 숙성 과정에서 다양한 유산균이 증식하며 특유의 풍미와 향미를 형성한다(Park 등, 2014). 그러나 자연 발효 김치의 경우 원료에 존재하는 미생물 조성이 일정하지 않아, 발효 속도나 맛, 품질의 일관성을 유지하기 어렵다는 한계가 있다(Gautam 등, 2025). 이러한 문제는 발효 초기 특정 유산균의 우점을 유도할 수 있는 스타터 배양균(starter culture)을 활용함으로써 개선할 수 있으며, 이를 통해 일정한 품질의 김치 생산이 가능하다(Choi 등, 2020; Lee 등, 2024).
Leuconostoc mesenteroides는 김치 발효 초 · 중기에 우세하게 존재하는 대표적인 이형발효형 유산균으로, 젖산, 이산화탄소, 에탄올, 아세트산 등 다양한 대사산물을 생성한다(Jung 등, 2012). 특히 만니톨 생성능이 우수하여 김치의 풍미 향상과 기호도에 긍정적인 영향을 미치는 것으로 알려져 있다(Behare 등, 2020; von Weymarn 등, 2002). 김치의 발효에는 Lactobacillus, Leuconostoc, Lactococcus, Enterococcus, Streptococcus, Pediococcus 등 다양한 유산균이 관여한다(Kim 등, 2012). 이 중 L. mesenteroides는 발효 초기 우점균으로 작용하지만, 숙성이 진행됨에 따라 Lactobacillus plantarum 또는 Saccharomyces cerevisiae 등과 같은 미생물로 점차 대체되는 경향을 보인다. 이러한 미생물들은 높은 젖산을 생산하여 김치를 빠르게 산성화시키고 시어지게 만들기 때문에, L. mesenteroides의 우점 상태를 유지하는 것이 김치의 풍미와 저장성 유지에 중요하다(Sa 등, 2002). Leuconostoc 속 미생물을 김치 제조를 위한 스타터로 사용하여 품질 특성에 대해 연구한 결과 빠르게 젖산의 농도가 빠르게 상승하여 저장 수명을 연장하고 감각적 품질이 개선되었으며(Li 등, 2020), 박테리오신을 생산하는 L. citreum을 김치 제조시 스타터로 사용한 결과 자연 발효조건에서 다른 미생물의 성장을 제어하기 위해 유용하게 적용될 수 있다 보고한 바 있어(Chang과 Chang, 2010) Leuconostoc 속 미생물은 김치 제조를 위한 스타터로서 높은 활용 가치를 가질 것으로 예상된다.
따라서 고성 해양심층수로부터 분리한 48종의 유산균에 대하여 기초 효능평가와 생존율을 분석 후 L. mesenteroides GS76 균주(Kim 등, 2025)를 선별하여 스타터로 제조하였다. 10주 간의 발효과정 동안 스타터 접종 시험구와 비접종 대조구를 비교 분석하여 해당 스타터가 김치 발효 품질의 안정성, 유기산 및 만니톨 생성, 미생물 군집변화, 그리고 발효 기간 단축에 미치는 영향을 규명하고 L. mesenteroides GS76 균주의 스타터로서의 산업적 활용 가능성을 평가하고자 하였다.
2. 재료 및 방법
본 연구에서는 재단법인 발효미생물산업진흥원(Microbial Institute for Fermentation Industry (MIFI, Sunchang, Korea)이 보유한 균주 중 해양심층수에서 분리한 유산균 중 내산성 및 내염성이 우수한 Leuconostoc mesenteroides GS76을 선별하여 발효미생물산업진흥원 발효미생물산업화센터에서 분말 형태의 스타터로 제조하였으며(Kim 등, 2025), 이를 김치 제조를 위한 스타터로 사용하였다. 김치는 강원특별자치도 고성군 관내 업체인 영농조합법인 아라김치(Arakimchi, Goseong, Korea)에서 업체에서 기존에 김치를 생산한 방식 그대로 제조하여 연구에 이용하였다. 사용된 배추는 고성에서 재배된 추광(Brassica rapa subsp. pekinensis)을 사용하였으며, 해양심층수 농축수를 이용하여 절인 후 이용하여 김치를 제조하였다. 김치 양념은 상업적 제조 방식과의 일관성을 확보하기 위해 해당 업체의 기존 제조 방법을 적용하였다. 김치 제조를 위한 양념의 재료로는 무, 고춧가루, 마늘, 천일염, 대파, 양파, 새우젓, 배, 조미육수, 부추, 멸치액젓, 생강, 설탕을 사용하였다. 연구 목적에 따라 스타터는 106 CFU/g의 농도로 조정하여 양념에 첨가한 뒤 균일하게 혼합하였으며, 절인 배추와 스타터를 혼합한 양념을 7:3 비율로 혼합하였다. 해당 업체는 완제품 포장 후 0-1°C의 냉장창고에서 일정 기간 숙성한 뒤 출하하고 있어 본 연구에서도 동일한 조건에서 숙성을 수행하였다. 시료는 업체의 포장 및 보관 절차를 준용하여 제조 완료 후 김장 봉투에 포장하였으며, 숙성기간 동안 7일 간격으로 시료를 수집하여 분석에 사용하였다.
수집한 김치 시료는 분쇄기를 이용하여 고르게 분쇄하여 Whatman filter no. 1 (Cytiva, Little Chalfont, UK) 여과지로 여과하였다. pH 및 총산도의 측정은 자동적정장치 T50 (Mettler Toledo GmbH, Greifensee, Switzerland)을 이용하였고(Oh 등, 2014), 총산도는 시료 2 g에 0.1 N NaOH를 첨가하여 pH 8.3이 될 때까지 소모된 양을 lactic acid로 환산하여 총산도(%)로 표시하였다(Kim 등, 2012). 모든 측정은 3회 반복 수행하였다.
유리당 표준용액은 glucose, sucrose, fructose, D-mannitol (Sigma-Aldrich, St.Louis, MO, USA) 각각을 1.0 mg/mL 농도로 제조하여 여과 후 사용하였다. 유기산 표준물질은 organic acid kit (Sigma-Aldrich)를 사용하여 동일 농도로 제조한 후 여과하여 사용하였다. 유기산 및 만니톨, 유리당 분석은 분쇄된 분석 시료를 13,000 rpm에서 10분간 원심분리한 후, 상등액을 0.45 μm syringe filter (Sartorius, Goettingen, Germany)로 여과하였다. 여과된 시료는 HPLC (Agilent 1200 series, Agilent Technologies, Santa Clara, CA, USA)를 이용하여 분석하였다. 분리에 사용된 column은 Aminex HPX-87H (300×7.8 mm, Bio-RAD, Hercules, CA, USA)였으며, 이동상으로 5 mM sulfuric acid (Sigma-Aldrich)를 사용하였다. 유속은 0.6 mL/min으로 유지하였고, 검출기는 DAD (210 nm)와 RID detector (Agilent Technologies)를 이용하여 동시에 분석을 수행하였다(Jang 등, 2016).
발효 기간별로 수집한 김치 시료로부터 DNA를 추출하기 위한 kit로는 DNeasey Power Food Microbial Kit (Qiagen, Hilden, Germany)를 사용하였다. 각 시료로부터 얻은 genomic DNA의 순도는 1차적으로 NanoDrop One UV-Vis spectrophotometer (Thermo Fisher Scientific, Waltham, MA, USA)로 측정하였으며, 260 nm / 280 nm, 260 nm / 230 nm 값을 산출하였다. Qubit 4 fluorometer (Invitrogen, Carlsbad, CA, USA)를 이용하여 정확한 dsDNA의 농도를 분석하였으며, 0.8% agarose gel 전기영동을 실시하여 DNA 분해 정도와 품질을 최종 확인하였다. 발효 기간에 따라 수집한 시료의 미생물 군집 분석을 위한 16S metagenomic library는 Illumina (Illumina, San Diego, California, USA)사의 16S metagenomic sequencing library에 따라 제작하였다(Illumina, 2013). 16S rDNA 유전자의 V3-V4 부분을 증폭시키기 위한 primer로 16S amplicon PCR forward primer (5’-TCG TCG GCA GCG TCA GAT GTG TAT AAG AGA CAG CCT ACG GGN GGC WGC AG-3’)와 16S amplicon PCR reverse primer (5’-GTC TCG TGG GCT CGG AGA TGT GTA TAA GAG ACA GGA CTA CHV GGG TAT CT A ATC C-3’)를 사용하였으며, 2× KAPA HiFi HotStart Ready Mix (Roche, Basel, Switzerland)를 혼합하여 25 cycle의 1차 PCR을 수행하였다. 1차 PCR 산물은 AMpure XP Bead (BECKMAN COULTER, Brea, California, USA)와 80% ethanol을 이용해 정제하였다. 각 read들의 기원 시료를 구분하기 위한 index로 Nextera XT Index kit v2 (Illumina)를 사용하였으며, 각 library의 말단에 각 index를 부착하기 위한 8 cycle의 2차 PCR을 수행하였으며, 2차 PCR 산물도 동일한 방법으로 AMpure XP Bead (BECKMAN COULTER)를 이용해 정제하였다. 최종 library는 Qubit 4 fluorometer 및 Nanodrop One spectrophotometer (Thermo Fisher Scientific, Waltham, MA, USA)로 농도와 순도를 확인하였으며 0.8% agarose gel electrophoresis를 통해 library와 크기와 품질을 검증하였다. 모든 library는 4 nM 농도로 동일하게 희석하였으며, library와 PhiX control v3 (illumina)를 혼합한 후, MiSeq Reagent Kit v3 (Illumina)를 이용한 MiSeq platform (Illumina)을 활용하여 paired-end 방식의 sequencing을 수행하였다.
생산된 read들의 염기서열 정보를 포함하는 fastq file은 EzBiocloud 16S-based microbiome taxonomic profiling (MTP, CJ Bioscience Inc., Seoul, Korea) pipeline에 업로드하였으며, 미생물 composition, α-diversity, β-diversity 분석에는 comparative MTP analyzer를 사용하여 분석하였다(Yoon 등, 2017). MiSeq platform으로부터 생산된 raw read들로부터 low quality, chimeric, non-target amplicon은 trimming process를 통해 제거하였으며, 마이크로바이옴 분석을 위한 최종 valid read들을 얻었다. 염기서열 정보를 담고있는 read로부터 미생물 분류를 위한 database로는 PKSSU v4.0이 사용되었으며(Yoon 등, 2017), 97%의 염기서열 유사성을 기준으로 미생물 종을 추정치(operational taxonomic units, OTUs)를 산출하였다. 미생물 비율(relative abundance)이 0.0001% 기준으로 noise를 제거하였으며, 김치의 발효 기간에 따른 우점 미생물과 유해 미생물의 비율을 1주일 간격으로 분석하였다.
3. 결과 및 고찰
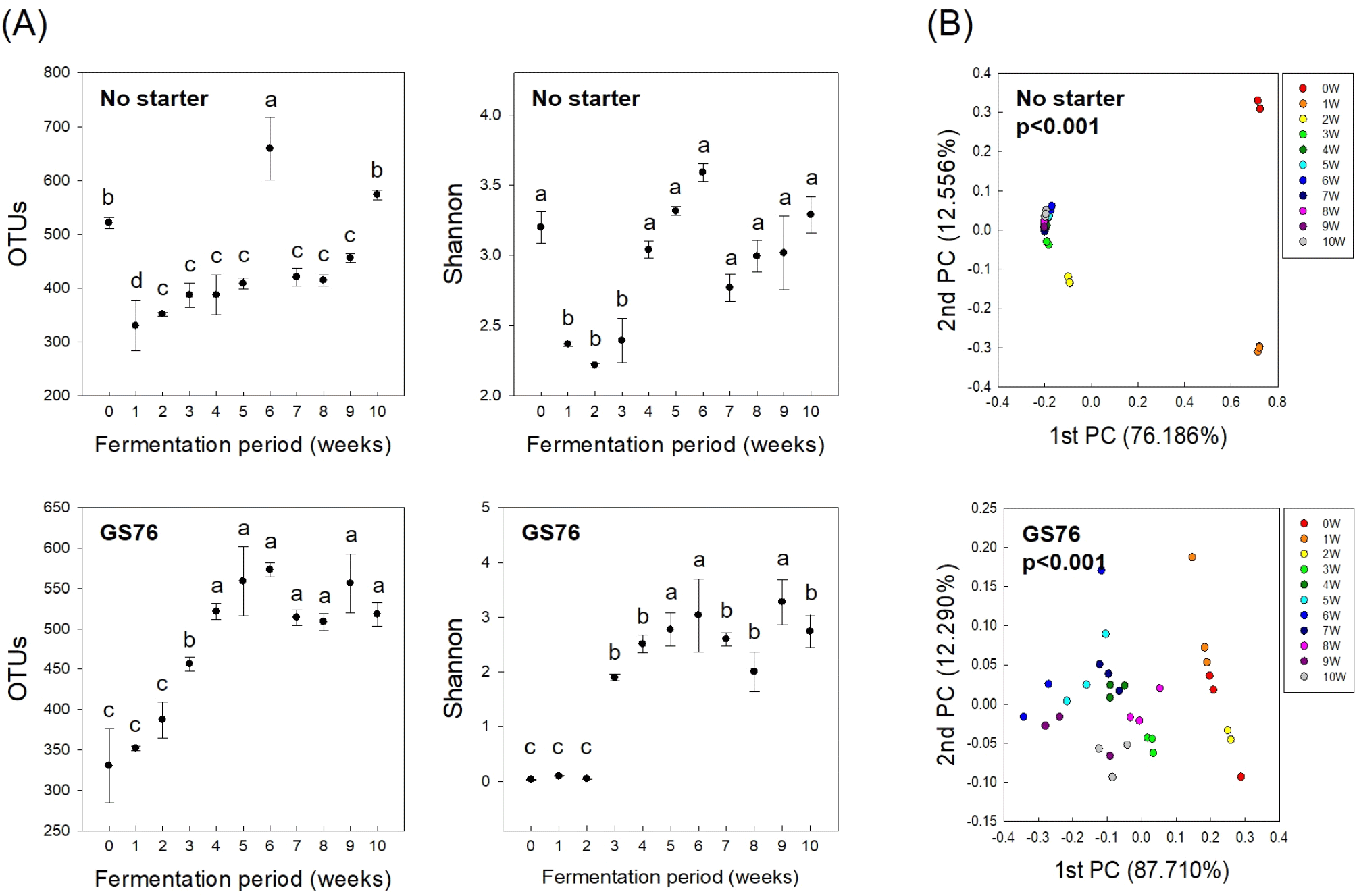
스타터를 접종하지 않은 대조구와 L. mesenteroides GS76을 스타터로 접종한 시험구의 미생물 군집 분포를 속(genus) 및 종(species) 수준에서 발효 기간별로 분석한 결과를 Fig. 1에 나타내었으며, 발효 기간에 따른 종 균등도(evenness) 지수로 사용된 Shannon과 Bray-Curtis dissimilarity metric 기반의 principal coordinate analysis (PCoA) 분석 결과를 Fig. 2에 나타내었다.
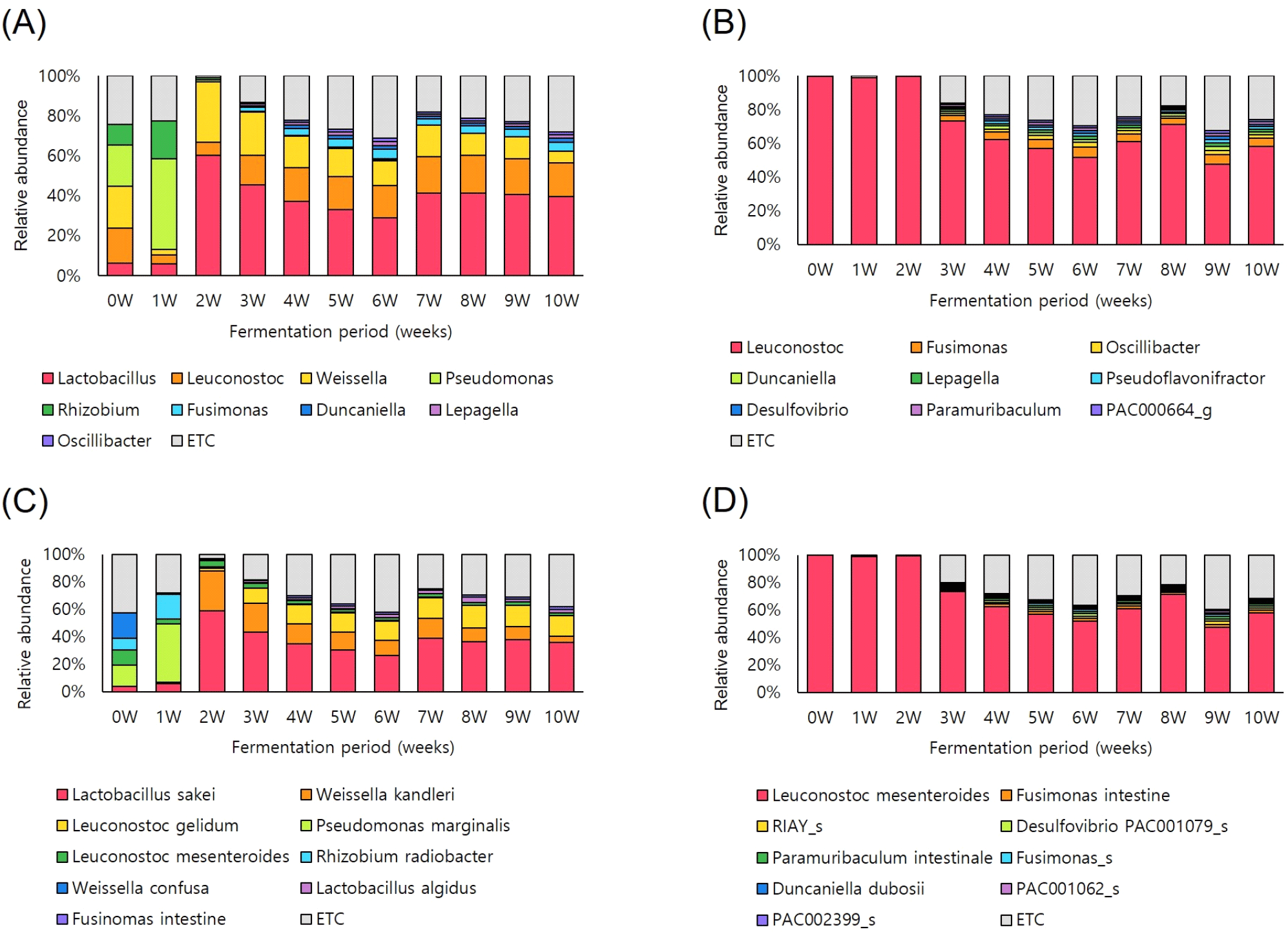
이전 연구(Kim 등, 2016)에 따르면 다양한 상업용 김치에서 Weissella, Lactobacillus, Leuconostoc 속이 주요 우점 미생물로 확인되었다. 특히 Lactobacillus 속은 김치 발효가 진행됨에 따라 pH가 4.3-4.7 수준으로 낮아지는 산성 환경에서 상대적으로 생존에 유리하여 우점화되는 것으로 보고되었다. 본 연구에서도 발효 0-1주 차의 발효 초기 단계에서 스타터를 접종하지 않은 대조구의 경우 Lactobacillus, Leuconostoc, Weissella, Pseudomonas 속이 우점하였다. Song 등(2021)은 원재료에 따라 Weissella, Leuconostoc, Lactobacillus, Pseudomonas 속이 우점할 수 있다고 보고한 바 있으며, 이는 본 연구의 스타터를 접종하지 않은 김치에서 관찰된 미생물 군집구조와 유사하다. 이러한 결과로부터 스타터를 접종하지 않은 김치에서는 발효 초기 단계에 원 · 부재료로부터 기인한 미생물이 우점하는 것으로 판단된다.
발효 기간에 따른 Shannon 지수는 10주 간의 발효 기간 동안 가장 우점하는 것으로 나타난 Lactobacillus 속 미생물의 비율이 증가할수록 낮아지는 경향이 나타나 우점 미생물의 비율이 전체 미생물 군집구조에 큰 영향을 미치는 것으로 나타났다. 발효 기간에 따른 미생물 군집구조 차이를 시각화하기 위한 PCoA 분석 결과 전체 발효 기간에 따라 미생물 군집구조가 통계적으로 매우 유의한 수준(p<0.001)의 차이가 있는 것으로 나타났으나 특히 발효 초기인 0주 차부터 3주 차까지는 미생물 군집구조에 변화가 큰 것으로 나타났으며, 발효 4주 차부터 10주 차까지는 거의 변화가 없는 것으로 나타났다. 이전의 연구 결과(Mannaa 등, 2019)에 의하면 김치 제조를 위한 원 · 부재료의 종류에 따라 2주 차 이후에 미생물 군집구조가 안정화되어 발효 기간에 따른 미생물 구조에 차이가 감소한다고 보고하여 본 연구 결과와 유사하였다. 이러한 결과는 발효 초기에는 원 · 부재료로부터 기인한 다양한 미생물이 존재하지만 발효 기간에 따라 유산균이 생산하는 젖산과 같은 대사산물에 의한 pH 감소로 인해 낮은 pH에 생존이 어려운 미생물의 성장이 억제되기 때문으로 판단된다(Mannaa 등, 2019).
스타터를 접종한 김치에서는 0-3주 차까지는 스타터로 접종한 L. mesenteroides가 99.5% 이상 차지하며 안정적으로 우점하는 것으로 나타났으며, 3주 차 이후에도 48-72%를 차지하며, 10주 동안의 전체 발효 기간 동안 가장 우점하는 미생물로 나타났다. 이러한 결과는 발효 초기 고농도로 접종한 Leuconostoc 속 미생물이 젖산 등 유기산을 생산하여 pH를 조기에 감소시키고, 산성 환경에서 생장하기 어려운 다른 미생물의 성장을 억제했기 때문으로 판단된다. 또한, 발효 기간에 따른 Shannon 지수를 분석한 결과 스타터로 접종한 Leuconostoc 속 미생물의 비율이 99.5% 이상 차지하는 것으로 나타난 발효 초기인 0-2주 차까지는 Shannon 지수가 0 수준으로 나타났으며, Leuconostoc 속의 비율이 낮을수록 Shannon 지수가 높아지는 경향이 나타나 대조구와 시험구 모두 전체 미생물 군집구조가 가장 우점하는 미생물에 큰 영향을 받는 것으로 판단된다.
발효 기간에 따른 미생물 군집구조의 차이를 시각화한 PCoA 분석 결과, 10주간의 전체 발효과정에서 미생물 군집구조가 통계적으로 매우 유의하게(p<0.001) 변화한 것으로 나타났으나 0주 차부터 2주 차까지의 미생물 군집구조가 유사하고, 3주부터 10주까지의 미생물 군집구조가 유사한 것으로 나타났다. 대조구와 L. mesenteroids GS76을 스타터로 사용하여 제조한 두 김치는 동일한 원 · 부재료를 사용하고 동일한 발효조건 및 환경에서 제조되었으나 발효 기간에 따른 미생물 군집구조에는 뚜렷한 차이가 있는 것으로 나타났다. 이전의 연구 결과에 의하면 다양한 전통 발효식품의 미생물 군집구조를 분석한 결과 스타터 사용 여부가 미생물의 군집구조에 중요한 결정 요인이었음을 보고한 바 있으며(Gautam 등, 2025), 발효식품에서 스타터를 접종했을 때 자연 유래 미생물의 성장이 억제된다는 연구(Zang 등, 2018)가 보고된 바 있어 발효식품 제조 시 스타터의 사용이 군집구조에 큰 영향을 미치며, 표준화된 제품 생산을 위해 스타터의 사용이 중요할 것으로 판단된다.
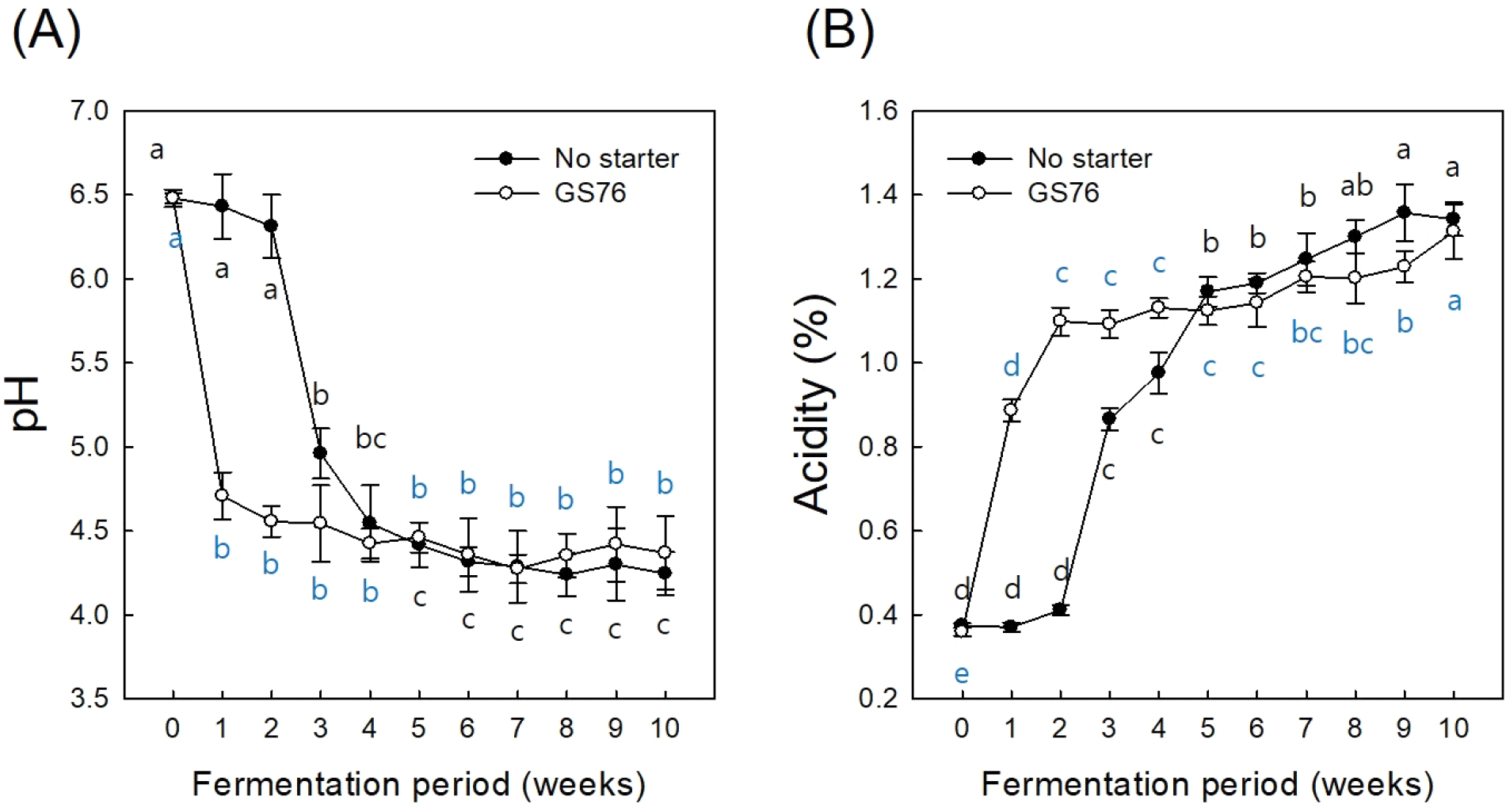
스타터를 접종하지 않은 김치와 L. mesenteroides GS76을 스타터로 접종한 김치를 0-1°C에서 10주간 발효시키며 측정한 pH 및 산도를 Fig. 3에 제시하였다. 0주 차부터 2주 차까지 발효 초기에는 스타터를 접종한 시료에서 pH 감소와 산도 증가 속도가 비접종 시료에 비해 빠르게 나타났다. 김치의 상미범위로 알려진 적정산도 0.6-0.8%에 도달하는데(Jeong 등, 2004) 스타터를 접종한 김치는 1주 이내, 대조구는 2-3주가 걸리는 것으로 분석되었다. 이는 발효 초기 L. mesenteroides가 우점하며 젖산을 포함한 유기산 생산을 촉진한 반면, 비접종 대조구에서는 Lactobacillus 속 미생물이 점차 우점하면서 산 생성이 늦게 일어난 결과로 해석된다. 또한, Weissella 속 미생물은 스타터 접종군에서 초기 발효를 보조하며 젖산과 아세트산을 동시에 생성하지만, L. mesenteroides에 비해 발효 속도가 느린 것으로 보고된 바 있다(Mheen, 2003). 이러한 차이는 발효 초기 산도 변화와 발효 속도의 차이를 설명하며, 스타터 접종의 효과를 뒷받침한다. L. meseteroides GS76을 접종한 김치에서는 발효 0주 차부터 유산균의 비율이 99.5% 이상을 차지하며 pH와 산도가 빠르게 변화하였으며, 스타터를 접종하지 않은 김치에서는 유산균의 우점도가 크게 증가한 2주 차부터 빠르게 변화하는 것으로 나타나 Leuconostoc 속 미생물을 스타터로 사용한 김치에서 대조구 대비 pH 감소 속도가 빠르다는 이전의 연구 결과(Li 등 2020)와 유사한 경향을 보였다. pH와 산도는 김치의 발효 진행 정도, 숙성 상태를 나타내는 평가 지표로 사용되며(Jeong 등, 2011), 이는 첨가한 스타터가 발효 속도를 조절함으로써 김치의 발효 기간을 단축하여 기존의 제품 출고일보다 제품을 빠르게 출하할 수 있음을 시사하며, 상업적 측면에서 스타터 사용의 경제적 유용성을 확인할 수 있었다.
L. mesenteroides는 김치를 포함한 다양한 발효식품의 초기 발효를 주도하는 대표적인 이형발효 유산균으로 pH 5.5-6.5 범위의 산성 환경에서도 생육이 가능하며, 과당과 포도당을 탄소원으로 활용하여 만니톨을 생산하고 젖산, 아세트산, 에탄올 및 이산화탄소 등 다양한 대사산물을 생산하는 것으로 알려져 있다(Cogan 등, 1994). 특히 만니톨은 김치의 풍미, 식감 및 품질 안정성에 중요한 역할을 하며(Carvalheiro 등, 2011; Lee 등, 2021), 발효 균형과 맛의 완성도를 반영하는 지표 물질로도 활용된다. 과당은 L. mesenteroides가 생산하는 만니톨 탈수소효소에 의해 환원되어 만니톨로 전환되며(Slantner 등, 1998), 이 과정은 발효식품의 풍미 형성과 품질 안정성에 기여한다.
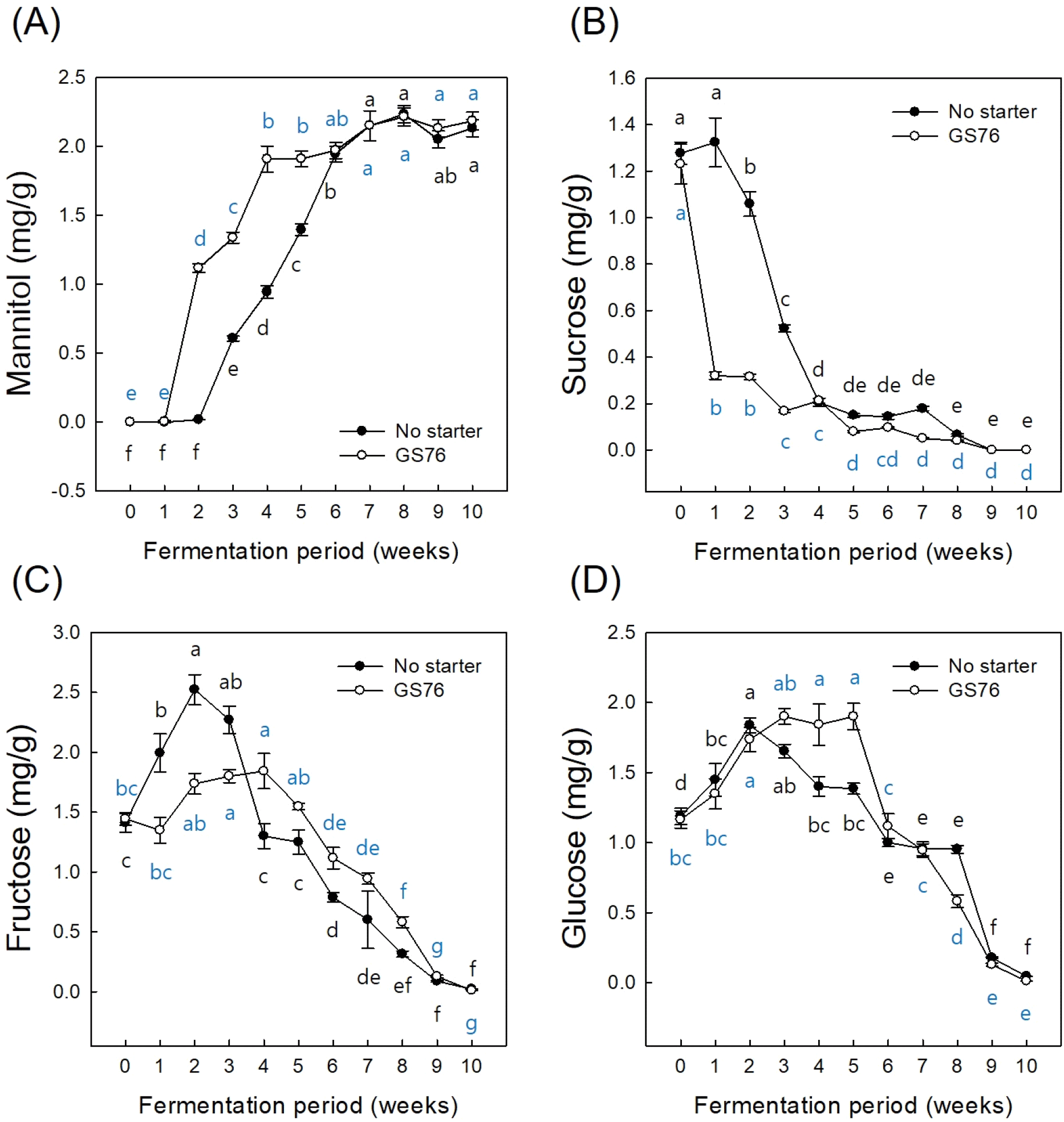
본 연구에서 GS76 스타터를 접종한 시험구에서는 발효 초기 만니톨 생성이 대조구 대비 유의하게 빠르게 진행되었으며(Fig. 4), 발효 1-2주 차에 만니톨 함량이 1.0 mg/g에 도달하였다. 반면 스타터 비접종 대조구에서는 발효 3주 차에 만니톨 함량이 0.5 mg/g 수준에 도달하여 스타터 접종이 초기 만니톨 생성에 영향을 미치는 것으로 확인되었다. 발효 기간 동안의 유리당 함량 변화를 분석한 결과 자당은 발효 초기에 1.2 mg/g으로 가장 높은 함량을 나타낸 후 지속적으로 감소하였다. 반면 과당과 포도당은 발효 초기 증가했다가 중기 이후 추세적으로 감소하였다. 이는 스타터를 접종한 시험구에서 자당이 L. mesenteroides가 생산하는 sucrose phosphrylase 및 dextransucrase 효소 작용에 의해 과당과 포도당 전구체로 전환되었기 때문으로 판단된다(Dols 등, 1997; Goedl 등, 2007; Schwarz 등, 2007). 발효 초기 시험구에서는 생성된 과당이 만니톨 생산에 사용되어 과당 축적이 적게 나타난 반면 대조구에서는 초기 우점 균주의 만니톨 생성 능력이 낮아 과당이 상대적으로 더 많이 축적된 것으로 판단된다(Kim 등, 2002). 이후 발효 중기에는 두 시료 모두 과당과 포도당이 주요 탄소원으로 활용되며 농도가 감소하였다.
발효 기간 동안의 유기산 함량 변화를 분석한 결과 스타터를 접종한 시험구에서는 구연산이 시간 경과에 따라 완만히 감소하였으며, 젖산의 농도는 발효 초기부터 증가하여 4주 차 이후 안정화되었으며, 아세트산은 발효 중기까지 증가한 후 후기에 다시 감소하였다(Fig. 5). 이는 시험구에서 L. mesenteroides가 초기부터 안정적으로 우점하여 일부 구연산이 젖산 및 만니톨 생성에 사용되었기 때문으로 예상된다(Marty-Teysset 등, 1996; Ricciardi 등, 2022). 반면 대조구에서는 발효 중기 이후 L. sakei, L. plantarum, Weissella spp. 등 구연산 이용 능력이 높은 유산균이 우점하면서 구연산이 급격히 감소한 것으로 판단된다(Marty-Teysset 등, 1996; Schmitt 등, 1997). 젖산 생성량은 발효 초기에는 시험구에서 다소 높았으나, 중기 이후에는 대조구에서 약 2배 높은 수준을 보였다(Kim 등, 2002). 이는 대조구에서 중기 이후 Lactobacillus, Weissella 속 미생물이 빠르게 증식하며 젖산을 대량 생산하기 때문으로 판단된다. L. mesenteroides는 이형발효 유산균으로 동형발효 유산균에 비해 젖산 생성량이 낮지만, 스타터로 첨가된 GS76이 초기부터 우점한 시험구에서는 경쟁 미생물의 생장이 억제되고 일부 탄소원이 만니톨 등 다른 대사산물 생산에 활용됨에 따라 전체적인 젖산 농도가 비교적 안정적으로 유지된 것으로 예상된다. 아세트산은 시험구에서 발효 초기부터 우점한 L. mesenteroides에 의해 빠르게 증가하였으나, 스타터를 접종하지 않은 대조구에서는 발효 2주 차 이후 Lactobacillus, Weisella 속 미생물의 우점도가 높아지는 2주 차 이후 아세트산의 농도가 증가하는 것으로 나타났다(Shim 등, 2012).
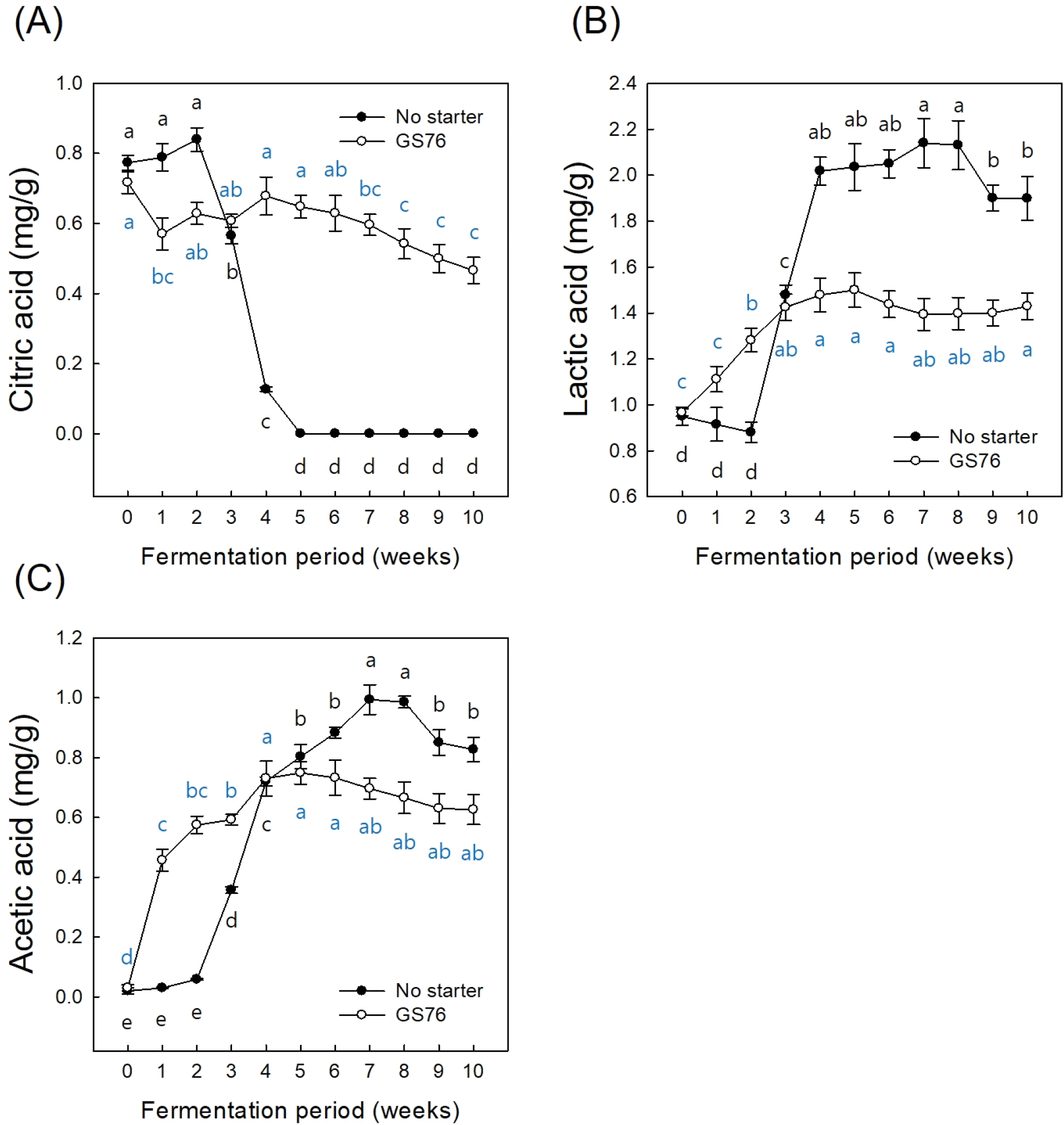
스타터를 접종한 시험구에서는 발효 초기부터 만니톨과 젖산 생산이 촉진되어 발효 속도가 빠르고 품질이 안정적으로 유지되었다(Jang 등, 2016). 발효 후기에는 시험구와 대조구 모두 산도, 만니톨, 유리당 및 유기산 농도가 유사하게 나타났는데, 이는 서로 다른 미생물 군집이라도 기능적 중복성(functional redundancy)을 통해 유사한 대사 기능을 수행하기 때문으로 예상된다(Jung 등, 2011; Lee 등, 2015). 특히 시험구에서 유기산의 변화량이 대조구에 비해 완만하게 나타난 것은, L. mesenteroides GS76이 발효 초기부터 안정적으로 우점하여 유기산 생성이 균일하게 이루어지고, 경쟁 미생물의 과도한 증식이 억제되며, 일부 탄소원이 만니톨 등 다른 대사산물 생산에 활용되었기 때문으로 판단된다. 이러한 결과는 발효 기간 단축, 품질 균일화, 감미와 산미의 조화 유지 등 산업적 김치 생산에서 스타터 사용의 장점을 뒷받침하며, 발효과정의 안정성과 재현성을 확보할 수 있음을 시사한다(Jang 등, 2016).
김치 내 유산균의 증식은 Bacillus cereus, Staphylococcus aureus와 같은 유해 미생물 및 식중독 미생물의 제어에 중요한 요인으로 알려져 있다(Kim 등, 2008). 스타터를 접종하지 않은 김치와 L. mesenteroides GS76을 스타터로 접종한 김치의 발효 0주 차부터 10주 차까지 Bacillus cereus, Escherichia coli, Staphylococcus aureus, Pseudomonas spp., Enterobacteriaceae와 같은 부패 원인균 또는 유해 미생물의 분포를 분석하였다. 스타터를 접종하지 않은 대조구에서는 Escherichia coli, Staphylococcus aureus는 발효 1주 차, Bacillus cereus, Enterobacteriaceae는 2주 차, Pseudomonas spp.는 3주 차부터 비율이 유의하게 감소하는 것으로 나타나 대조구에서 2주 차 이후 Lactobacillus의 비율이 증가하면서 발효 기간에 따라 저해되는 것으로 예상된다. 반면, L. mesenteroides GS76을 스타터로 접종한 김치에서 대부분의 발효 기간 동안 유해 미생물의 비율이 더 낮은 것으로 나타났으며, 특히 대조구에 비해 발효 0주부터 1주 차의 발효 초기에 유해 미생물의 비율이 더 낮은 것으로 나타났다(Fig. 6). 이는 Leuconostoc mesenteroides 균주가 Staphylococcus aureus, Salmonella spp., Escherichia coli 등 24종의 식중독균에 대해 강력한 항균 활성을 보인다는 연구결과가 보고된 바와 유사하였다(Ahmed, 2019). 이는 발효 초기 단계에서 L. mesenteroides GS76이 빠르게 증식하여 젖산 및 아세트산과 같은 유기산을 다량 생성함으로써 김치 내 pH를 저하시켜 유해 미생물의 생육을 억제한 결과로 판단된다. 본 연구 결과, 스타터를 접종한 김치는 발효 초기 단계에서 대조구 대비 유해 미생물의 비율이 낮게 관찰되었으며, 이러한 결과는 스타터 사용이 김치 발효 과정 중 유해 미생물 오염을 억제하여 제품의 안전성을 향상시킬 가능성을 시사한다.
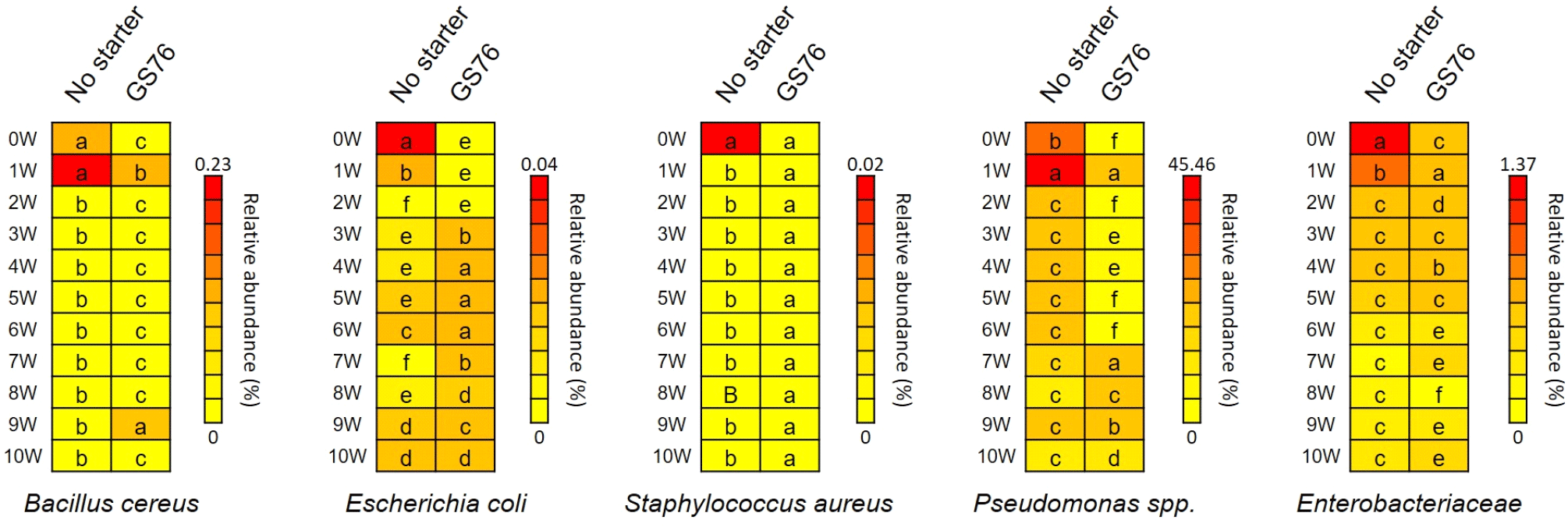
본 연구에서 L. mesenteroides GS76 스타터를 접종한 시험구는 비접종 대조구와 비교했을 때 김치의 발효 전반에서 뚜렷한 차이를 나타냈다. 시험구는 발효 초기 pH 감소와 산도 증가가 빠르게 진행되어 대조구 대비 적정 산도에 1-2주 빠르게 도달하였으며, 이는 발효 초기부터 스타터로 접종한 GS76이 안정적으로 우점하여 발효를 주도한 결과로 판단된다. 시험구에서는 발효 전 기간 동안 L. mesenteroides가 높은 비율을 유지하며 미생물 군집구조가 안정적으로 유지된 반면, 대조구는 발효가 진행됨에 따라 원재료로부터 기인한 것으로 예상되는 미생물에서 Lactobacillus로 우점종이 전환되는 등 군집 변화의 폭이 큰 것으로 나타났다. 또한 시험구에서는 발효 초기에 김치의 풍미 향상과 기호도에 긍정적인 영향을 미치는 것으로 알려진 만니톨의 함량이 높았으며, 유해 미생물의 성장을 억제시키는 것으로 나타나 해양심층수 유래 L. mesenteroides GS76이 김치의 제품 출하를 위한 발효 기간 단축과 균일한 발효 품질 확보 및 보존성과 저장성 향상을 위한 스타터로서 상업적으로 활용 가치가 높을 것으로 판단된다.
4. 요약
본 연구는 해양심층수 유래 L. mesenteroides GS76 스타터가 김치 발효에 미치는 영향을 평가하기 위해 수행되었다. L. mesenteroides GS76은 강원도 고성의 해양심층수 소재에서 분리되었으며, 발효미생물산업진흥원에서 분말형 스타터로 제조되었다. 김치는 스타터를 접종한 시험구와 비접종 대조구로 구분하여 제조하였으며, 0-1°C에서 10주 동안 발효시켰다. 발효과정 중 pH, 산도, 만니톨, 유리당, 유기산 등의 이화학적 특성을 분석하였으며, 미생물 군집의 변화는 NGS를 이용하여 분석하였다. 스타터를 접종한 김치는 발효 초기 2주 이내에 pH가 빠르게 감소하고 산도가 증가하였으며, 대조구에 비해 발효 초기 단계에서 만니톨 함량이 빠르게 증가하였다. L. mesenteroides는 발효 전 과정에서 우점 미생물로 유지되어 미생물 군집의 안정성을 확보하였으며, 이러한 결과는 해양심층수 유래 스타터가 발효과정을 효과적으로 단축하면서 일정한 품질과 조절된 대사 특성을 유지함을 나타냈다. 본 연구 결과는 스타터의 적용이 발효 기간 단축 및 유해 미생물의 성장 억제를 통해 산업적으로 김치의 생산성을 향상시킬 수 있음을 시사하며, 해양심층수 유래 L. mesenteroides GS76이 김치 제조 스타터로서 산업적인 활용 가치가 있을 것으로 판단된다.










