1. 서론
한약재로 많이 사용되어 온 인삼은 장시간 보관하기 위해 백삼으로 건조하여 널리 사용되어 왔으나 백삼도 오랫동안 보관할 시 해충이 번식하여 장기 저장에는 한계가 있다. 우리 선조들은 이러한 문제를 해결하는 방법으로 식품이나 한약재를 찌거나 삶아서 해충의 알을 죽인 후 건조하여 장기간 보관하는 방법을 개발해 왔다(Lee, 2020; Nam 등, 2012). 태극삼은 동남아시아 시장에서 홍삼의 수요가 급격히 증가하는 시기에 홍삼전매제도로 홍삼의 공급이 부족해지자 민간에서 수출상품으로 개발되었다(Jang과 Jeong, 2014). 태극삼의 제조 초기에는 인삼을 물에 넣어 삶은 후 건조하여 태극삼을 제조하였으나, 현재 태극삼은 여러 번 찌고 말리는 홍삼, 흑삼의 제조와 유사하게 제조 현장에서 90-100°C 범위에서 1회의 찌고 말리는 과정으로 제조하는 경우가 많다(Lee, 2022).
태극삼은 표피의 일부 전분을 호화시켜 만든 제품으로, 색상은 홍삼과 같이 연한 갈색을 띠고 있지만, 황색에 가깝다. 표피를 제거하지 않아 표피가 피부백삼과 비슷하지만, 절단 시 단면이 담홍갈색으로 둥근 환을 이루고 있어 홍삼과 차이가 난다(Jang과 Jeong, 2014).
태극삼은 1회의 열탕처리 또는 증숙과정을 거침으로서 ginsenoside의 변환이 일부 일어날 수 있으나 ginsenoside 조성이 거의 백삼에 가까우며. 홍삼에서 생성되는 ginsenoside Rg3는 거의 나타나지 않는다(Hwang 등, 2005: Lee 등, 2013). 그러나 Lee(2022)는 수삼을 초산용액에서 침지 및 증숙처리를 함으로서 면역활성 효능이 있는 ginsenoside Rg3가 발현되어 ginsenoside Rg3가 풍부한 태극삼을 제조한 바 있다.
인삼의 ginsenoside와 산성다당체는 추출용매에 대한 용해도가 서로 다르므로 용매를 바꾸어가면서 반복 추출해야만 충분한 함량의 수율을 얻을 수 있다(Lee, 2023). 인삼의 ginsenosides는 물보다는 상대적으로 비극성인 ethanol에 잘 녹지만(Nam, 1996), 인삼 산성다당체는 고분자로서 ethanol뿐만 아니라 물에도 용해도가 낮아 낮은 온도에서 여과 시 많이 제거되는 경향이 있으나, 찌고 말리는 과정을 반복한 홍삼, 흑삼 등의 산성다당체는 저분자화되면서 용해도가 증가하여 잘 녹는다(Lee, 2023).
백삼, 태극삼, 홍삼, 흑삼 등의 추출방법은 열수로 장시간 추출하는 전통적인 방법이 주로 사용되고 있으나, 최근 산업체에서는 70% ethanol 용액으로 홍삼을 추출하는 방법이 많이 적용되고 있다(Lee 등, 2013). 인삼의 열수 추출에서는 산성다당체 등 수용성 성분이 많이 추출될 수 있으나, 물에 잘 용해되지 않는 ginsenosides는 추출 수율이 낮다(Li 등, 2009).
본 연구에서는 태극삼의 기능성 성분 추출을 위해 추출용액의 ethanol 농도와 추출 온도에 따른 가용성 고형분 함량, ginsenosides 함량 및 산성다당체 함량의 변화를 모니터링하고, 그 조건을 최적화하기 위해 반응표면분석을 하였다.
2. 재료 및 방법
실험 재료인 태극삼은 6년근 수삼을 사용해 만든 태극삼의 주근을 금산군에 소재하는 우신산업㈜에서 구입하여 사용하였다. 추출 및 분석 실험에 사용된 시약은 ginsenoside Rg1, Rb1, Re, Rb2, Rb3, Rh4, Rf(Wako, Osaka, Japan), D-(+)-galacturonic acid monohydrate(Sigma Chemical Co, St. Louis, MO, USA), acetonitrile(JT Baker, Philipsburg, PA, USA), H2SO4(Sigma Chemical Co), methanol(JT Baker), carbazole(Sigma Chemical Co.), ethanol(삼전화학, 서울, 대한민국) 등이다.
건조 태극삼 주근의 분쇄는 분쇄기를 이용하여 25 mesh 이하로 분쇄하여 수분함량 9.45%인 분말을 추출에 사용하였다. 추출은 태극삼 20 g을 500 mL 삼각 flask에 넣고 추출용매 200 mL를 첨가한 후 100 rpm에서 24시간 동안 교반하여 가용성 고형분, ginsenosides, 산성다당체 등을 추출하였다. 이때 추출조건은 실험계획에 따라 ethanol 함량을 0-80%로 설정하고, 추출 온도는 60-80°C로 각각 설정하여 추출하였다.
본 실험은 태극삼 추출에 따른 가용성 고형분 함량, ginsenosides 함량, 산성다당체 함량 등의 변화를 조사하고자 반응표면분석을 시행하였다. 이때 실험계획은 중심합성계획법(Park, 1991)으로 설계하였으며, 중심합성 실험계획법으로 설계된 태극삼의 추출조건은 ethanol 용액의 ethanol 농도(X1)와 추출 온도(X2)로 다섯 단계로 부호화(−2, −1, 0, 1, 2)하여 실험값을 나타내었다(Table 1). 그리고, 이러한 조건변수에 대한 반응변수들은 3회 반복 측정하여 그 평균값을 이용하여 반응표면을 SAS 프로그램(SAS Institute Inc, Cary, NC, USA)으로 분석하였다.
태극삼의 수율을 측정하고자 태극삼 추출물의 가용성 고형분의 함량을 측정하였다. 즉, 항량을 구한 수기에 추출물 50 mL를 넣고 105°C 항온기에서 증발건조시킨 후 그 무게를 달았으며, 태극삼의 가용성 고형분 수율은 %로 나타내었다.
Ginsenosides는 건강기능식품공전(2023)의 시험방법을 이용하여 시험용액을 조제하여 측정하였다.
시험용액은 50 mL mass flask에 태극삼 추출액 5.0 mL를 취한 다음 70% methanol로 용해한 후 0.45 μm 막 필터로 여과하여 일정 농도로 희석하였다.
시험용액 정제를 위해 C18 cartridge에 methanol과 증류수 각각 5 mL와 10 mL를 순서대로 통과시킨 다음 시험용액 5 mL를 통과시켜 시험용액을 흡착시켰다. 시험용액이 흡착된 cartridge에 증류수와 25% methanol 각각 25 mL와 10 mL로 2-3 mL/min의 유속으로 불순물을 제거한 다음 methanol로 ginsenosides를 용출시켰다. 이 용출액은 5 mL mass flask에 넣고 methanol로 정용한 것을 측정용 시험용액으로 희석하여 사용하였다.
태극삼 ginsenosides 분석은 HPLC-UVD(2489UV, Waters, Milford, MA, USA)을 사용하였다. 분석조건은 Xbridge C18 column(4.6×250 mm, 5 μm, Merck, Darmstadt, Germany)에 시료 10 μL를 주입하였으며, 검출기의 파장이 203 nm, column 온도가 30°C이었다. 여기서 이동상의 A 용액으로 증류수를, B 용액으로 acetonitrile를 혼합 용매로 사용하였고, 유속이 1.0 mL/min, 0-55 min 동안 B액을 20-50%로 점점 증가시킨 다음, 55-75 min 동안 55-20%로 점점 감소시키면서 분석하였다.
태극삼 산성다당체의 추출은 Cho 등(2008)의 방법으로 15 mL falcon tube에 태극삼 추출액과 증류수를 각각 1 mL, 10 mL 넣은 다음 80°C, 15 min 동안 추출액을 완전히 용해시켰다. 녹은 용액을 100 mL mass flask에 넣고 표선까지 증류수를 채운 후 3,000 rpm, 15 min 동안 원심분리(Micro 12, Hanil Sci. Inc., Incheon, Korea)를 한 후 상징액을 0.45 mL 막 필터로 여과하였다. 이렇게 얻은 여액을 일정 농도로 희석하여 태극삼 산성다당체의 정량에 사용하였다.
태극삼의 산성다당체 정량은 산성다당체 용해액, carbazole, sulfuric acid를 각각 0.5 mL, 0.25 mL, 3 mL를 순서대로 넣고 충분히 혼합하였다. 공시험구는 carbazole 대신 ethanol 0.25 mL를 넣고 sulfuric acid 3 mL를 첨가하였다. 85°C에서 5분간 수욕조에서 가온한 다음 15 min 간 상온에서 정치한 후 UV spectrophotometer(SpcetraMax ABS, Molecular Devices Co, St. San Jose, CA, USA)를 이용하여 525 nm에서 O.D.를 측정하였다. 이때 galacturonic acid monohydrate를 표준물질로 사용하였다.
3. 결과 및 고찰
태극삼의 추출 수율을 조사하고자 각각의 추출조건별 가용성 고형분 함량을 측정하였다. 추출조건에 따른 태극삼의 가용성 고형분 함량은 32.44-60.58 g/100 g이었다(Table 1). 이를 회귀분석하였으며, 태극삼 가용성 고형분의 모델식 R2은 0.8894(p<0.05)로 통계적으로 유의하였다(Table 2). Lee(2023)는 홍삼과 흑삼의 추출 수율을 조사하여 흑삼이 다소 낮게 조사되었으나 홍삼과 흑삼의 ethanol 용액 추출 수율의 차이는 크지 않는 것으로 보고하였다. 그러나 홍삼과 흑삼의 추출 수율이 22-54%로 보고되어 태극삼의 ethanol 용액 추출 수율이 상대적으로 높은 것을 확인할 수 있었다. 이러한 현상은 태극삼이 상대적으로 열처리가 적게 일어나고 증숙과정에서 가용성 고형분이 적게 소실되기 때문으로 여겨진다.
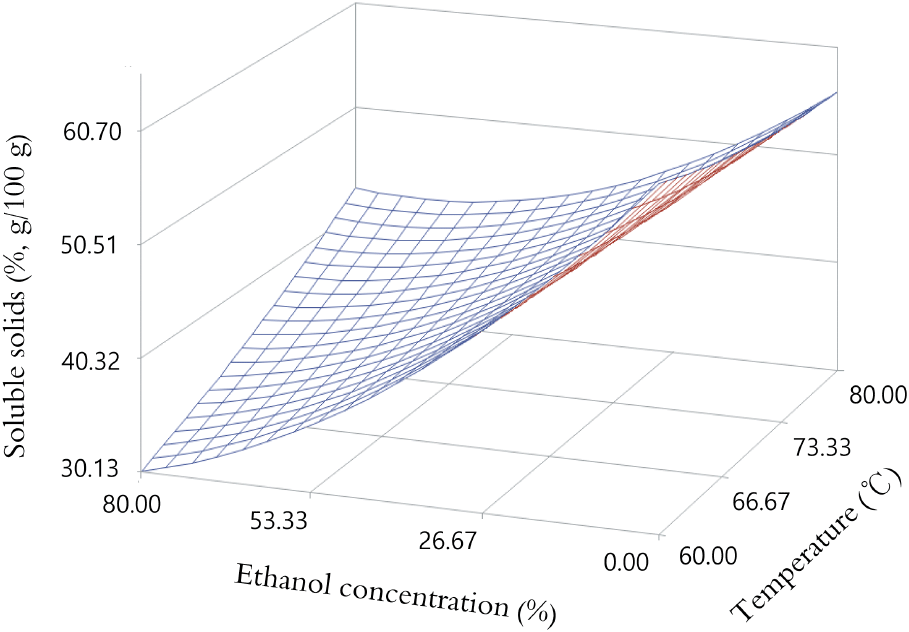
태극삼의 가용성 고형분에 대한 ethanol 농도와 추출 온도의 영향을 조사하고자 F값을 구해보았으며(Table 2), 추출용매인 ethanol 농도의 F값이 10.32(p<0.05)로 ethanol 농도가 태극삼의 가용성 고형분의 추출에 큰 영향을 미치고 있었으나, 추출 온도의 영향은 낮았다. 그리고 능선분석을 통해 최대 및 최소 추출조건을 분석해 보았으며(Table 3), 반응표면의 모형은 최소점의 형태였으며, ethanol 농도 0.22%, 추출 온도 68.96°C에서 고형분의 수율이 57.81%로 최대가 되었으나, ethanol 농도 72.18%, 추출 온도 64.06°C에서 고형분의 수율이 32.99%로 최소가 되었다. 이러한 태극삼 수율의 최적 추출조건인 ethanol 농도 0.22%와 추출 온도 68.96°C는 태극삼의 주된 성분이 대부분 가용성 성분으로 에탄올보다는 물에서 더 잘 추출되기 때문으로 여겨지며, ethanol 농도가 낮고 추출온도가 약 67°C인 홍삼 및 흑삼의 추출 최적 조건과도 큰 차이가 없었다(Lee, 2023). 태극삼의 고형분 함량은 ethanol의 농도가 낮을수록 상대적으로 증가하였으며, 온도의 변화에 따른 수율의 변화는 상대적으로 적었으나, ethanol 농도가 높은 조건에서만 추출 온도가 증가할수록 다소 증가하였다(Fig. 1). 이러한 반응표면의 패턴은 증숙과정을 1회만 시행하는 태극삼이 증숙과정에서 가용성 고형분의 소실이 적으므로 홍삼보다 상대적으로 가용성 고형분의 추출 수율이 높게 나타났으나 추출패턴은 홍삼의 반응표면 패턴과 유사하였다(Lee, 2023).
본 연구에서는 태극삼의 ginsenoside Rg1, Rb1, Re, Rb2, Rb3, Rh4 함량을 측정해 반응표면분석을 통해 ginsenosides 각각의 함량 변화와 총 ginsenoside 함량 변화를 모니터링하였다. 추출조건에 따른 태극삼의 ginsenoside 함량(Table 1)은 ginsenoside Rg1 1.60-4.04 mg/g, Rb1 1.90-5.67 mg/g, Re 0.72-1.40 mg/g, Rb2 0.70-2.36 mg/g, Rb3 0.60-2.14 mg/g, Rh4 0.81-2.33 mg/g 그리고 총 ginsenoside 6.34-18.71 mg/g의 범위로 나타났다(Table 1).
태극삼 ginsenosides에 대한 회귀분석 결과 ginsenoside Rg1, Rb1, Rb2, Rb3에 대한 모델식의 R2은 각각 0.8361(p<0.10), 0.9330(p<0.05), 0.9924(p<0.01), 0.9649(p<0.01)로 통계적으로 유의하였으나, ginsenoside Re, Rh4 등은 유의성이 인정되지 않았다. 그리고 총 ginsenoside에 대한 모델식의 R2는 0.9354 (p<0.05)로 유의미하였다(Table 2).
조건변수의 영향을 알아보고자 총 ginsenoside의 F값을 구해보았으며(Table 2), ethanol 농도의 F값이 18.65(p<0.01)로 ginsenoside 추출에 큰 영향을 미치는 것으로 나타났으나 추출 온도의 영향은 거의 없었다. Ginsenoside Rg1, Rb1, Re, Rb2, Rb3, Rh4의 F값 또한 총 ginsenoside의 F값과 큰 차이가 없었다(Table 2). 이러한 결과는 홍삼의 ethanol 용액 추출 시 대부분 추출 온도보다는 ethanol 농도의 영향을 주로 받고 있다는 Lee(2023)의 연구결과와 유사한 경향이었다.
태극삼의 ethanol 용액 추출에 따른 총 ginsenoside의 반응표면은 ethanol 농도가 감소할수록 비례적으로 감소하는 경향을 나타내었다(Fig. 2). 각각의 ginsenoside인 Rg1, Rb1, Rb2, Rb3의 반응표면들 또한 총 ginsenoside의 반응표면과 같이 ethanol 농도가 감소할수록 비례적으로 감소하는 경향을 보여 거의 차이가 없었다(Fig. 3). 가용성 고형분과 산성다당체는 친수성 성분이 많으므로 ethanol 함량이 낮은 조건에서 수율이 높게 나오지만, ginsenosides는 물보다 ethanol 용해성이 우수하여 ethanol 농도가 높은 조건에서 잘 추출되는 것으로 알려져 있다(Nam, 1996).
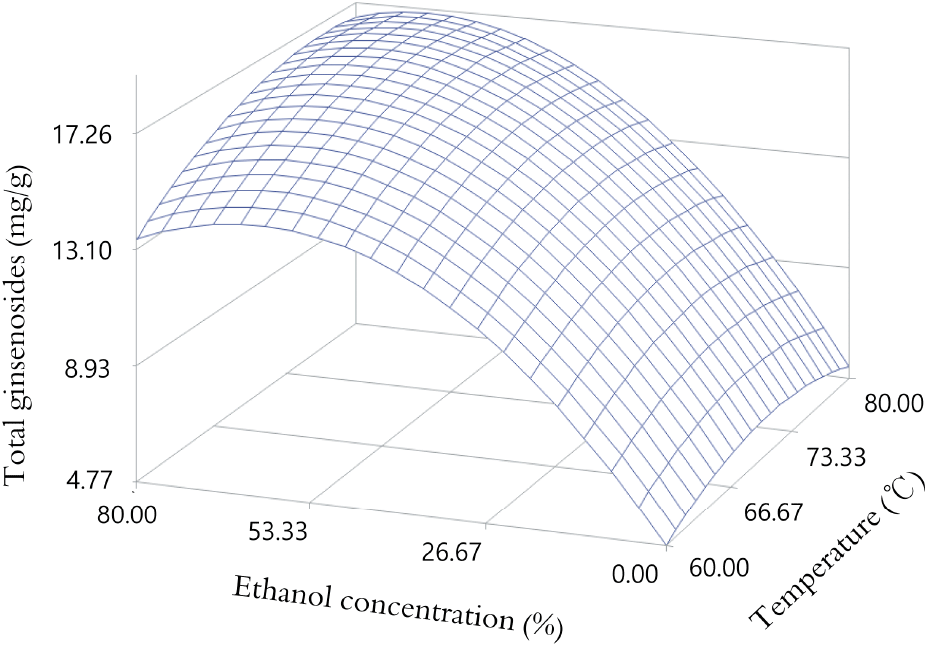
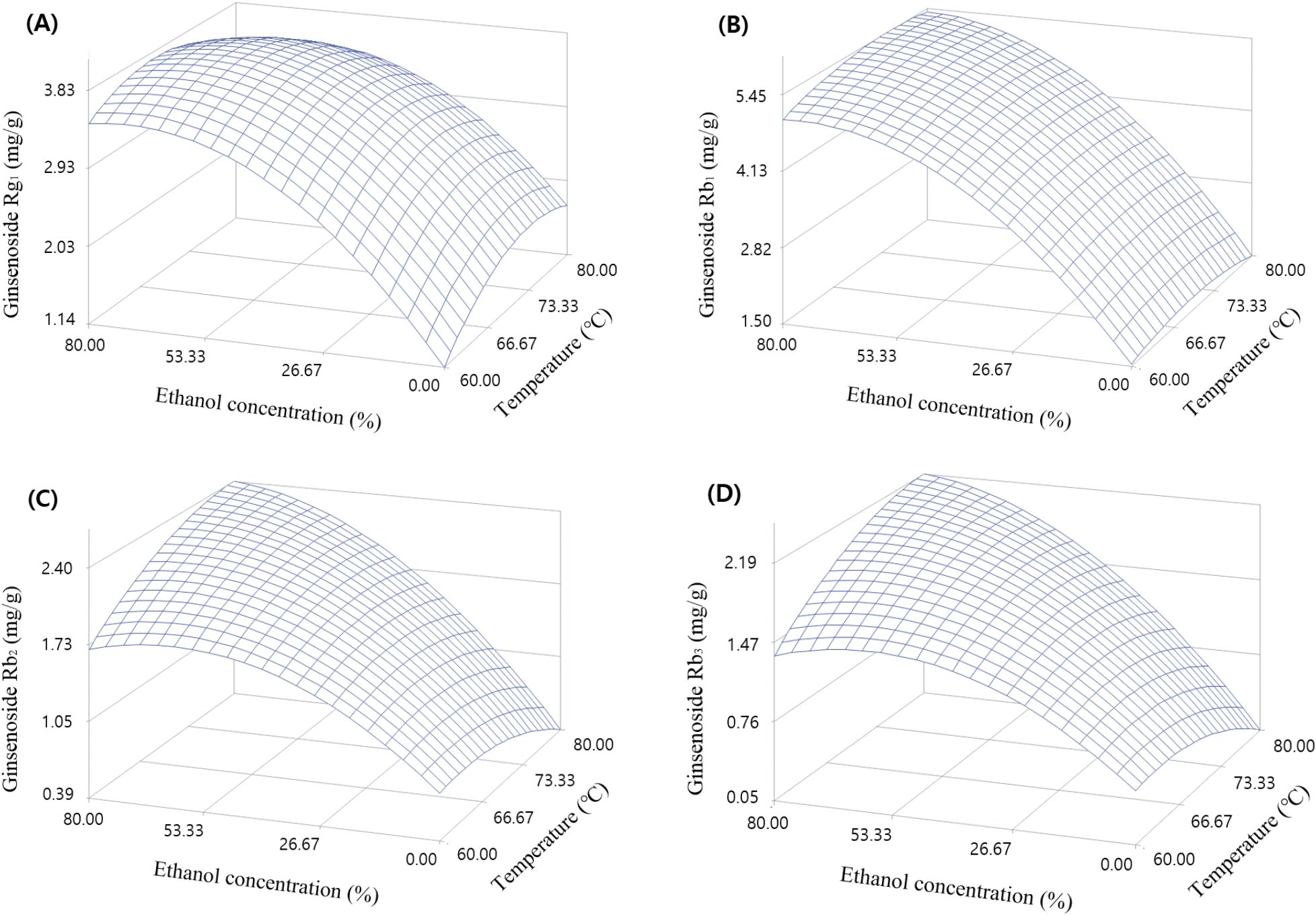
그리고, 총 ginsenoside의 최적 추출조건을 알아보고자 능선분석을 이용하여 분석해 보았으며(Table 3), 총 ginsenoside의 반응표면 모형은 최대점 형태였으며, ethanol 농도 66.41%, 추출 온도 77.03°C로 추출 시 총 ginsenoside 함량이 17.24 mg/g으로 가장 높게 나타났으며, ethanol 농도 0.00%, 추출 온도 69.86°C로 추출 시 총 ginsenoside의 함량이 6.11 mg/g으로 가장 낮게 나타났다. 각각의 ginsenoside인 Rg1, Rb1, Rb2, Rb3의 반응표면의 모형은 모두 최대점 형태를 나타내었으며, ethanol 농도 68.00-78.69%에서 70.04-75.68°C의 범위에서 추출할 경우 ginsenosides 함량이 2.10-5.45 mg/g의 범위 내에서 모두 높게 나타났으며, ethanol 농도 0.00-1.06%에서 68.46-72.28°C로 추출 시 추출물의 ginsenosides 함량이 0.50-1.77 mg/g의 범위로 모두 낮게 나타났다.
Lee와 Do(2006)는 작은 입자의 홍삼박을 효소처리한 경우 홍삼박의 산성다당체 수율이 증가하였으나 1회 추출에서 대부분 추출된다고 하였다. 본 연구에서는 태극삼 산성다당체의 추출 특성을 조사하고자 ethanol 농도와 추출 온도의 변화에 따른 산성다당체 함량을 측정해 보았다.
추출조건의 변화에 따른 태극삼의 산성다당체 함량은 13.93-19.10 mg/g으로 측정되었다(Table 1). 이것을 회귀분석해 보았으며, 태극삼의 모델식 R2은 0.8929(p<0.05)에서 통계적으로 유의하였다(Table 2).
조건변수들의 영향을 알아보고자 태극삼 산성다당체의 F값을 구해보았으며(Table 2), ethanol 농도의 F값이 4.76(p<0.05)으로 ethanol 농도가 산성다당체의 추출에 어느 정도 영향을 미쳤으며, 추출 온도의 F값이 6.39(p<0.05)로 산성다당체의 수율에 ethanol의 농도보다 다소 높게 영향을 미치고 있었다. 이것은 ginsenosides의 추출에서와는 상반되는 결과로서, ginsenosides가 ethanol 용해성이 아주 높고 물에는 용해성이 극히 낮은 반면, 증숙과정을 거쳐 저분자화된 태극삼 산성다당체는 상대적으로 고온의 에탄올 용액에 대한 용해성이 다소 있으며 열수에도 잘 용해되기 때문으로 여겨진다.
그리고, 산성다당체의 최적 추출조건을 알아보고자 능선분석을 실시하였으며(Table 3), 산성다당체의 반응표면 모형은 최대점의 형태였으며, ethanol 농도 0.38%, 추출 온도 71.37°C로 추출 시 산성다당체의 함량이 19.03 mg/g으로 가장 높았으나, ethanol 농도 52.42%, 추출 온도 60.49°C로 추출 시 산성다당체가 14.04 mg/g으로 가장 낮았다.
태극삼의 ethanol 용액 추출 시 산성다당체 반응표면은 ethanol 농도가 낮을수록 비례적으로 증가하였으며, 70°C까지는 추출 온도가 증가할수록 증가하였으나 70°C 이상에서는 추출 온도가 증가할수록 감소하는 경향을 나타내었다(Fig. 4).
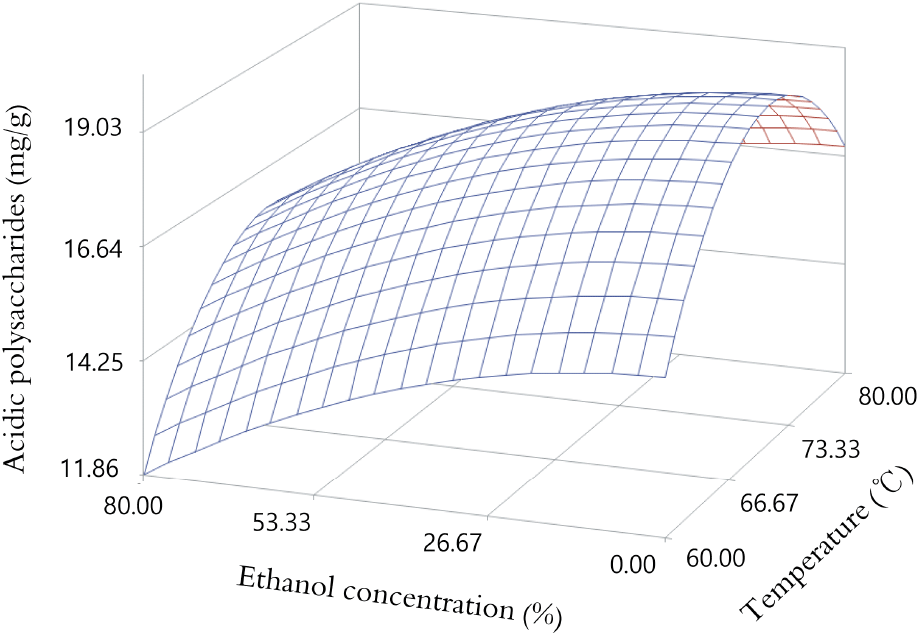
이러한 경향은 산성다당체가 추출 온도의 영향을 받아 추출 수율이 증가하지만, 홍삼에서와 유사하게 70°C 이상의 고온에서는 장시간 추출시에는 산성다당체가 저분자로 분해되어 상대적으로 그 함량이 낮아지는 것으로 여겨진다(Lee, 2023).
본 연구는 반응표면분석을 통하여 가용성 고형분, ginsenosides 및 산성다당체의 최적 추출 조건을 모니터링할 수 있었으며, 추출조건을 최적화 수 있었다. 그리고, 조건변수 중 ethanol 농도가 가용성 고형분, ginsenosides 및 산성다당체의 반응표면에 주로 영향을 미치고 있음을 확인할 수 있었다.
태극삼의 가용성 고형분과 산성다당체는 친수성 성분이 많으므로 ethanol 함량이 낮은 조건에서 수율이 높게 나왔지만, ginsenosides는 물보다 ethanol 용해성이 높아서 ethanol 농도가 높은 조건에서 잘 추출되었다.
따라서 ethanol 함량이 30-50%에서 추출하여 산성다당체와 ginsenosides의 추출 수율을 동시에 높일 수 있는 조건을 설정하거나, ethanol 함량이 높은 용액에서 1차 추출한 후 물로 2차 추출하는 방법을 적용해 볼 수 있다. 그러나 태극삼을 1회만으로 추출할 경우에는 ginsenoside 함량을 높일 것인지, 아니면 산성다당체와 고형분의 수율을 높일 것인지를 먼저 설정한 후 추출용매의 ethanol 농도를 적절하게 조절하여 가장 적합한 추출조건을 설정할 필요가 있다.
4. 요약
본 연구는 반응표면분석을 통해 태극삼의 기능성 성분 추출을 극대화하고자 ethanol 추출조건을 모니터링하여 최적 추출조건을 조사하였다. 태극삼의 가용성 고형분, 총 ginsenoside 및 산성다당체 모델식의 R2은 0.8894-0.9354(p<0.05)였다. 추출조건에 따른 태극삼의 가용성 고형분과 산성다당체는 ethanol 함량이 낮은 조건에서 수율이 높게 나왔으나, ginsenosides는 ethanol 농도가 높은 조건에서 잘 추출되었다. 가용성 고형분의 최적 추출조건은 ethanol 농도 0.22%, 추출 온도 68.96°C였으며, 최대 추출 수율은 57.81%였다. 총 ginsenoside의 최대 추출 수율은 태극삼을 ethanol 농도 66.41%에서 77.03°C로 추출하였을 때 17.24 mg/g이었다. Ginsenoside Rg1, Rb1, Rb2 및 Rb3에 대한 최적 추출조건은 ethanol 농도 68.00-78.69%, 추출 온도 70.04-75.68°C 범위로 나타났으며, 이때 각각의 ginsenoside 함량은 2.10-5.45 mg/g의 범위 내로 모두 높게 나타났다. 그리고 산성다당체의 최대 추출 수율은 ethanol 농도 0.38%에서 71.37°C로 추출하였을 때 19.03 mg/g이었다. 태극삼 기능성 성분의 추출 수율은 30-50% ethanol로 추출할 경우 산성다당체와 ginsenosides의 수율을 동시에 높일 수 있다.










