Article
자색케일(Brassica oleracea L. var. acephala) 안토시아닌 색소의 안정성에 영향을 미치는 요인
김미리1
,
김명현1,
한영실1,*
Factors affecting stability of anthocyanin pigment extracted from red kale (Brassica oleracea L. var. acephala)
Mi Ri Kim1
,
Myung Hyun Kim1,
Young Sil Han1,*
Author Information & Copyright ▼
1Department of Food and Nutrition, Sookmyung Women’s University, Seoul 04310, Korea
*Corresponding author. E-mail:
ygkmh5@nate.com, Phone:+82-2-710-9471, Fax:+82-2-710-9474
Copyright © The Korean Society of Food Preservation. This is an Open-Access article distributed under the terms of the
Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/4.0/) which permits
unrestricted non-commercial use, distribution, and reproduction in any
medium, provided the original work is properly cited.
Received: Apr 20, 2021; Revised: Aug 19, 2021; Accepted: Aug 30, 2021
Published Online: Oct 30, 2021
요약
본 연구는 처리조건에 따른 자색케일 안토시아닌의 색소 안정성을 조사하였다. 자색케일 용액은 pH 1.0에서 가장 안정적이었으며, 높은 흡광도 값을 보였다. 0.05 M의 유기산을 첨가한 자색케일 용액을 10일간 저장 시 malic acid, formic acid, acetic acid, citric acid 순으로 높은 색소잔존율을 보였다. 저장 기간별 금속이온에 대한 안정성을 측정한 결과, K+, Mg2+, Ca2+, Na+, Fe2+ 순으로 높은 색소 잔존율을 보였다. 열처리에 따른 안정성을 측정한 결과, 온도가 낮을수록 색소가 안정적임을 확인하였다. 0.1 M의 당을 첨가한 자색케일 용액을 6일간 저장 시 glucose, maltose, sucrose, galactose, fructose 순으로 높은 색소 잔존율을 보였다. 빛과 암소 조건에서 색소 안정성을 측정한 결과, 일광에 노출하였을 때보다 암소 조건에서 색소가 안정적임을 확인하였다. 저장온도에 따른 색소 안정성을 측정한 결과, −40°C, −20°C에서 비교적 안정적이었으나, 37°C에서는 저장기간에 따라 색소가 감소하는 경향을 보였다. 본 연구에 의하면 자색케일의 안토시아닌 색소는 처리조건에 따라 색소 안정성의 차이를 보이므로, 천연색소로 활용할 경우 색소 안정성에 유의할 필요가 있다고 생각된다.
Abstract
This study examined the pigment stability of red kale anthocyanin according to different conditions. The red kale extract was the most stable at pH 1.0 showing high absorbance at 538 nm. When a 0.05 M organic acid solution was added to the red kale extract, which was then stored for 10 days, the pigment retention rates were observed in the order of malic > formic > acetic > citric acids. When measuring the stability in the presence of metal ions, the pigment retention rates were observed in the order of K+ > Mg2+ > Ca2+ > Na+ > Fe2+. The stability based on heat treatment was confirmed that the lower the temperature, the more stable the color. When 0.1 M sugar solution was added to the red kale extract, which was then stored for 6 days, the pigment retention rates were observed in the order of glucose > maltose > sucrose > galactose > fructose. The color was more stable in darkness than upon exposure to sunlight. The color was relatively stable at −40°C and −20°C, but at 37°C, color stability decreased. In conclusion, the anthocyanin pigment of red kale showed different color stability depending on the processing conditions, and these should be considered when using it as a natural pigment.
Keywords: red kale; anthocyanin; pigment; color stability
서 론
식품의 색은 식품마다 고유한 빛깔을 나타내어 관능적인 품질과 기능성을 나타내는 중요한 역할을 한다. 이러한 식품의 색은 가공 방법이나 저장환경에 따라 변색되어 품질 저하가 일어나기도 하는데, 특히 천연 색소는 장기간 저장 시 화학 구조적 특성에 의해 변색이 되어 안정성이 낮아진다(Rhim과 Kim, 1999). 이를 방지하기 위하여 합성 색소를 첨가하여 식품의 색과 품질 등을 향상시켰으나, 발암성 등 인체 위험성에 관한 문제가 대두되면서 천연색소에 관한 연구가 매우 활발해지고 있다(Lee 등, 1996).
천연색소인 안토시아닌은 식물계에 광범위하게 존재하는 적색 색소로 붉은색, 분홍색, 자주색 등을 띠며, 과실류나 채소류 등에 많이 함유되어 있다. 안토시아닌은 cyanidin계의 색을 지닌 chrysanthemin으로 물에 쉽게 용해되므로 식품에 사용하기 비교적 용이하나, 구조적으로 불안정한 oxonium 화합물이므로 가공할 시 색소가 변색 또는 퇴색되어 품질 저하의 원인이 될 수 있다(Chung 등, 2004; Hong 등, 2002). 안토시아닌은 식품 소재에 따라 구조와 종류가 달라져 색소마다 고유한 특성을 보이게 되는데, 안토시아닌의 특성과 안정성을 알아본 선행연구로는 오디(Kang 등, 2003), 장미 꽃잎(Yang과 Cho, 2006), 매자나무(Laleh 등, 2006), 히비스커스(Mourtzinos 등, 2008), 아로니아(Hwang과 Ki, 2013), 양하(Kim과 Han, 2016), 적양배추(Ratanapoompinyo 등, 2017), 아마란스(Lee 등, 2017) 등이 있다.
일반적으로 케일은 남유럽 지중해 주변이 원산지로 수천 년 동안 아메리카와 유럽의 온화한 기후에서 재배되었다(Ahluwalia 등, 1979). 케일은 십자화과 채소로써, 페놀성 화합물, 섬유소, 플라보노이드, 비타민 C 등이 함유되어 있으며 항돌연변이, 항암효과가 있다고 보고되었다(Kim 등, 2014). 특히 폐암 발병률을 감소시키는 sulforaphane이 함유되어 있으며, 항암 물질로 잘 알려진 glucosinolates를 다량 함유하고 있다(Forman 등, 1999; Schmidt 등, 2010). 케일 종류 중 안토시아닌에 의해 붉은색, 보라색을 띠는 자색케일은 주로 유럽 지역에서 많이 재배되며, 가장 많이 존재하는 종은 ‘Redbor F1 hybrid’이다(Olsen 등, 2010). 최근 전라남도 해남군에서도 자색케일이 대규모로 생산되기 시작하였다. Olsen 등(2010)에 따르면 자색케일에는 기존 십자화과 속에 함유된 10개의 페놀 화합물을 포함하여 47개 구조의 페놀 화합물이 발견되었으며, 다양한 hydroxycinnamates와 한 개의 hydroxybenzoate가 발견되었다. 또한, flavonoids 중 caffeic, p-coumaric, ferulic, hydroxyferulic, sinapic acid가 flavonoid glucoside molecule에 연결되어 있으며, kaempferol, quercetin, cyanidin이 자색케일에 있는 aglycone으로 발견되었다. 자색케일의 안토시아닌은 12개의 구조가 발견되었는데, 그 중 cyanidin-3-sinapoyl-feruloyl-diglucoside-5-glucoside 성분의 함량이 가장 높았다.
천연색소인 안토시아닌을 이용하기 위해서는 색소에 영향을 주는 요인과 저장에 따른 안정성을 규명하는 것이 색소 활용성 면에서 매우 중요하다. 따라서 본 연구에서는 pH, 유기산, 금속이온, 열, 당, 빛, 저장온도, 저장기간 처리에 따른 안토시아닌 색소 안정성을 비교 분석하여 자색케일에 관한 기초자료를 제공하고자 한다.
재료 및 방법
실험재료
본 연구에서 사용된 자색케일은 전라남도 해남군에서 2021년도 1월에 수확한 것으로, 무게 80-100 g, 길이 50-70 cm의 자색케일을 구매하여 사용하였다. 구매한 자색케일은 세척 후 줄기를 제거하고 잎만 분리하여 착즙기(HH-SBF11, Hurom Co., Ltd., Gimhae, Korea)로 즙을 내었고, 4°C에서 보관하며 사용하였다. 자색케일 즙은 1,008 ×g, 4°C에서 10분간 원심분리(Combi 514R, Hanil Science Industrial Co., Ltd., Gimpo, Korea)하고, 상등액만 취하여 Whatman No. 2에 여과하였다. 여과된 자색케일 즙은 4°C에서 보관하며 실험에 사용하였으며, 여과액을 각각의 cap test tube에 넣고 실험에 맞게 완충용액으로 희석하여 3회 반복 실험하였다.
자색케일 추출액 제조
자색케일 착즙액에 Clark-Lubs 완충용액(0.2 M KCl + 0.2 M HCl) 또는 Macllvain 완충용액(0.1 M citric acid + 0.2 M Na2HPO4)을 섞어 일정 농도로 희석한 뒤 추출액을 제조하여 실험에 사용하였다. 완충용액의 제조 및 분석용 시약은 Sigma-Aldrich Chemical Co. (St. Louis, Mo, USA)로부터 구매하여 사용하였으며, 그밖에 모든 시약은 특급시약을 사용하였다.
pH의 영향
pH에 따른 자색케일 색소 안정성을 측정하기 위하여 모든 추출액은 1% 농도로 제조되었다. 자색케일 착즙액에 Clark-Lubs 완충용액을 첨가하여 pH 1.0-2.0으로 조정하였고, Macllvain 완충용액을 첨가하여 pH 3.0-7.0으로 조정하였다. 조정한 pH 추출액은 400-600 nm의 파장범위에서 spectrophotometer(T60UV, PG Instruments, Wibtoft, England)로 측정하여 최대 흡수 파장을 측정하였다.
유기산의 영향
유기산의 종류에 따른 자색케일 색소 안정성을 측정하기 위하여 citric acid, acetic acid, formic acid, malic acid에 pH 2.0의 Clark-Lubs 완충용액을 첨가하여 0.01 M, 0.05 M, 0.1 M 농도로 용해한 후, 착즙액에 첨가하여 1% 농도의 추출액을 제조하였다. 유기산을 농도별로 첨가한 추출액의 흡광도는 538 nm에서 측정하였으며, 색소의 강도가 비교적 높았던 0.05 M 농도에서 저장 기간에 따른 색소 안정성을 측정하였다. 유기산을 첨가한 추출액을 cap test tube에 넣고 10일 동안 4°C에 보관하였고, 2일 간격으로 시료를 취하여 538 nm의 흡광도에서 변화를 측정하였다.
금속이온의 영향
금속이온의 종류에 따른 자색케일 색소 안정성을 측정하기 위하여 Fe2+(FeSO4), Na+(Na2SO4), K+(K2SO4), Ca2+(CaCl2), Mg2+(MgSO4)에 pH 2.0의 Clark-Lubs 완충용액을 첨가한 후, 착즙액에 첨가하여 1% 농도의 추출액을 제조하였다. 금속염을 첨가한 추출액을 cap test tube에 넣고 10일 동안 60°C에 보관하였으며, 2일 간격으로 시료를 취하여 538 nm의 흡광도에서 변화를 측정하였다.
열에 의한 영향
열에 따른 자색케일 색소 안정성을 측정하기 위하여 pH 2.0의 Clark-Lubs 완충용액을 착즙액에 첨가하여 1% 농도의 추출액을 제조하였다. 추출액을 cap test tube에 넣고 30°C, 60°C, 100°C의 항온수조(BF-355B, Bio free, Seoul, Korea)에서 10시간 동안 보관하였고, 2시간 간격으로 538 nm의 흡광도에서 변화를 측정하였다.
당에 의한 영향
당류의 종류에 따른 자색케일 색소 안정성을 측정하기 위하여 glucose, fructose, maltose, sucrose, galactose에 pH 2.0의 Clark-Lubs 완충용액을 첨가하여 0.1 M, 0.5 M, 1 M 농도로 용해한 후, 착즙액에 첨가하여 1% 농도의 추출액을 제조하였다. 당류를 농도별로 첨가한 추출액의 흡광도는 538 nm에서 측정하였으며, 색소의 강도가 가장 높았던 0.1 M 농도에서 저장 기간에 따른 색소 안정성을 측정하였다. 당을 첨가한 추출액을 cap test tube에 넣고 6일 동안 60°C에 보관하였고, 2일 간격으로 시료를 취하여 538 nm의 흡광도에서 변화를 측정하였다.
빛에 의한 영향
빛의 유무에 따른 자색케일 색소 안정성을 측정하기 위하여 pH 2.0의 Clark-Lubs 완충용액을 착즙액에 첨가하여 1% 농도의 추출액을 제조하였다. 추출액은 투명 유리병과 암소병에 각각 담아 약 25°C의 상온에서 일광 노출 또는 암소 처리 하였으며, 10일 동안 2일 간격으로 시료를 취하여 538 nm의 흡광도에서 변화를 측정하였다.
저장온도 및 저장기간에 의한 영향
냉장 및 냉동온도에서 저장에 따른 자색케일 색소 안정성을 측정하기 위하여 pH 2.0의 Clark-Lubs 완충용액을 착즙액에 첨가하여 1% 농도의 추출액을 제조하였다. 추출액을 cap test tube에 넣고, −40°C, −20°C, 4°C, 37°C에서 60일 동안 보관하였으며, 10일 간격으로 538 nm의 흡광도에서 변화를 측정하였다.
통계처리
실험 결과의 통계처리는 SPSS package(Statistical Analysis Program, version 25, IBM Co., Armonk, NY, USA)를 이용하였으며, 각 실험은 3회 반복하여 평균과 표준편차로 나타내었다. 유의성 검증을 위해 각 실험군 간 ANOVA를 이용했으며, 사후검증으로 Duncan’s multiple range test를 실시하였다(p<0.05).
결과 및 고찰
pH의 영향
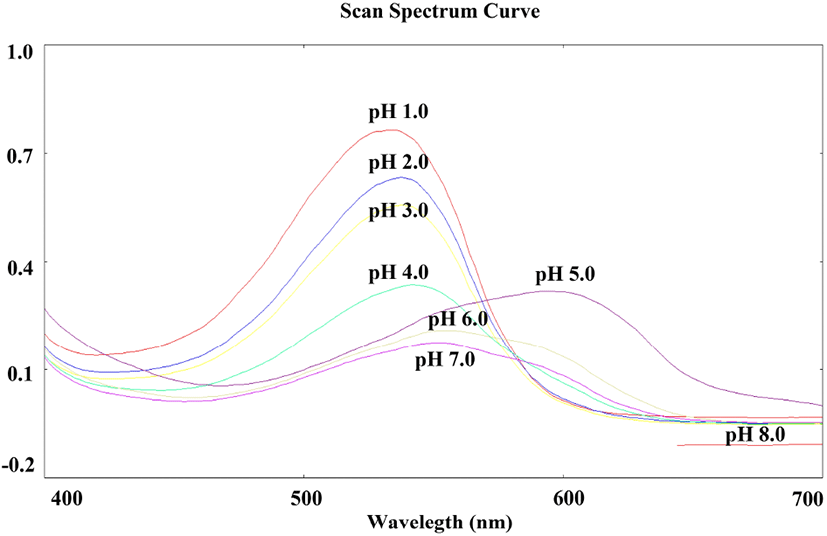
자색케일 안토시아닌 색소의 pH에 의한 변화는 Fig. 1에 나타내었다. 자색케일은 pH 1.0에서 가장 높은 흡수 스펙트럼을 보였으며, 특히 538 nm에서 가장 높은 흡광도를 보였다. 또한 자색케일 추출액의 분광학적인 spectrum 변화를 보았을 때, pH가 증가할수록 최대 흡수 파장이 장파장 쪽으로 변하는 bathochromic shift 현상을 나타내었다. 이는 안토시아닌 색소에서 발견되는 특징으로, pH 4.0 이상으로 증가 시 적색이 청색으로 변하면서 최대 흡수 파장이 급격하게 증가하기 때문이다(Rhim과 Kim, 1999). 일반적으로 안토시아닌 색소는 pH 1.0-3.0에서 적색 또는 연한 자주색이며, pH 7.0-8.0에서는 무색, pH 9.0 이상에서는 청색을 나타낸다(Jackman 등, 1987). 이는 안토시아닌이 pH가 낮은 산성 용액일 때 적색의 flavylium 양이온으로 존재해 안정적인 진한 적색을 나타내고, 중성에서는 flavylium이 수소이온을 잃어 carbinol pseudobase를 형성하여 무색이 되기 때문이다. 또한 pH 9.0 이상에서는 anhydrobase 형태가 되어 푸른색을 형성한다고 보고되었다(Bassa과 Francis, 1987).
유기산의 영향
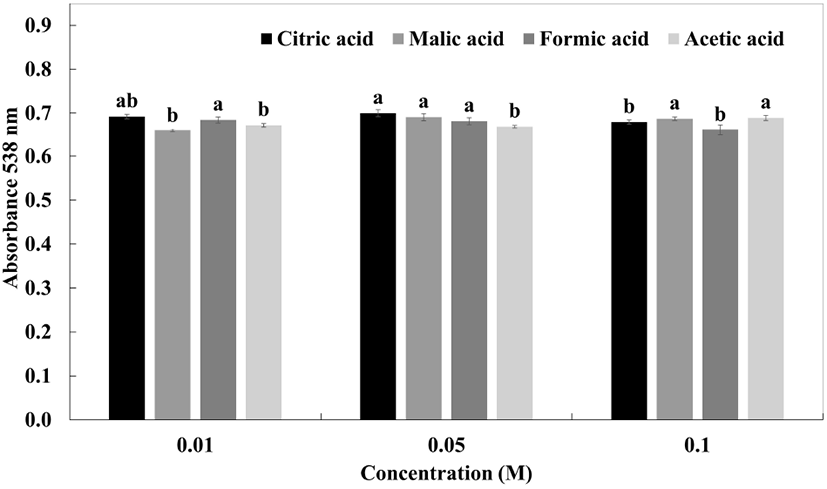
자색케일 안토시아닌 색소의 유기산 농도에 의한 변화는 Fig. 2에 나타내었다. 유기산은 식품을 가공할 시 저장성을 연장하기 위해 사용되기도 하므로 이에 따른 영향을 알아보는 것이 중요하다(Kang 등, 2003). 유기산을 농도별로 첨가하여 안토시아닌 색소의 변화를 측정한 결과, 농도 간의 유의적인 차이는 없었다. 아로니아의 색소 안정성(Hwang과 Ki, 2013) 실험 결과에 따르면 0.01 M, 0.05 M, 0.1 M의 농도 중 0.05 M에서 가장 안정적이었으며, 0.01 M에서는 유기산 간의 차이가 미미하였다고 보고되었다.
Fig. 2.
Effect of organic acid on the color stability of red kale extract at different concentration.
Results are presented as the mean±SD (n=3). Means with different letters (a-b) on the bar are significantly different by Duncan’s multiple range test at p<0.05.
Download Original Figure
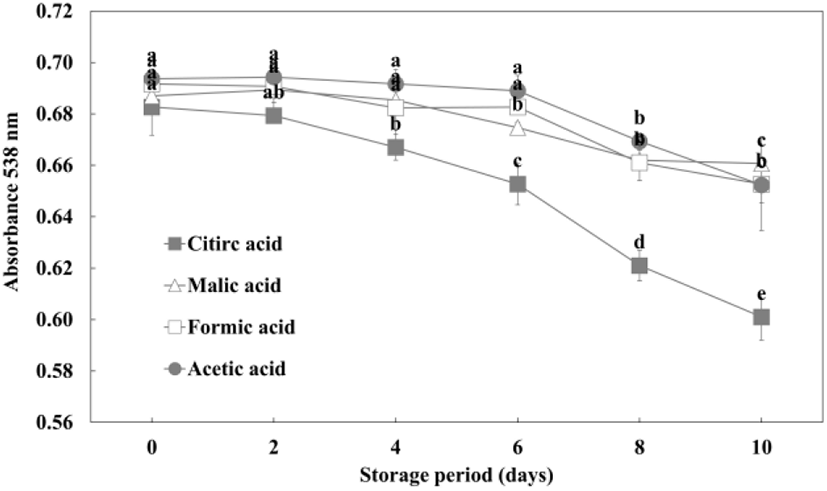
비교적 색소의 강도가 높았던 0.05 M의 유기산을 첨가한 자색케일 안토시아닌 색소의 저장 기간별 변화는 Fig. 3에 나타내었다. 유기산 첨가 10일 경과 시 malic acid, formic acid, acetic acid, citric acid 순으로 높은 색소 잔존율을 보였다. 유기산을 첨가하였을 때 전반적으로 90% 이상의 잔존율을 보여 높은 안정성을 보였으나, 그중 citric acid를 첨가할 시 88%의 낮은 색소 잔존율을 보였다. Kang 등(2003)의 연구결과, 오디 추출물에 citric acid 첨가 시 색소 잔존율이 가장 낮아 본 실험 결과와 일치하였으며, Alcazar-Alay 등(2017)에 따르면 아사이베리 과육 추출물에 citric acid를 첨가 시 다른 화합물들의 방출을 증가시켜 추출물의 순도를 낮추고, 안토시아닌 수율을 감소시키는 역효과를 보였다고 보고되었다. Pacheco-palencia 등(2007)의 연구에서도 citric acid는 안토시아닌의 색을 유지하는 데 부정적인 영향을 미치며, 화합물 분해를 촉진시킨다고 하여 본 연구와 유사한 결과를 보였다. 따라서 자색케일의 안토시아닌 색소를 장기간 저장 및 가공 시 citric acid 첨가에 유의할 필요성이 있다고 판단된다.
Fig. 3.
Effect of 0.05 M organic acid on the color stability of red kale extract during storage.
Results are presented as the mean±SD (n=3). Means with different letters (a-e) are significantly different by Duncan’s multiple range test at p<0.05.
Download Original Figure
금속이온의 영향
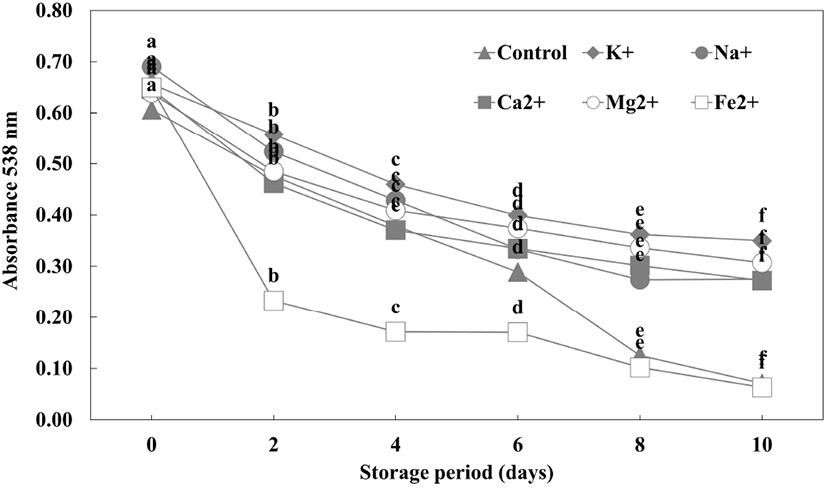
자색케일 안토시아닌 색소의 금속이온에 의한 변화는 Fig. 4에 나타내었다. 안토시아닌은 각종 금속이온과 반응성이 크기 때문에 착화합물을 형성하여 변색을 초래한다(Yang과 Cho, 2006). 따라서 안토시아닌 색소를 함유하는 식품을 금속 용기에 저장하거나 금속으로 가공할 시 변색을 초래할 수 있어 유의해야 한다(Song과 Jo, 1997).
Fig. 4.
Effect of metal ion on the color stability of red kale extract during storage.
Results are presented as the mean±SD (n=3). Means with different letters (a-f) are significantly different by Duncan's multiple range test at p<0.05.
Download Original Figure
저장 기간에 따른 자색케일의 색소 안정성을 측정한 결과, K+, Mg2+, Ca2+, Na+, Fe2+ 순으로 높은 색소 잔존율을 보였다. Fe2+을 첨가 시 10일 후 색소 잔존율이 9%로 가장 안정성이 떨어졌으며, K+을 첨가 시 색소 잔존율이 53%로 색소 잔존율이 가장 높았다. Kim과 Han(2016)에 따르면 양하 추출물에 Fe2+을 첨가 시 다른 금속이온에 비해 색소의 잔존율이 가장 낮았으며, Ca2+, K+을 첨가 시 색소 잔존율이 비교적 높아 본 연구의 결과와 유사한 경향을 보였다. 또한 적양배추의 안토시아닌에 금속이온을 첨가한 결과, Sn2+을 첨가할 시 대조군에 비해 2배 감소된 안토시아닌 함량을 보였으며, Ca2+, Fe3+을 첨가 시 낮은 안정성을 보인 반면 Al3+을 첨가 시 안정성이 높아졌다(Ratanapoompinyo 등, 2017). 자색옥수수의 안토시아닌에 금속이온을 첨가할 시 Ca2+, Al3+, K+, Cu2+에서는 큰 변화가 없었고, Mn2+에서는 긍정적인 영향을 보였으나, Fe3+, Mg2+, Zn2+을 첨가 시 색소 안정성이 감소하였다(Mei 등, 2014).
이처럼 안토시아닌의 색소 잔존율이 차이가 나는 이유는 안토시아닌 색소의 metal complex 구조간 반응속도, 평형상수 및 평형에 도달하는 시간 등이 달라져 metal complex 형성반응에 영향을 주기 때문이라고 보고되었다(Kim과 Ahn, 1978). 따라서 금속이온 첨가 시 색소 안정성은 안토시아닌의 종류와 화학적 구조에 영향을 받는 것으로 보인다(Kim과 Han, 2016). 이처럼 자색케일의 안토시아닌 색소를 장기간 저장 및 가공 시 금속이온의 종류에 따른 안정성에 주의해야 하며, 특히 Fe2+ 첨가에 유의할 필요성이 있다고 판단된다.
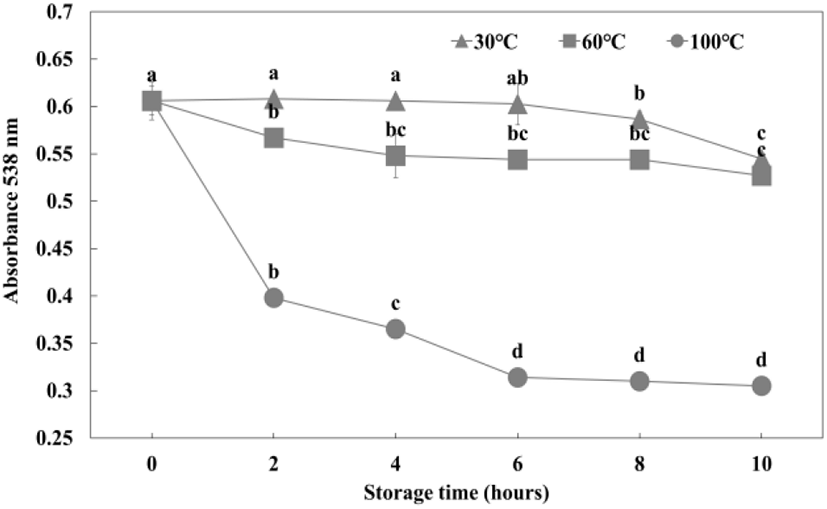
열에 의한 영향
자색케일 안토시아닌 색소의 열에 의한 변화는 Fig. 5에 나타내었다. 본 실험 결과, 저장온도가 높아질수록 색소 잔존율이 급격하게 낮아졌다. 자색케일 안토시아닌 추출액을 10시간 동안 30°C 저장 시 색소 잔존율은 89%로 비교적 안정하였으나, 60°C 저장 시 86%, 100°C에서는 50%의 낮은 잔존율을 보였다. 이는 안토시아닌 색소를 함유한 장미 꽃잎(Yang과 Cho, 2006), 아로니아(Hwang과 Ki, 2013), 양하(Kim과 Han, 2016)의 색소 잔존율 결과와 일치하였다. 안토시아닌은 온도에 민감하여 40°C 이상에서 색소파괴가 일어나며, glycoside 결합의 가수분해가 일어나 α-diketone, chalcone 등이 형성되어 갈색 물질을 만든다고 보고되었다(Adams, 1972; Roobha 등, 2011). 따라서 자색케일을 장기간 저장 및 가공 시 높은 온도의 열에 노출되지 않도록 유의할 필요성이 있다고 판단된다.
Fig. 5.
Effect of temperature on the color stability of red kale extract at different heating time.
Results are presented as the mean±SD (n=3). Means with different letters (a-d) are significantly different by Duncan’s multiple range test at p<0.05.
Download Original Figure
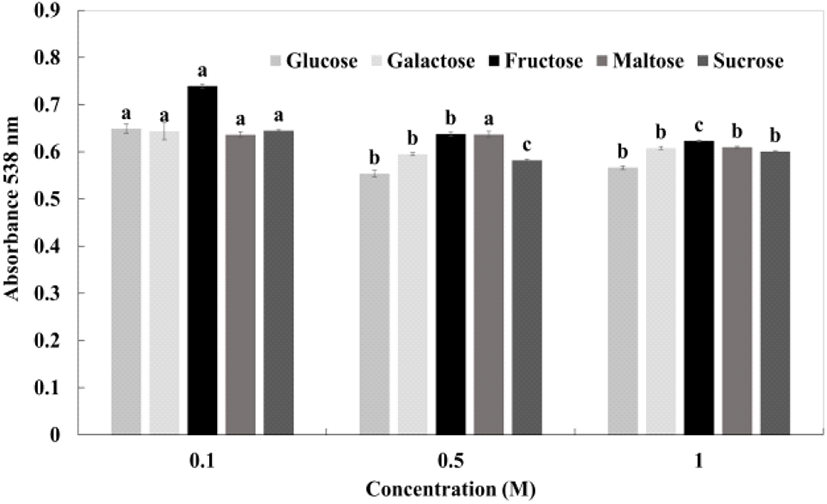
당에 의한 영향
자색케일 안토시아닌 색소의 당 농도에 의한 변화는 Fig. 6에 나타내었다. 당을 농도별로 첨가하여 안토시아닌 색소의 변화를 측정한 결과, 0.1 M에서 가장 높은 흡광도 값을 보여 색소 안정성이 가장 높음을 알 수 있었다. 이는 자색고구마(Lee 등, 1996), 자색감자(Rhim과 Kim, 1999), 오디(Kang 등, 2003), 장미 꽃잎(Yang과 Cho, 2006), 아로니아(Hwang과 Ki, 2013), 양하(Kim과 Han, 2016)의 당에 의한 색소 안정성 실험 결과와 유사한 경향을 보였다. 따라서 당을 첨가하는 농도가 높아질수록 자색케일 안토시아닌의 색소 안정성이 감소함을 확인할 수 있었다.
Fig. 6.
Effect of sugar on the color stability of red kale extract at different concentration.
Results are presented as the mean±SD (n=3). Means with different letters (a-c) on the bar are significantly different by Duncan’s multiple range test at p<0.05.
Download Original Figure
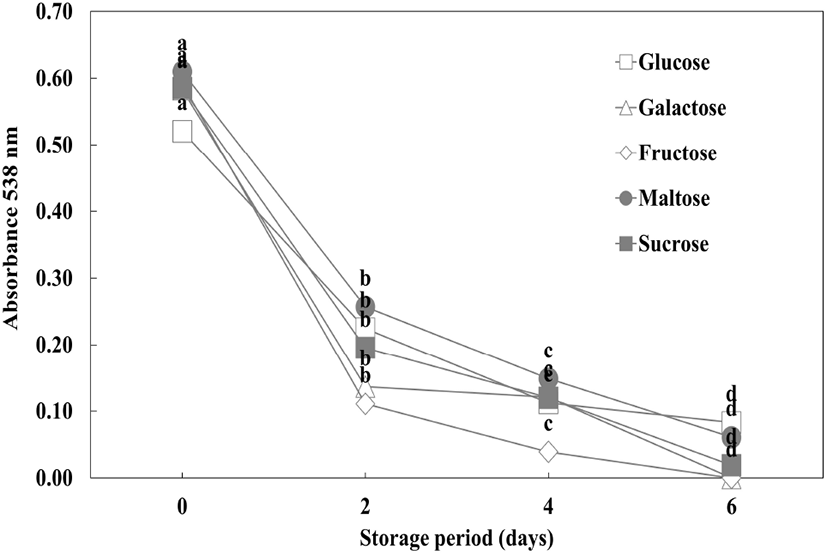
0.1 M의 당을 첨가한 자색케일 안토시아닌 색소의 저장 기간별 변화는 Fig. 7에 나타내었다. 당 첨가 6일 경과 시 glucose, maltose, sucrose, galactose, fructose 순으로 높은 색소 잔존율을 보였다. 저장 2일 경과 시 모든 당 첨가군에서 색소 잔존율이 50% 미만이었으며, 특히 fructose 첨가 시 잔존율이 18%로 색소 파괴가 매우 빠르게 나타났다. 저장 6일차 경과 시 galactose, fructose의 색소 잔존율이 (-) 값을 보여 자색케일 안토시아닌에 당을 첨가할 시 색소 안정성이 매우 떨어지는 것을 알 수 있었다. Yoon 등(1997)에 따르면 유색미의 안토시아닌에 당을 첨가할 시 fructose에서 매우 낮은 색소 잔존율을 보여 본 연구와 같은 경향을 보였다. 하지만 Hwang과 Ki(2013)에 따르면 아로니아 추출물에 당을 첨가 시 fructose에서 색소 안정성이 가장 높았고, maltose 첨가 시 색소 안정성이 가장 낮아, 본 연구와 상반된 결과를 보였다. 이는 식물체마다 안토시아닌 구조에 연결된 당의 종류가 다르기 때문으로 생각된다(Lee 등, 1996).
Fig. 7.
Effect of 0.01 M sugar on the color stability of red kale extract during storage.
Results are presented as the mean±SD (n=3). Means with different letters (a-d) are significantly different by Duncan’s multiple range test at p<0.05.
Download Original Figure
당 첨가 시 안토시아닌 색소의 잔존율이 감소하는 것은 당이 첨가되었을 때 glycosidic hydrolysis, ring opening, brown reaction 등의 화학작용이 일어나 색소가 분해되기 때문이라고 보고되었다(Yang 등, 1982). 따라서 자색케일의 안토시아닌 색소를 장기간 저장 및 가공 시 당류의 첨가에 유의할 필요성이 있다고 판단된다.
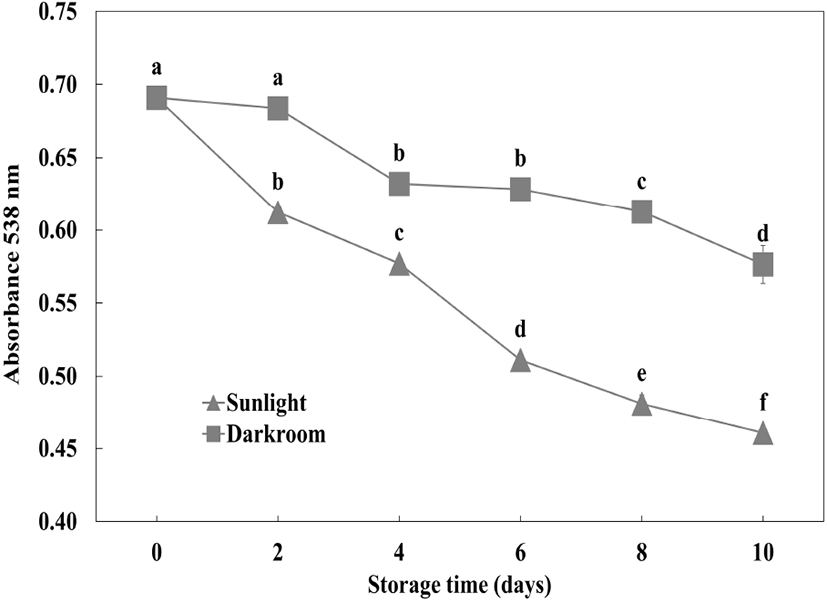
빛에 의한 영향
자색케일 안토시아닌 색소의 빛에 의한 변화는 Fig. 8에 나타내었다. 10일 동안 빛과 암소 조건에서 저장한 결과, 빛 조건에서의 색소 잔존율은 66%였으며, 암소 조건에서의 잔존율은 83%였다. Hong 등(2002)에 따르면 거봉포도 과피의 안토시아닌 색소는 일광에서 잔존율이 급격히 감소하였으나, 암소에서는 색소 감소율이 미비하다고 보고되어 본 연구와 유사한 경향을 보였다.
Fig. 8.
Effect of light on the color stability of red kale extract during storage.
Results are presented as the mean±SD (n=3). Means with different letters (a-f) are significantly different by Duncan’s multiple range test at p<0.05.
Download Original Figure
Mei 등(2014)에 따르면 자색옥수수의 안토시아닌 색소를 암소 보관 시 5일 차에 변화가 거의 없었으나, 일광 조건에서는 감소하는 경향을 보였다. 이후에는 색소 잔존율이 빠르게 감소되어 장기간 저장 시에는 빛을 피해야 한다고 보고되었다. 이처럼 자색케일의 안토시아닌 색소는 빛에서 안정성이 낮고 암소에서는 비교적 안정적이므로, 장기간 저장 시 빛을 차단하는 포장재 또는 암소 저장 환경이 필요할 것으로 판단된다.
저장온도 및 저장기간에 의한 영향
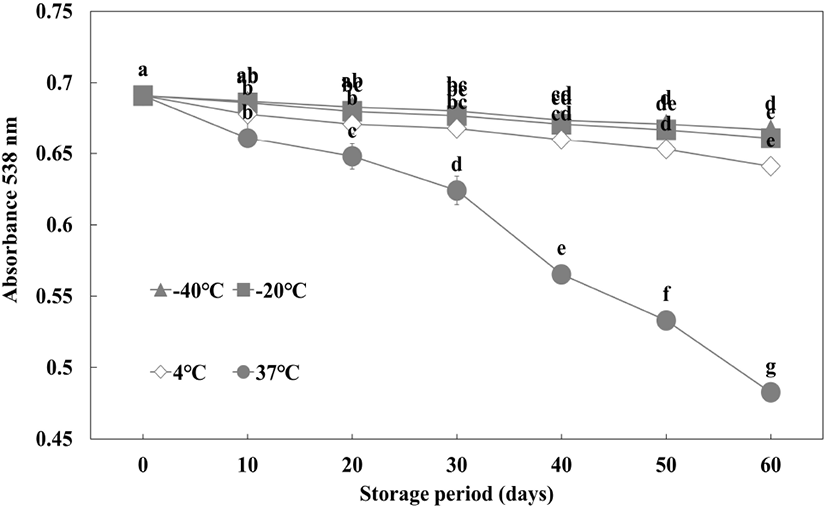
자색케일 안토시아닌 색소의 저장온도, 저장기간에 의한 변화는 Fig. 9에 나타내었다. 저장 기간과 저장온도에 따른 색소 안정성을 측정한 결과, 37°C, 4°C, −20°C, −40°C 순으로 낮은 색소 잔존율을 보여 온도가 높아질수록 색소 안정성이 감소함을 확인하였다. 60일 경과 시 −40°C에서는 97%, −20°C에서는 96%, 냉장 온도인 4°C에서는 93%, 37°C에서는 70%의 잔존율을 보였다. 아로니아 추출액의 경우, −75°C에서 색소 안정성이 가장 높았으며, 4°C에서 색소 파괴가 급격하게 나타났다(Hwang과 Ki, 2013). Kim과 Han(2016)에 따르면 양하 추출액을 60일 동안 저장했을 때 −70°C에서는 73%의 색소 잔존율을 보였으나, 4°C에서는 69%의 낮은 잔존율을 보여 본 연구와 유사한 결과를 보였다. 또한 매자나무 열매를 84일 동안 온도를 달리하여 저장한 결과, 5°C에서는 41%의 안토시아닌이 감소하였고, 35°C에서는 89%가 감소하였다. 이처럼 온도가 증가할수록 색소파괴가 빨라지는 이유는 3-glycoside 구조의 가수분해에 의한 것이라고 보고되었다(Laleh 등, 2006). 따라서 자색케일을 장기간 저장 및 가공 시 낮은 온도에서 냉동 또는 냉장 저장하는 것이 색소 안정성을 높이는 데 도움이 될 것으로 판단된다.
Fig. 9.
Effect of storage temperature on the color stability of red kale extract during storage.
Results are presented as the mean±SD (n=3). Means with different letters (a-g) are significantly different by Duncan’s multiple range test at p<0.05.
Download Original Figure
감사의 글
본 논문은 교육부 및 한국연구재단의 4단계 두뇌한국21 사업(4단계 BK21 사업)으로 지원된 연구입니다.
References
Adams CHM, Mackenzie K, Cawley DJ. Sequential wagner-meerwein rearrangements in the protolysis of monodechloroaldrin and monodechloroisodrin into a unique saturated ketone. Tetrahedron Lett, 13, 1311-1314 (1972)


Alcazar-Alay SC, Cardenas-Toro FP, Osorio-Tobon JF, Barbero GF, Alemeida Meireles MA. Obtaining anthocyanin-rich extracts from frozen acai (
Euterpe oleracea Mart.) pulp using pressurized liquid extraction. Food Sci Technol, 37, 48-54 (2017)


Bassa LA, Francis FJ. Stability of anthocyanins from sweet potatoes in a model beverage. J Food Sci, 52, 1753-1754 (1987)


Chung KW, Joo YH, Lee DJ. Content and color difference of anthocyanin by different storage periods in seed coats of black soybean (
Glycine max (L.) Merr.). Korean J Int Agric, 16, 196-199 (2004)

Forman MR, Zhang J, Gunter E, Yao SX, Gross M, Qiao YL, Graubard BI, Tayor PR, Keith S, Mather M. Season specific correlation between dietary intake of fruits and vegetables and levels of serum biomarkers among Chinese tin miners at high risk for lung cancer. Ann N Y Acad Sci, 889, 230-239 (1999)



Hong JH, Chung HS, U Hong, Youn KS. Storage stability of anthocyanin pigment isolated from a wasted grape peels. Korean J Food Preserv, 9, 327-331 (2002)

Hwang ES, Ki KN. Stability of the anthocyanin pigment extracted from aronia (
Aronia melancocarpa). Korean J Food Sci Technol, 45, 416-421 (2013)


Kang CS, Ma SJ, Cho WD, Kim MJ. Stability of anthocyanin pigment extracted from mulberry fruit. Korean J Soc Food Sci Nutr, 32, 960-964 (2003)


Kim HS, Ahn SY. Studies on the formation of anthocyanin metal complex. Appl Biol Chem, 21, 22-30 (1978)


Kim JD, Lee OH, Lee JS, Jung HY, Kim BK, Park KY. Safety effects against nitrite and nitrosamine as well as anti-mutagenic potentials of kale and
Angelica keiskei vegetable juices. Korean J Soc Food Sci Nutr, 43, 1207-1216 (2014)


Kim MH, Han YS. Stability study of the pigment extract from yangha (
Zingiber mioga Rosc). Korean J Food Cook Sci, 32, 325-332 (2016)


Laleh GH, Frydoonfar H, Heidary R, Jameei R, Zare S. The effect of light, temperature, pH and species on stability of anthocyanin pigments in four berberis species. Pak J Nutr, 5, 90-92 (2006)


Lee JH, Lee HB, Choi SI, Jung TD, Cho BY, Choi SH, Sim WS, Han XG, and Lee OH. Stability and antioxidant activities of anthocyanin from amaranth (
Amaranthus spp. L.) baby leaf extracts. Korean J Soc Food Sci Nutr, 46, 1550-1555 (2017)


Lee LS, Rhim JW, Kim SJ, Chung BC. Study on the stability of anthocyanin pigment extracted from purple sweet potato. Korean J Food Sci Technol, 28, 352-359 (1996)

Mei X, Qin H, Wang J, Wang G, Liu C, Cai Y. Studies on physicochemical characteristics of anthocyanin from super dark maize. J Food Nutr Res, 2, 109-114 (2014)


Mourtzinos I, Makris DP, Yannakopoulou K, Kalogeropoulos N, Michali I, Karathanos VT. Thermal stability of anthocyanin extract of
Hibiscus sabdariffa L. in the presence of beta-cyclodextrin. J Agric Food Chem, 56, 10303-10310 (2008)



Olsen H, Aaby K, Borge G. Characterization, quantification, and yearly variation of the naturally occurring polyphenols in a common red variety of curly kale (
Brassica oleracea L. convar.
acephala var.
sabellica cv. ‘Redbor’). J Agric Food Chem, 58, 11346-11354 (2010)



Pacheco-palencia LA, Hawken P, Talcott ST. Juice matrix composition and ascorbic acid fortification effects on the phytochemical, antioxidant and pigment stability of acai (
Euterpe oleracea Mart.). Food Chem, 105, 28-35 (2007)


Ratanapoompinyo J, Nguyen LT, Devkota L, Shrestha P. The effects of selected metal ions on the stability of red cabbage anthocyanins and total phenolic compounds subjected to encapsulation process. J Food Process Preserv, 41, 1-8 (2017)


Rhim JW, Kim SJ. Characterictics and stability of anthocyanin pigment extracted from purple-fleshed potato. Korean J Food Preserv, 31, 348-355 (1999)

Roobha JJ, Saravanakumar M, Aravindhan KM, Devi PS. The effect of light, temperature, pH on stability of anthocyanin pigments in
Musa acuminata bract. Res Plant Biol, 1, 5-12 (2011)

Schmidt S, Zietz M, Schreiner M, Rohn S, Kroh LW, Krumbein A. Genotypic and climatic influences on the concentration and composition of flavonoids in kale (
Brassica oleracea var.
sabellica). Food Chem, 119, 1293-1299 (2010)


Song JC, Jo WD. Processed food and food coloring. Bull Food Technol, 10, 62-67 (1997)

Ahluwalia KS, Roy SK, Chatterjee SS, Swarup V. Kale
Brassica oleracea var.
acaphala-a nutritionally rich vegetable [India]. Indian Horticulture, 24, 9-10 (1979)

Yang HC, Lee JM, Song KB. Anthocyanins in cultured
Schizandrae chinensis Baillon and its stability. J Korean Agric Chem Soc, 25, 35-43 (1982)

Yang MO, Cho EJ. Stability for rose petals pigment as a food material. J East Asian Soc Dietary Life, 16, 468-473 (2006)

Yoon JM, Cho MH, Hahn TR, Paik YS, Yoon HH. Physicochemical stability of anthocyanins from a Korean pigmented rice variety as natural food colorants. Korean J Food Sci Technol, 29, 211-217 (1997)