서 론
인체에 산소는 생명유지를 위한 에너지 생산과정에 중요한 작용을 하나, 자외선, 흡연, 매연, 약물 및 방사선 등의 여러 요인에 의하여 superoxide(O2−), nitric oxide(NO), nitrogen dioxide(NO2), hydroxyl(OH) 및 peroxynitrite(ONOO−) 등과 같은 활성산소종(reactive oxygen species)으로 변하며, 산화적 스트레스를 유발하게 된다(Halliwell과 Aruoma, 1991). 생체 내에는 활성산소종의 활동을 억제하는 superoxide dismutase, catalase, peroxidase 등의 항산화 효소 및 비타민 C, 비타민 D 및 glutathione 등과 같은 항산화 물질이 존재한다(Fang 등, 2002). 하지만 과도하게 생성된 산화적 스트레스는 세포의 구성성분인 지질, 당, 단백질 및 DNA를 비선택적, 비가역적 파괴를 촉진시켜 노화, 암, 뇌질환, 심혈관계질환 및 피부 질환 등의 각종 성인병을 유발한다(Lobo 등, 2010). 따라서 체내의 활성산소종 및 자유라디칼을 억제하고 조절하여 노화방지 및 성인병 예방 등의 기능을 하는 추가적인 성분이 필요하다(Hussain 등, 2003). 최근 butylated hydroxyanisol, butylated hydroxytoluene 및 tertiary butylhydroquinone 등과 같은 합성 항산화제가 개발되었으나, 이들 합성 항산화제들은 독성 및 발암성 등의 부작용이 발견되어 사용을 제한하고 있어(Williams 등, 1999) 보다 안정하고 부작용이 적은 천연 항산화제의 개발이 필요한 실정이다(Lee 등, 1998).
Purpurogallin은 benzotropolone 골격의 화합물로 Quercus 속의 오배자(nutgall)에 주요 성분으로 알려져 있으며(Abou- Karam과 Thomas, 1999), pyrogallol의 산화반응에 의해 생성되는 것으로 보고되어 있다(Critchlow 등, 1967). 이전 연구에서 purpurogallin은 tyrosine-specific protein kinase(Abou- Karam과 Thomas, 1999), xanthine oxidase(Honda 등, 2017) 및 glutathione S-transferase(Das 등, 1984) 등의 효소 저해활성이 보고가 되었으며, 항염증(Park 등, 2013), 항혈소판(Ku와 Bae, 2014), 항골다공증(Kim 등, 2018) 및 항균(Inamori 등, 1997) 등 다양한 기능성 활성을 나타내는 화합물로 알려져 있다. 최근 연구에서는 식도암(esophageal cancer) 관련 세포 및 동물실험에 우수한 항암 활성이 보고가 되었다(Xie 등, 2019).
감마선 조사는 식품에 직접적인 가열처리를 하지 않고 살균, 멸균 및 저장기간의 연장 등의 식품 품질을 향상시키는 기술로 세계적으로 많이 사용되고 있다(Farkas, 1998). 이전부터 감마선 조사 기술은 식품의 물리 화학적 특성 변화와 관련된 연구가 활발히 진행 중이며(Nagy 등, 2011; Song 등, 2007), 그중 녹차(green tea) 추출물에 감마선을 조사한 결과, 항산화와 관련된 활성이 상승한 것이 보고가 되었다(Lee 등, 2006). 또한 감마선 조사된 잔디(Eremochloa ophiuroides) 추출물에서 미백 및 주름개선과 관련된 tyrosinase 및 elastase 효소를 효과적으로 저해하는 것이 보고가 되었고(Lee 등, 2013), anthocyanin 화합물인 cyanidin-3-O-xylosylrutinoside가 함유되어 있는 오미자(Schizandra chinensis) 추출물에 감마선을 조사한 결과, cyanidin-3-O-xylosylrutinoside의 함량이 감소되고, 신규 생성된 물질이 LC-MS 분석으로 구조 동정되었으며, 색소 제거 메커니즘이 검증되었다(Lee 등, 2011). 또한 flavonoid, phenylpropanoid, chlacone 및 xanthone 등의 다양한 페놀성 화합물에 감마선 조사시 구조 변환된 신규 물질이 동정되었으며, 우수한 기능성 활성 등이 보고가 되었다(Byun 등, 2018; Jo 등, 2016). 하지만 benzotropolone 골격의 화합물에 대한 감마선 조사에 의한 구조 변환 및 기능성 상승과 관련된 연구 결과는 없었다.
본 연구에서는 대표적인 benzotropolone 골격의 화합물인 purpurogallin에 감마선 조사 후 신규 생성된 화합물을 HPLC 분석으로 확인하였으며, 각 선량별 purpurogallin 조사산물을 항산화 활성과 관련된 DPPH, ABTS+ 및 hydroxyl 라디칼 소거활성 평가를 수행하였다. 신규 생성물을 칼럼크로마토그래피 및 기기분석을 이용하여 구조를 동정하였으며, 분리된 화합물에서 강한 라디칼 소거활성을 확인하였기에 그 결과를 보고하고자 한다.
재료 및 방법
본 실험에서 사용한 purpurogallin과 라디칼 소거활성 평가에 사용된 1,1-diphenyl-2-picrylhydrazyl(DPPH), 2,2'-azino-bis (3-ethylbenzothiazoline-6-sulfonic acid)(ABTS+), deoxyribose 및 (+)-catechin 등의 시약은 Sigma Chemical Co.(St Louis, MO, USA)에서 구입하여 사용하였다. 1H 및 13C NMR 스펙트럼은 CD3OD용매(δH 3.35, δC 49.0)를 이용하여 600 MHz FT-NMR spectrometer(FT-NMR, Varian VNS600, Palo alto, CA, USA)로 측정하였으며, 분석 및 column chromatography용 용매는 특급시약을 사용하였다. FABMS 스펙트럼은 JMS- 700 spectrometer(JEOL, Tokyo, Japan)를 활용하여 분자량을 측정하였다.
순수한 purpurogallin(200 mg)을 methyl alcohol(MeOH) 400 mL에 녹인 후 바이알에 넣어 각 10, 25, 50 및 100 kGy 선량으로 한국원자력연구원 첨단방사선연구소 내 선원 10만 Ci의 cobalt-60 감마선 조사시설(point source AECL, IR-79, MDS Nordion international Co. Ltd., Ottawa, ON, Canada)을 이용하여 감마선 조사를 하였다(Jeong 등, 2018). 흡수선량 확인은 alanine dosimeter(5 mm, Bruker Instruments, Rheinstetten, Germany)를 사용하였으며, dosimeter는 국제원자력기구(IAEA)의 규격에 준용하여 표준화한 후 사용하였다. 각 선량별 조사된 purpurogallin 조사산물의 분석에는 HPLC(LC-20A, Shimadzu, Tokyo, Japan)와 ODS column (YMC gel ODS A-323, 4.6 mm×150 mm)을 사용하였다. 이동상 용매로는 0.1% formic acid(solvent A)와 acetonitrile (solvent B)을 사용하여 gradient elution을 90% A; 10% B로 분석하여 5 min, 5% A; 95% B, 20 min의 용매조성으로 물질을 분석하였고, 이동상의 유속은 1.0 mL/min으로 유지하였으며, 검출기는 SPD-M20A(Shimadzu, Tokyo, Japan)를 이용하여 280 nm에서 화합물을 검출하였다(Fig. 1).
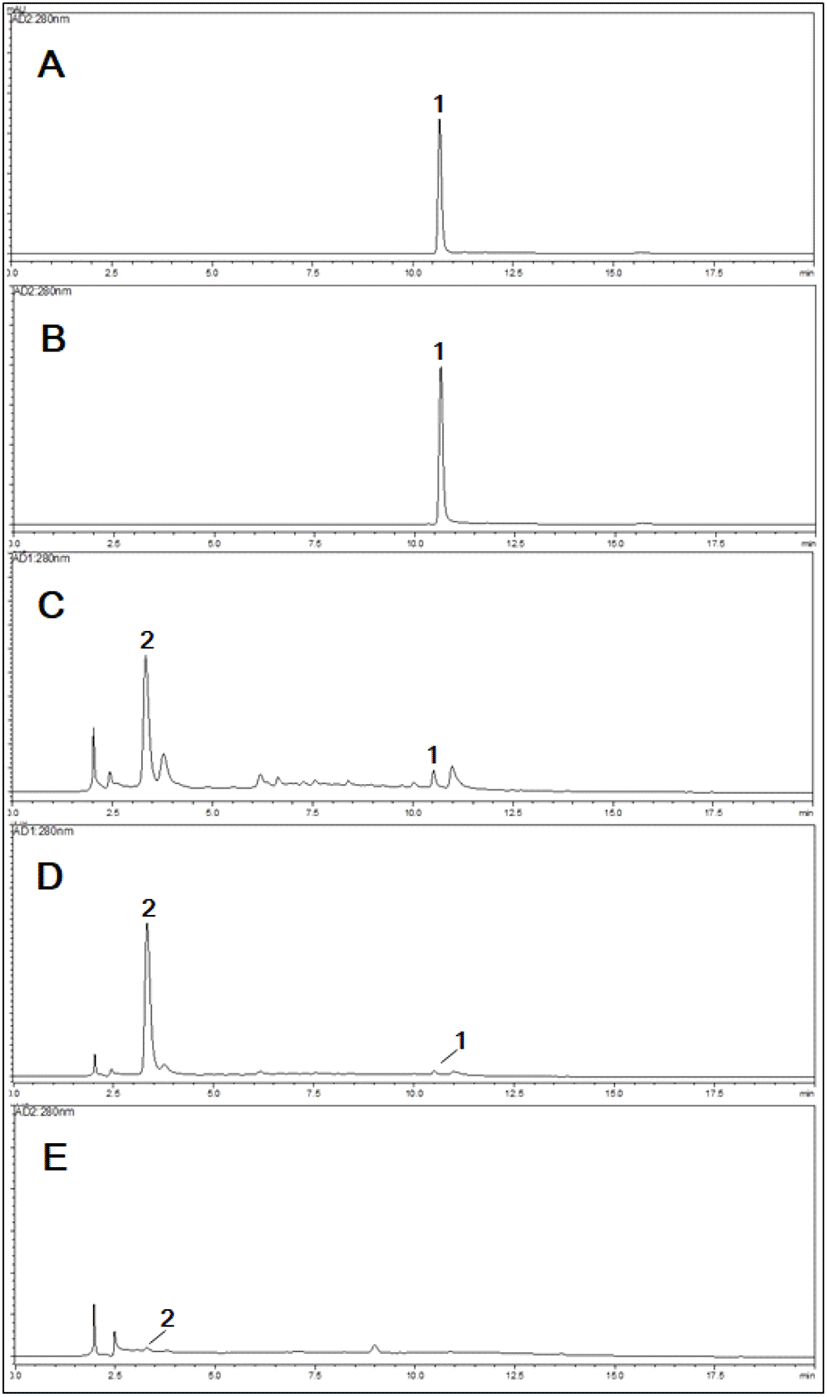
순수한 purpurogallin에 각 10, 25, 50 및 100 kGy 선량으로 감마선 조사한 후 각 조사산물을 항산화 활성과 관련된 DPPH, ABTS+ 및 hydroxyl 라디칼 소거활성 평가를 수행하였다. 그 결과, 50 kGy 선량으로 조사된 purpurogallin 조사산물에서 상대적으로 가장 우수한 라디칼 소거 활성을 나타내어 활성물질의 분리 및 정제를 하였다(Table 1). 50 kGy 선량으로 조사된 purpurogallin 조사산물(176 mg)을 ODS gel(YMC gel ODS AQ 120-50S, YMC Co., Kyoto, Japan) 칼럼크로마토그래피(1 cm i.d.×42 cm) 및 semi-preparative HPLC를 이용하여 화합물의 분리 및 정제를 수행하였으며, 10% MeOH을 용출하여 얻어진 fraction에서 화합물 2가 검출되었고, 건조한 결과 67.2 mg을 수득하였다. 분리된 단일물질은 감마선 조사된 purpurogallin 분해산물과 비교․분석하여 pyrogallol(2)(tR 3.3 min)의 존재를 HPLC 분석으로 확인하였고, NMR 및 FABMS 등의 기기분석을 활용하여 구조를 동정하였다(Fig. 2).
감마선 조사된 purpurogallin 조사산물 및 분리된 단일물질의 DPPH 라디칼 소거활성은 Blois(1958)가 행한 방법을 변형하여 측정하였다. 각 시료용액 120 μL에 0.45 mM의 DPPH 용액 60 μL를 넣고 교반한 후 15분간 방치한 다음 ELISA reader(Infinite F200, Tecan Austria GmBH, Grödig, Austria)를 이용하여 517 nm에서 흡광도를 측정하였다.
ABTS+ 라디칼 소거능은 Re 등(1999)의 방법을 변형하여 다음과 같이 측정하였다. 7 mM ABTS+ 와 2.4 mM 과황산칼륨 동량을 혼합 후 암실에서 12시간 방치하여 라디칼의 생성을 유도하였다. 생성된 ABTS+ 라디칼 용액을 희석하여 734 nm에서 흡광도 값이 0.7-0.8 정도가 되도록 희석한 후 사용하였다. 희석한 ABTS+ 라디칼 용액 100 μL와 각 선량별 조사산물과 단일물질 100 μL를 혼합하여 실온에서 7분간 반응시킨 후 ELISA reader로 734 nm에서 흡광도를 측정하였다.
Hydroxyl 라디칼 소거활성은 deoxyribose 방법(Li, 2013)을 변형하여 다음과 같이 측정하였다. 2.5 mM deoxyribose, 1.5 mM H2O2, 100 μM FeCl3 및 100 μM EDTA를 10 mM phosphate buffer(pH 7.4)에 녹인 후 농도 별로 제조한 시료에 첨가한다. 반응 시작 전 100 μM ascorbic acid를 첨가한 후 37°C에서 1시간 동안 반응시킨다. 반응 후 0.5% thiobarbituric acid와 2.8% trichloroacetic acid를 첨가한 후 80°C의 온도에서 20분 동안 가열한다. 이후 급속 냉각시킨 후 ELISA reader를 이용하여 532 nm에서 흡광도를 측정한다.
DPPH, ABTS+ 및 hybroxyl 라디칼 소거활성 평가에 사용한 양성대조군은 천연 항산화제로 알려진 (+)-catechin를 사용하였으며, purpurogallin의 감마선 조사산물과 분리된 화합물의 라디칼 소거활성은 시료용액의 첨가군과 무첨가군의 흡광도 감소율을 확인하였고, SC50(half maximal scavenging activity concentration)값은 시료가 DPPH, ABTS+ 및 hybroxyl 라디칼을 50% 소거하는 농도로 나타내었다.
결과 및 고찰
순수한 purpurogallin을 MeOH에 녹인 후 10, 25, 50 및 100 kGy 선량으로 감마선을 조사 후 농축하였으며, 감마선 조사 선량별 purpurogallin 조사산물에 대해 항산화 활성과 관련된 DPPH, ABTS+ 및 hydroxyl 라디칼 소거활성 평가를 수행하였다. DPPH 라디칼 소거 활성 평가에서 10 및 25 kGy 선량으로 조사된 purpurogallin 조사산물의 SC50 값이 각 15.5±0.4 및 12.8±0.5 μg/mL의 활성으로 대조군(SC50: 17.7± 0.3 μg/mL)에 비해 조금 상승한 라디칼 소거활성을 나타내었으며, 50 kGy 선량으로 조사된 조사산물의 SC50 값이 10.8± 0.1 μg/mL로 상대적으로 가장 우수한 DPPH 라디칼 소거활성을 나타내었다. 하지만 100 kGy 선량으로 조사된 purpurogallin 조사산물의 SC50 값은 12.7±0.3 μg/mL로 50 kGy 선량으로 조사된 조사산물에 비해 낮은 활성을 나타내었다.
ABTS+ 라디칼 소거활성 평가에서 25 및 50 kGy 선량으로 조사된 purpurogallin 조사산물의 SC50 값이 각 4.8±0.3 및 3.5±0.2 μg/mL로 상승된 ABTS+ 라디칼 소거활성을 나타내었고 hydroxyl 라디칼 소거활성에서도 역시 조사선량이 증가함에 따라 라디칼 소거활성이 증가하는 경향을 나타내었으며, 50 kGy 선량으로 조사된 purpurogallin 조사산물의 SC50 값이 24.5±0.6 μg/mL로 가장 우수한 라디칼 소거활성을 나타내었다. 하지만 100 kGy 선량으로 조사된 purpurogallin 조사산물은 다소 낮은 라디칼 소거활성을 나타내었다(Table 1). 이에 각 선량별 조사산물을 HPLC를 이용하여 분석을 수행한 결과, 25 및 50 kGy 선량으로 조사된 반응물에서 purpurogallin은 감소하였고, 신규 생성된 peak가 retention time(tR) 3.3분에서 검출되었다(Fig. 1). 100 kGy 조사산물에서도 신규 생성물이 미량 검출되었으며, 25 및 50 kGy 조사산물보다 낮은 라디칼 소거활성은 신규 생성물의 함량에 의한 차이임을 확인하였다. 가장 우수한 활성을 나타낸 50 kGy 선량으로 조사된 purpurogallin 조사산물의 신규 생성 물질은 ODS gel을 충진제로 활용한 칼럼크로마토그래피를 이용하여 저분자 페놀 유도체를 분리하였다. 분리된 화합물은 구조 결정을 위하여 1H, 13C NMR 및 FABMS 스펙트럼을 측정하였다(Fig. 2).
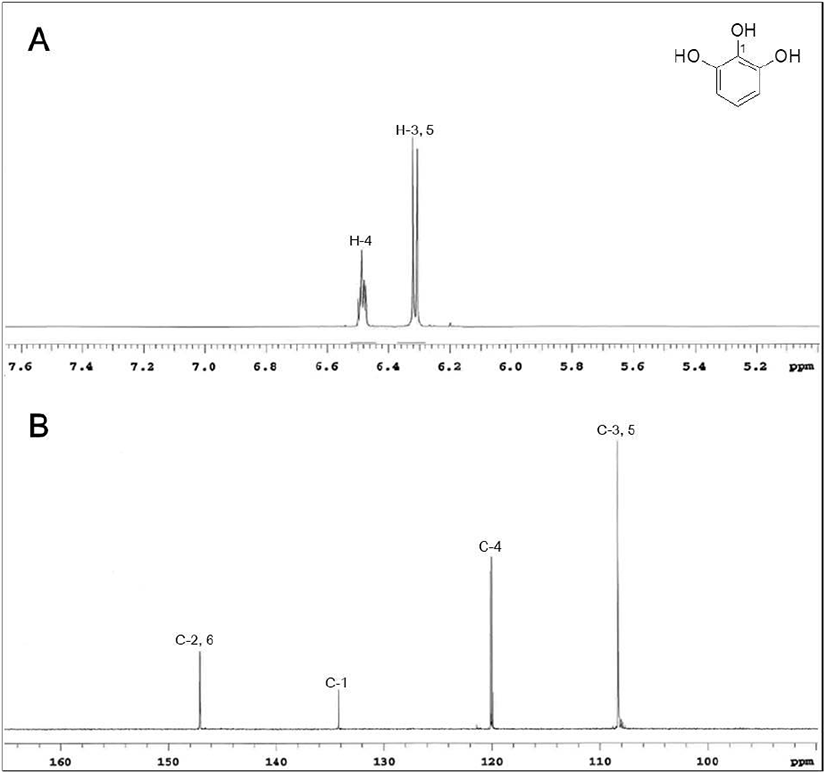
화합물 2는 흰색의 무결정형 분말상으로 얻어졌으며, FABMS 측정 결과 m/z 127[M+H]+에서 base peak를 확인하여 C6H6O3의 분자식을 추정하였다. 1H NMR 스펙트럼 해석으로 2개의 방향족 proton 시그널을 δH 6.48(1H, t, J = 8.4 Hz, H-4) 및 6.32(2H, d, J = 8.4 Hz, H-3과 H-5)로 관찰하였다. 또한 13C NMR 스펙트럼 해석으로 δC 147.0(C-2와 C-6), 134.2(C-1), 119.9(C-4) 및 108.3(C-3과 C-5)에서 6개의 벤젠 유래의 carbon 시그널이 관찰되었다. 이상의 1H 및 13C NMR 데이터 해석과 문헌치(Kularni 등, 2008) 및 표품과의 HPLC를 직접 비교하여 화합물 2는 저분자 페놀성 화합물인 pyrogallol로 구조 동정하였다(Fig. 2).
감마선 조사된 purpurogallin 조사산물에서 우수한 라디칼 소거활성을 확인하였고, ODS gel을 충진제로 이용한 칼럼크로마토그래피 및 기기분석을 이용하여 신규 생성된 화합물의 분리 및 정제를 수행하였다. 분리된 화합물은 저분자 페놀성 화합물인 pyrogallol(2)으로 구조 동정하였으며, 항산화 활성과 관련된 DPPH, ABTS+ 및 hydroxyl 라디칼 소거활성 평가를 수행하였다. 그 결과, 신규 생성된 저분자 페놀성 화합물인 pyrogallol(2)의 DPPH 라디칼 소거능의 SC50 값은 9.5±0.3 μM로 나타내었으며, purpurogallin(1)(SC50: 65.1±1.0 μM)에 비해 월등히 상승된 활성임을 확인하였다.
ABTS+ 라디칼 소거능에서 감마선 조사된 purpurogallin 조사산물에서 신규 생성된 화합물 2의 SC50 값이 12.6±0.4 μM으로 우수한 ABTS+ 라디칼 소거활성을 나타내었으며, hydroxyl 라디칼 소거능에서도 48.1±0.9 μM의 SC50 값을 나타내어 purpurogallin에 비해 상승된 라디칼 소거활성을 나타내었다. 감마선 조사된 purpurogallin 조사산물로부터 신규 생성된 저분자 페놀성 화합물 2는 항산화 활성 평가에서 양성대조군으로 사용된 천연 항산화제인 (+)-catechin보다 우수한 DPPH, ABTS+ 및 hydroxyl 라디칼 소거 활성을 나타내었다(Table 2).
| Compounds | SC50 values (μM) | ||
|---|---|---|---|
| DPPH | ABTS+ | Hydroxyl | |
| Purpurgallin (1) | 65.1±1.0a1) | 36.3±0.6a | 124.9±1.7a |
| Pyrogallol (2) | 9.5±0.3c | 12.6±0.4b | 48.1±0.9c |
| (+)-Catechin2) | 22.4±0.7b | 14.7±0.5b | 60.9±1.4b |
최근 연구에서 콩과 식물의 주요 성분인 genistein에 감마선을 조사한 결과, 신규 생성된 genistein 유도체가 genistein보다 우수한 항산화 활성을 나타냄이 보고가 되었다(Jung 등, 2009). 또한 감마선 조사된 cyanidin 3-rutinoside 조사산물로부터 신규 생성된 phenolic acid 유도체 화합물인 protocatechuic acid methyl ester가 구조 동정되었고, 우수한 DPPH 라디칼 소거활성이 보고가 되었다(Lee 등, 2014). 본 연구에서도 purpurogallin에 감마선 조사로 신규 생성된 저분자 페놀 유도체를 분리 및 구조 동정하였고, 항산화 활성과 관련된 DPPH, ABTS+ 및 hydroxyl 라디칼 소거활성 평가에서 우수한 소거활성을 확인하였다. 향후 신규 생성물은 세포 실험 및 동물 실험을 통해 항산화 활성 기작에 대한 연구가 필요하며, 이상의 연구 결과는 감마선 조사시 생성되는 화합물의 구조 및 항산화 활성 변화와 관련된 기초자료로서의 활용이 가능할 것으로 사료된다.










