서 론
유지(fats and oils)는 식품에 맛과 향을 제공하며 인체에도 중요한 영향을 끼친다. 그중에서도 식품을 통해 섭취를 해야 하는 linoleic acid(C18:2, ω-6)와 α-linolenic acid(C18:3, ω-3)와 같은 필수지방산들은 탄소 체인에 이중결합을 2-3개 가지고 있는 불포화 지방산이다(1). 이와 같은 불포화 지방산들은 이중결합을 가지고 있지 않은 포화지방산들보다 저장 및 취급 중에 산소, 빛, 열과 같은 요인들에 의해 더욱 쉽게 산화되며, 이는 특히 불포화 지방산을 다량 함유하고 있는 유지 또는 이를 함유한 식품의 산화 안정성에 부정적 영향을 미친다(1).
유지는 식품조리과정에서 열전달 매체로써 이용되며, 조리 후 식품에 고유한 풍미와 조직감을 향상시켜준다. 이때 조리 온도는 튀김(frying)의 경우 일반적으로 150-190℃이다(2,3). 유지의 산화는 공기 중의 산소를 흡수하며 일어나는 자동산화뿐만 아니라 가열에 의하여 분해 및 중합이 일어나며, 이로 인하여 유지에서 공액이중결합의 증가, 색변질, 변향(flavor reversion), 산화생성물의 증가, 중합반응으로 인한 점도 증가 등 물리화학적 변화를 초래한다(2,4). 가열산화는 자동산화에서보다 급격히 가속화되어 일어나며, 오랜 시간 동안의 가열 과정 중에 발생되는 산화물들은 동맥경화, 간 손상 등 인체에 해로운 영향을 준다고 보고되고 있다(5). 이와 더불어 산화에 의하여 유지 또는 유지를 함유한 식품의 색과 향의 변화가 일어나게 되는데, 이러한 변화는 산화 과정 중에 발생되는 여러 종류의 aldehydes, ketone과 같은 2차 산화물들이 그 요인이 된다(4). 이에 따라 식품 산업계에서는 산화에 대한 안정성을 유지하기 위하여 항산화제가 널리 사용되고 있다. 특히, 유지를 가열할 때 유지가 자연적으로 함유하고 있는 천연항산화제 혹은 이들의 인위적 첨가는 산화를 억제시키기 때문에 유지 및 유지함유 식품의 품질을 안정적으로 유지할 수 있다. 일반적으로 많이 사용되는 천연 항산화제인 토코페롤(tocopherol)과 ascorbyl palmitate는 대표적인 지용성 항산화제로서 산화단계에서 생성되는 라디칼에 수소를 공여하여 라디칼의 생성을 막거나 저해하는 역할을 할 수 있다(6). 한편 caffeic acid phenehtyl ester(CAPE)는 caffeic acid와 phenethyl alcohol의 에스테르 화합물로서 항산화능이 보고되었다(7,8).
본 연구에서는 caffeic acid phenethyl ester(CAPE), caffeic acid(CA), ascorbyl palmitate(AP), 그리고 α-tocopherol(α-TO)을 대두유(SBO)에 첨가한 후, 가열 산화 조건에서 색상(Hunter parameters, L*, a*, b*, 그리고 ΔE)의 변화와 토코페롤의 함량 변화를 평가하여 각 항산화물질이 유지 가열시 어떠한 영향을 받는지를 관찰하였다.
재료 및 방법
본 연구에서 사용한 대두유(SBO)는 대형마켓(Daejeon, Korea)에서 구입하였고, 실험에 항산화제로 사용된 α-tocopherol(α-TO), ascorbyl palmitate(AP)도 Sigma-Aldrich Co., (St. Louis, MO, USA)에서 구입하여 사용하였다. CAPE는 선행된 연구에서 기술한 방법을 이용하여 caffeic acid와 phenethyl alcohol의 화학적 반응을 이용한 esterification반응으로 제조하였으며(7,8), CAPE를 합성하기 위한 caffeic acid, phenethyl alcohol, dicyclohexylcarbodiimide(DCC), tetrahydrofuran(THF), SupelcleanTM LC-Si solid-phase extraction tube(6 mL)는 Sigma-Aldrich Co.에서 구입하였다. 추출에 사용된 용매는 normal grade를 사용하였으며 HPLC 분석에 사용한 용매 및 시약들은 HPLC grade 분석용 시약을 Fisher Scientific(Seoul, Korea)에서 구입하여 사용하였다. CAPE 합성 및 분리를 확인하기 위해 사용한 TLC silica gel 60 F254은 MERCK Co. (Darmstadt, Germany)에서 구입하였다.
가열 산화 조건에서의 유지 산화는 다음과 같이 수행되었다. SBO(40 g)을 100 mL screw cap vial에 취한 후 CA, CAPE, α-TO 및 AP을 각각 200 ppm(8 mg)씩 첨가하였다. 균질화를 위해 50℃에서 20 min동안 sonication(Kodo, Daejeon, Korea)한 후, 각 vial을 cap이 없는 상태에서 180±5℃로 유지시킨 히팅 블록에서 가열 산화 반응을 하였다. 반응은 첫날에 4시간을 가열산화한 후 시료를 채취하였고, 4시간을 또다시 수행하여 총 8시간을 가열산화 하였다. 이후 계속해서 매일 8시간씩 가열산화하여 총 32시간(4, 8, 16, 24 및 32 시간)동안 시료를 채취하였다. 반응이 끝난 후 각 시간별로 취한 시료는 5 mL씩 나누어 질소 충진 후 분석하기 전까지 -20℃에서 보관하였다. 실험에 적용된 시간대별 반응이 끝난 후 새로운 SBO의 추가는 하지 않았고, 가열 반응이 끝난 시료는 vial cap을 닫은 채 다음날 실험 전까지 상온의 후드 안에서 방치하였다.
산화생성물인 aldehydes는 1H-NMR(BRUKER AVANCE Ⅲ 600, Bruker, Germany)로 분석하였다. 가열 산화된 유지 시료(약 50 mg)는 700 μL의 chloroform-d[purity 99.8%, contain 0.1% tetramethylsilane (TMS)]에 녹여서 NMR tube(5-mm diameter)에 옮겼다. 1H-NMR 분석을 위한 조건은 12335.5 Hz(spectral width), 16 rounds(scan number), 2.656 s(acquisition time)이었다. Chemical shifts(δ)는 TMS를 δ=0 ppm으로 설정 후 획득하였다. Aldehyde(n-alkenals, 4,5-epoxy-(E)-2-alkenals, (E,E)-2,4-alkadienals, and (E)-2-alkenals)의 signal은 이전의 발표된 연구결과들(8-10)과 비교하였다.
색 변화 측정은 색차계(Color Techno System Corp, Tokyo, Japan)를 이용하여 측정하였으며, Hunter체계 Hunter units L*=[100(white), 0(black)], a*=[+a(red), -a(green)], b*=[+b(yellow), -b(blue)]를 기준으로 하였다. Calibration은 백판(white standard)을 이용하여 수행하였다. Total color difference(ΔE)는 초기 SBO을 기준으로 구하였으며 식은 아래와 같다.
유지 가열 산화에 따른 토코페롤의 조성 변화 및 감소량을 확인하기 위해 형광검출기가 연결된 HPLC(G1311A, Agilent Technologies, Germany)를 이용하여 분석하였고, 토코페롤의 추출은 알칼리 비누화법을 이용하였다(11). 추출관에 시료 500 mg과 6% pyrogallol ethanol용액 10 mL를 첨가하고 2분동안 vortex로 혼합한 후 질소 충진하여 10분 동안 sonication을 하였다. 그 후 60% KOH 용액 8 mL를 첨가하고 균질화 후 75℃, 100 rpm shaking water bath(BS-21, Lab Companion, Ramsey, MN, USA)에서 1 시간 동안 검화 반응을 진행하였다. 토코페롤을 추출하기 위하여 추출용매 hexane:ethyl acetate(85:15, v/v, 0.01% BHT) 15 mL, 2% NaCl 용액 20 mL를 넣고 2 min동안 vortex로 혼합한 후 방치하여 층 분리를 유도한 뒤 상층액만을 취해 anhydrous sodium sulfate column을 통과시켜 수분을 제거하였다. 이를 총 3회 반복 한 후 50 mL volumetric flask에 정용하였다. 토코페롤을 분석하기 위하여 추출물 5 mL를 취한 뒤 질소를 이용하여 용매를 완전히 제거한 후 2.5 mL의 hexane에 녹여 0.50 μm syringe filter(Toyo Roshi Kaisha, Ltd., Japan)로 여과하였고, 이를 20 μL를 주입하여 HPLC로 분석하였다. 사용된 column은 LiChrospher® Diol 100 (Merck KGaA, 250×4 mm, 5 μm, Darmstadt, Germany)이었고, detector는 1200 series 형광검출기[fluorescence(Exλ=290 nm, Emλ=330 nm), Agilent Technologies, Palo Alto, CA, USA]을 사용하였다. 이동상은 hexane:2-propanol (99.4:0.6, v/v)로 조제한 후 1 mL/min의 유속으로 등용리하여 분석하였다. 토코페롤의 함량은 α-, γ-, 그리고 δ-tocopherol 표준물질 분석을 이용하여 정량하였다.
두 번의 측정 결과는 평균값과 편차로 표기하였고 결과값에 유의적 차이를 검증하기 위해 SAS statistical Computer Package V.9.2(SAS institute., cary, NC) 프로그램의 Duncan’s multiple range test를 실시하여 95%(p<0.05) 수준에서 검증하였다(12).
결과 및 고찰
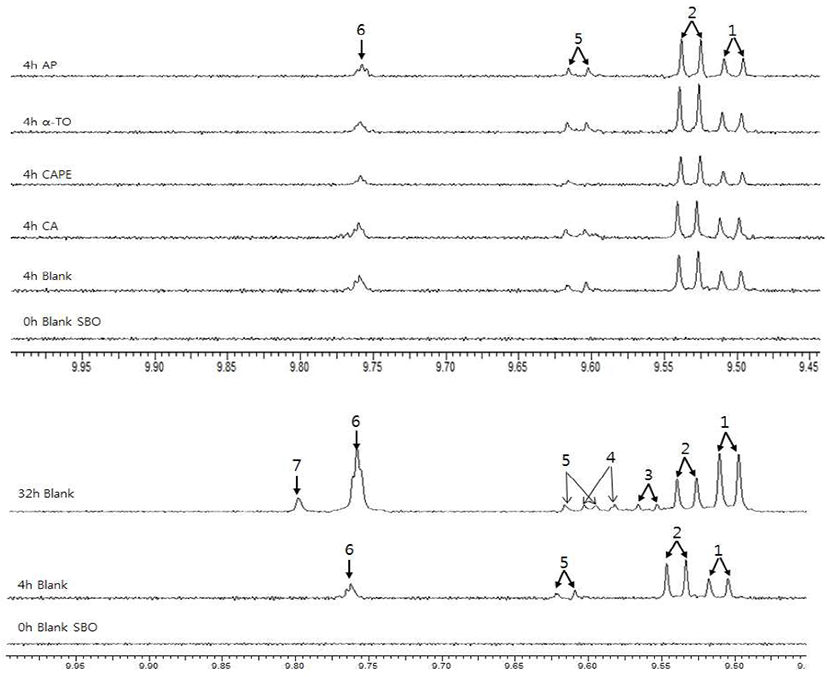
Fig. 1에서 1H-NMR을 이용하여 유지의 2차 산화물인 aldehydes류의 변화량을 나타내었다. 연구 결과에 따르면 유지의 산화 과정 중에 발생되는 산화물들은 1H-NMR로 분석된 8-10 ppm 사이의 chemical shift에서 검출이 가능하다고 하였다(8-10). 먼저 가열 산화하기 전인 SBO(0 시간 Blank SBO)에서는 9.45-9.8 ppm사이에서 유지 산화물로 예측되는 어떠한 peak도 나타나지 않았지만, 4시간 가열한 SBO(4시간 Blank)에서는 (E)-2-alkenals와 (E,E)-2,4-alkadienals를 포함한 aldehydes가 검출 되었고, 특히 32시간 가열 후에는 해당 peak들의 area가 커짐에 따라 산화물의 발생이 증가하였음을 알 수 있었다. (E,E)-2,4-alkadienals는 4시간 경과 후에 다른 aldehydes류보다 빠르게 형성되었다가 32 시간로 가열이 지속됨에 따라 감소하는 경향을 보였고, (E)-2-alkenals과 n-alkanals는 뚜렷하게 계속해서 생성되는 양이 증가하는 것을 볼 수 있었다. 한편, 4,5-epoxy-(E)-2-alkenals, 4-hydroxy-(E)-2-alkenals 그리고 4-oxoalkanals는 4시간 보다는 32시간으로 가열시켰을 때 보다 많이 발생되는 경향을 보였다(Fig. 1). 이와 같은 aldehydes류의 발생은 CAPE를 항산화물질로 사용하였을 때 가장 적었다. 가열 시간을 4시간하였을 때 200 ppm의 CAPE를 첨가한 SBO(4시간 CAPE)는 어떠한 항산화물질을 첨가하지 않은 SBO(4시간 Blank)뿐만 아니라 200 ppm의 AP(4시간 AP), CA(4시간 CA), 그리고 α-TO(4시간 α-TO)을 첨가한 SBO보다도 aldehydes peak의 area가 상대적으로 적었다. 이는 CAPE의 첨가가 유지의 가열산화를 일정 부분 억제할 수 있다는 것을 의미한다고 할 수 있다.
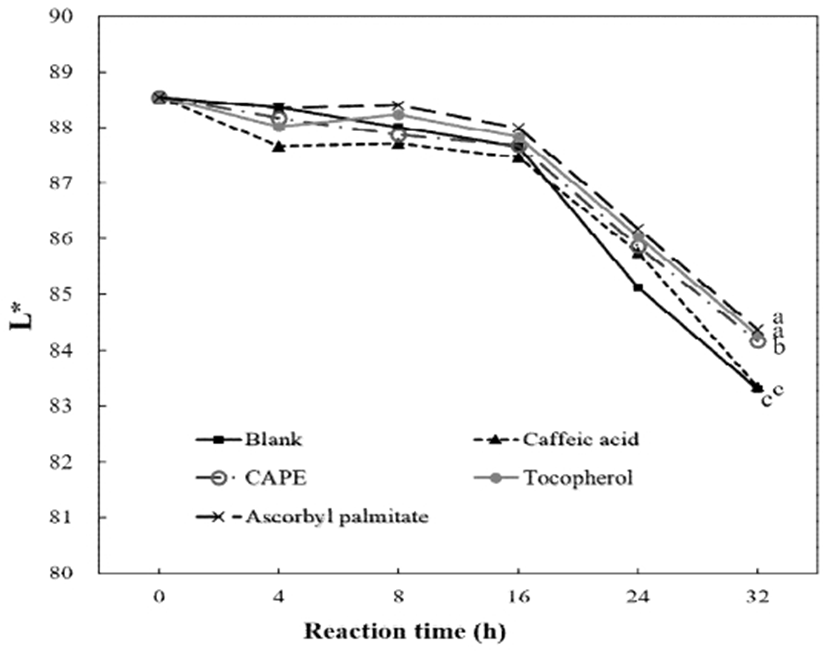
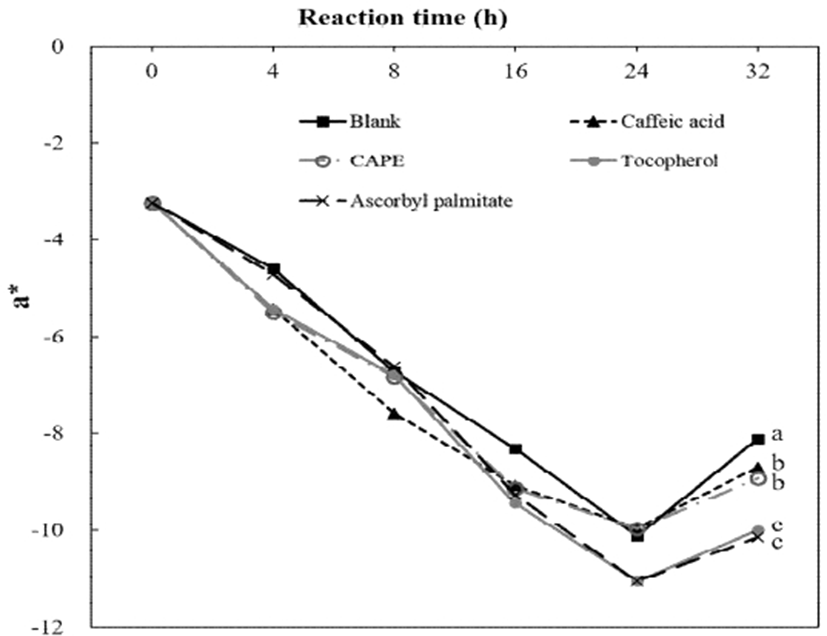
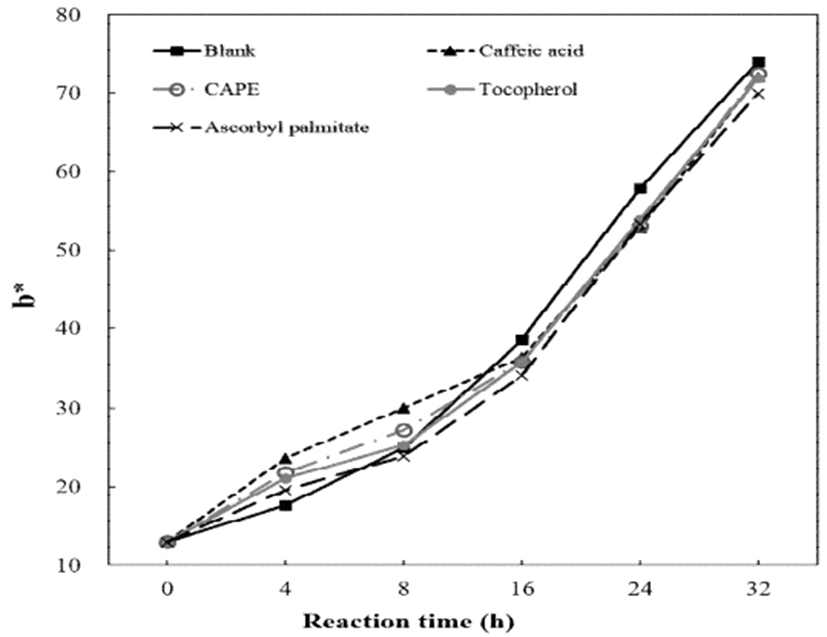
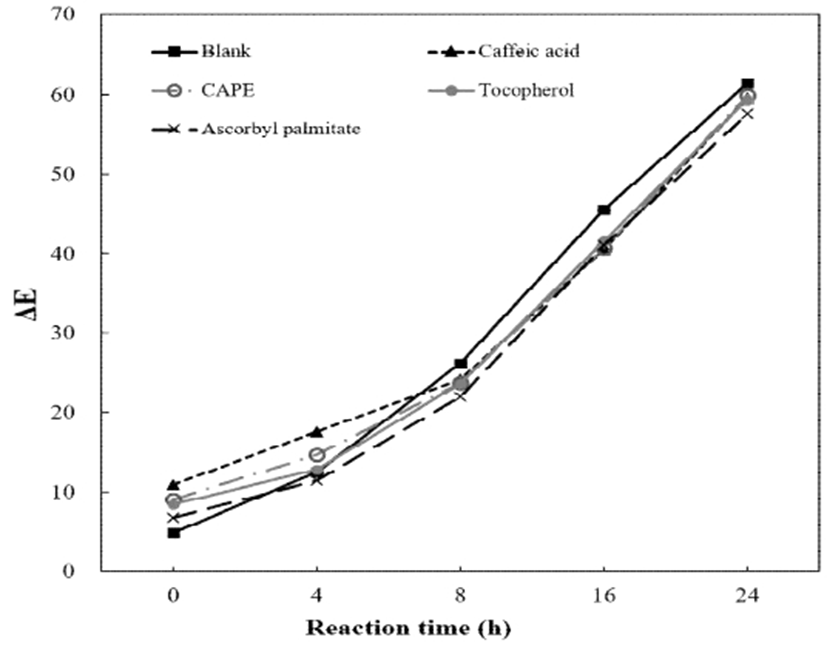
산화가 진행되는 유지에서 가장 눈에 띄게 변하는 현상 중 하나는 유지의 색이다. 일반적으로 가열 산화되는 시간이 길어질수록 유지의 색은 초기 연한 노란색에서 점차 검붉은 색으로 어두워진다. 이는 유지의 산화 반응, 중합 반응 및 기타 화학 반응 등 복합적인 결과이다(13). 본 실험에서는 산화 반응이 진행됨에 따라 유지의 색 변화를 육안 관측(Fig. 2) 및 Hunter parameters L*, a*, b* 그리고 ΔE로 나타내었다(Fig. 3-6). 육안으로 보았을 때 가열시간을 4시간에서 32시간으로 늘려감에 따라 가열된 SBO의 색은 뚜렷하게 진한 황색으로 변해가는 것을 관찰 할 수는 있었으나 첨가된 항산화 물질에 따른 색의 차이를 비교하기에는 어려움이 있었다. 일반적으로 유지의 색상은 Lovibond법을 이용하지만 본 연구에서는 색차계를 이용하여 L*, a*, b*, ΔE의 차이를 나타내었다. L*은 명도를 나타내는 지표인데 가열 산화하기 전인 SBO(Blank)는 88.5의 값을 보였으나, 32시간 가열 후에는 83.3으로 약 6% 감소하였다. 한편, 어떠한 항산화제(CAPE 및 CA, α-TO, AP)를 첨가하였더라도 24시간 동안의 L*값 차이는 서로 간에는 크지 않았으나, 항산화제를 첨가하지 않은 Blank보다는 높은 L*값을 보였다. 반면에 32시간 가열 후에서는 CA를 첨가한 SBO의 L*값이 Blank의 값과 유사하게 낮아지면서 CAPE, α-TO, 그리고 AP를 첨가한 SBO의 L*값과 유의적으로 차이를 보였다(p<0.05)(Fig. 3). 그러나 CA 이외의 항산화제들(CAPE, α-TO, AP)은 Blank보다 높은 L*값을 보였기 때문에 오랜 가열 산화에 의하여 유지의 색상이 어두워지는 현상을 특정 항산화 물질이 어느 정도 억제 할 수 있을 것으로 사료된다. a*값은 낮을수록 초록색을, 그리고 높을수록 붉은색을 나타내게 되는데 Blank의 경우 가열 산화하기 전에 -3.23를 보였고, 이는 24시간 가열할 때 -10.12로 낮아지다가 이후 다시 증가하는 경향을 나타내었다(Fig. 4). 항산화제를 첨가한 모든 SBO에서도 Blank와 유사한 경향, 즉 가열 시간이 길어질수록 a*값이 감소되다가 24 시간 이후 증가하는 경향을 보였다. 32시간 가열 후 사용된 항산화제들 중에서 CA 및 CAPE는 각각 -8.7, -8.9의 값을 보이면서 Blank보다 유의적으로 낮았고, α-TO와 AP는 Blank, CA 그리고 CAPE보다도 낮은 a*값을 나타났다(p<0.05)(Fig. 4). b*값은 높을수록 노란색을 나타내게 되는데 가열시간이 길어질수록 모든 시료에서 점차 증가하였다(Fig. 5). 가열 산화하기 전인 SBO(Blank)의 경우 13의 값에서 32시간 가열 후에서는 74까지 크게 증가하였다. 이는 육안으로 관찰하였을 때 모든 시료에서 뚜렷하게 황색으로 변한 것과 같은 결과로 볼 수 있다. 32시간 가열 후 항산화제가 첨가된 SBO에서 b*값은 69.9(AP), α-TO(71.8), CA(72.04)와 CAPE(72.50)으로 서로 유사하게 측정되어 유의적 차이는 없었다(p>0.05). 한편, 32시간 가열 후 전체적인 색 변화를 나타내는 ΔE(total color difference)의 순서는 Blank > CA = CAPE = α-TO > AP이었으나 서로간의 유의적 차이는 없었다(p>0.05) (Fig. 6). 가열 산화 유지에서 색의 변화는 원재료에 함유된 지용성 색소의 변화에 의한 영향과 중합체 생성물, 그리고 carbonyl 2차 산화물들이 주요 원인으로 알려져 있다(2,14,15). 또한, 식품을 유지에 튀겼을 경우에는 maillard reaction도 고려해 볼 수 있다. 유지 산화로부터 야기되는 carbonyl기와 식품으로부터 유리되는 amino기 간의 반응으로 melanoidin과 같은 갈색물질을 생성하기 때문이다. Totani 등(16)은 가열 유지의 색 변화가 유지 자체의 가열적 열화가 주된 원인이며, 그 외에도 가열 산화된 기름이나 지방산 그리고 튀김 식품에서 나온 아미노산으로 형성된 amino-carbonyl 화합물이 기여한다고 설명하고 있다. 그러나 본 실험에서는 식품의 첨가 없이 유지만 가열했기 때문에 maillard 반응으로 야기되는 색변화가 크게 기여하지 않았을 것으로 추정된다. 한편, Chu와 Luo(17)는 유지의 색상 측정은 유지 성분과 튀기는 식품 성분 요소의 간섭 가능성으로 인해 유지 품질을 모니터링 하는데 적절하지 않다고 제시하였다.

토코페롤 및 토코트리엔올은 자연적으로 발생하는 식물성 기름에서 중요한 생체 활성 성분으로서 효율적인 alkoxyl 및 peroxide radicals 제거할 수 있는 주요 친유성 산화 방지제뿐만 아니라 활성 산소 및 활성 질소 등으로 야기되는 산화 스트레스로부터 인간을 보호하는 역할을 한다(18). Deep frying 조건에서의 유지는 가열 산화, 가수 분해와 같은 반응이 일어남에 따라 유지의 품질 악화뿐만 아니라 토코페롤의 손실을 야기하며, 이는 유지의 안정성 감소로 이어져 튀겨진 식품의 유통 기한과 안정성에 대해 영향을 미칠 수 있다(19). 따라서 본 연구에서는 SBO의 가열 산화 조건에서 첨가된 항산화제(CA, CAPE, α-TO 및 AP)에 의한 토코페롤 손실 억제 정도를 평가하였다(Table 1). 실험에 사용된 SBO은 γ > α > δ 순으로 각각 191, 114, 및 14 ppm, 총 319 ppm의 토코페롤을 함유하였다. 이는 여러 콩 품종의 토코페롤 isomer 함량 보고에서 γ-토코페롤의 함량이 가장 많았다는 결과와 같다(20). 유지의 가열 산화가 진행됨에 따라 토코페롤은 모든 시료에서 급격하게 손실되었는데, δ- 보다는 α- 및 γ-토코페롤에서 함량의 감소 변화가 뚜렷하였다. 특히, 4시간 가열 후 항산화제를 첨가한 모든 SBO의 α-토코페롤 함량 변화는 Blank(항산화제 미첨가 SBO)보다 적었는데, α-토코페롤의 잔존율(retention)은 CAPE(60.4%) > AP(52.8%) > α-TO(43.9%) > CA(41.0%) > Blank(31.7%)순이었고, 이와 같이 항산화제를 첨가하였을 때 Blank보다 높은 잔존율(retention)이 나타나는 결과는 8시간 가열 후에서도 보였다(Table 1). 특히 α-TO는 200 ppm의 α-토코페롤을 첨가하였기 때문에 다른 시료들보다도 많은 총 314 ppm의 α-토코페롤을 함유하고 있었으나, 4시간 가열 후의 잔존율은 CAPE와 AP보다도 낮았다. 32시간 가열 후에서는 α-TO와 CAPE를 제외한 나머지 항산화제 첨가 시료들에서 α-토코페롤은 검출되지 않았고, CAPE (5.2%)에서 α-TO(2.8%)보다 잔존율이 높았다. Gordon과 Kourimská(21)에 따르면 튀김 온도에서 α-토코페롤이 가장 빨리 손실된다고 하였으며, 산화에 더 활동적인 항산화제의 존재는 토코페롤의 손실을 억제시킬 수 있는데, 로즈메리 추출물이나 ascorbyl palmitate의 사용이 토코페롤의 손실 속도를 줄일 수 있다고 하였다. γ-토코페롤은 α-토코페롤과 다소 다른 경향의 잔존율을 보였다. 4시간 가열 후의 γ-토코페롤 잔존율은 CAPE(76.9%) > AP(61.8%) > Blank (47.0%) > CA(32.2%) > α-TO(30.8%) 순이었고, 이유가 명확하지는 않으나 CA와 α-TO가 Blank보다도 낮은 γ-토코페롤 잔존율을 나타내었다. 그러나 8시간 가열 후에서는 CAPE(29.7%) ≥ AP(29.5%) > α-TO(21.1%) > CA(18.5%) ≥ Blank(18.4%)의 순서로 γ-토코페롤 잔존율을 보였고, 이후 모든 시료에서 점차적인 감소를 보이면서 32시간 가열 후에는 3.3-5.1%의 γ-토코페롤 잔존율이 나타났다(Table 1). 한편, 실험에 사용된 항산화제들 중에서 가장 polar한 성질을 가지고 있는 CA는 γ-토코페롤의 손실을 억제하는데 뚜렷한 효과를 보이지 못했다. 이러한 이유는 CA가 항산화제로서의 역할을 수행할 때, CA가 토코페롤보다 산화되는 속도가 느리기 때문이라 생각된다. Reblova 등(22)은 8가지의 페놀산(gallic, gentisic, protocatechuic, syringic, vanillic, ferulic, caffeic, 그리고 sinapic acid) 중에서 다른 페놀산보다 free radical의 소거능이 가장 큰 gallic acid를 제외한 나머지 물질에서는 산화 과정중의 α-토코페롤 손실에 대해서 효과를 볼 수 없었다고 보고하였다. 결론적으로 200 ppm의 CAPE와 AP는 초기 가열시간인 4시간과 8시간에서는 토코페롤 이성체들의 손실을 억제할 수 있었으나 16시간이후에서는 큰 영향을 미치지 않는 것으로 생각되며, 200 ppm α-토코페롤의 첨가는 가열 산화시에 α-토코페롤 잔존에도 효과가 크지 않았다고 할 수 있다. 그럼에도 불구하고 CAPE는 실험에 사용된 다른 어떤 항산화제들보다 초기 가열시간동안 토코페롤 이성체들의 손실을 억제하는데 가장 큰 효과가 있었다.
요 약
1H-NMR을 이용하여 유지의 2차 산화물류의 발생 변화량을 살펴보았을 때, 200 ppm의 CAPE 첨가는 AP, CA, 그리고 α-토코페롤을 첨가하였을 때 보다 aldehydes peak의 area가 뚜렷하게 적었고, 이는 CAPE의 첨가가 유지의 가열산화를 일정 부분 억제할 수 있다는 것을 의미한다고 할 수 있다. CAPE, α-TO, 그리고 AP 첨가구에서는 blank보다 32시간 가열된 유지에서 유의적으로 높은 L*값을 보였으나, 전체적인 색 변화를 나타내는 ΔE(total color difference)는 서로 간의 값 차이가 크지 않았다. 가열 산화 시에 손실되는 토코페롤 이성체들의 잔존율을 살펴본 결과, δ- 보다는 α- 및 γ-토코페롤에서 함량의 감소 변화가 컸으며, 실험에 사용된 항산화제들 중에서 가장 극성의 성질을 가지고 있는 CA는 CAPE와 AP보다 γ-토코페롤의 손실을 억제하는데 뚜렷한 효과를 보이지 못했다. 그러나 CAPE는 실험에 사용된 다른 어떤 항산화제들보다 초기 가열시간동안 토코페롤 이성체들의 손실을 억제하는데 가장 큰 효과가 있었다.










