서 론
1) 최근 생활수준이 향상됨에 따라 현대인들의 식생활은 서구화 되어 동물성 식품 및 고칼로리 인스턴트식품의 섭취 가 증가하고 있다. 이로 인해 건강에 대한 관심이 높아지고 있으며, 건강 증진을 위해 장내 균총을 새롭게 형성하거나 면역계 활성 등을 목적으로 프로바이오틱스(probiotics)라 는 미생물 유래 기능성식품이 소비되고 있다(1,2). 또한 비 만, 당뇨병 및 고혈압 등의 만성질환 유병률이 증가함에 따라 소비자들은 영양공급이라는 식품고유의 기능 이외에 건강증진과 질병치료 등의 기능을 가진 식품에 대한 관심이 늘어나고 있다(3,4). 식품공전에서의 효소식품은 식물성 원료에 식용 미생물을 배양시켜 효소를 다량 함유하게 하거나 식품에서 효소함유 부분을 추출한 것 또는 이를 원료로 하여 섭취가 용이하도록 가공한 것으로 정의하고 있다. 식 품 유형상 기타 식품류에 속하며 곡류 효소함유 제품, 배아 효소함유 제품, 과채류 효소함유 제품 및 기타 식물 효소 제품으로 분류된다(5).
발효는 미생물을 이용하여 유기물을 분해시키는 과정으 로 유효성분 및 흡수율 증가 등의 효과를 나타내어 다양한 기능성 연구가 활발히 이루어지고 있다(6). 특히, 영양성분 을 그대로 유지하면서 미생물이 분비하는 각종 가수분해효 소와 세포 내 조직에 결합되어 있는 생리활성 물질들이 유리화되면서 생체 이용률을 향상 시켜주는 효과가 있다 (7).
아마란스(Amaranthus ssp L.)는 비름과에 속하는 일년생 식물로 곡물과 비슷하여 아곡류(pseudocereal)로 불려지고 있으며 영양성분을 보면 조단백질은 17~18%, 지방은 7~8% 정도로 옥수수나 밀보다 높으며 섬유소는 비슷하거나 높게 함유하고 있다. 특히 아마란스 단백질은 화곡류에 부족한 lysine 함량이 단백질 100 g당 5.2 g으로 옥수수(3.4 g), 밀 (3.2 g)에 비해 높으며, 스쿠알렌, 토코트리에놀, 비 발효성 식이섬유, 인지질, 렉틴 및 기타 항산화 성분 등 다수의 유용한 기능성분을 함유하고 있다(8,9,10). 이와 같이 아마란 스는 영양 생리학 측면에서 유용 성분을 함유하고 있어 지질대사에 효과가 있으며 또한 아마란스 전분 입자의 크기 는 전분 중 가장 작아 다양한 용도로 이용이 가능하여 제과· 제빵용 혼합분, 국수, 비스켓 등에 혼합하여 사용되고 있다 (11,12,13).
따라서 본 연구에서는 곡류 효소함유 제품 개발을 위한 소재 탐색의 일환으로 아마란스를 영양원으로 하여 protease를 생산하는 Bacillus amyloliquefaciens CGD3로 발 효하였으며 발효시간에 따른 배양특성과 기능적 특성을 조사하였다.
재료 및 방법
본 실험에 사용한 아마란스는 원산지가 강원도 평창군인 제품을 농협 하나로마트에서 구입하여 이물질을 제거하고 분쇄기(J-NCM, Jisico, Seoul, Korea)로 분쇄하여 40 mesh 표준망체를 통과시켜 사용하였다. 아마란스 발효를 위해 사용된 미생물은 청국장으로부터 분리동정하여 보관중인 Bacillus amyloliquefaciens CGD3(KACC92048P) 균주를 이 용하였다.
아마란스 발효물 제조를 위한 starter 배양액은 nutrient broth를 121℃에서 15분간 멸균한 액체 배지에 nutrient agar(Difco, Detroit, MI, USA)로 37℃에서 24시간 동안 배양한 B. amyloliquefaciens CGD3를 1회 접종한 뒤, 진탕배양기 에서 37℃, 24시간 동안 배양하여 starter로 사용하였다.
발효시간에 따른 아마란스 발효물 제조를 위해 각각의 아마란스 분말 20 g을 삼각플라스크에 넣고 살균 후 40 mL의 멸균수를 가한 다음 미리 배양된 B. amyloliquefaciens CGD3 starter액을 2% 접종 후 37℃ 진탕배양기에서 96시간 까지 발효하였으며, 발효물의 배양적 특성은 배양 시간별 로 측정하였다. 배양이 완료된 발효물은 동결건조 하였으 며, 동결건조 분말은 -72℃에 보관하면서 실험에 사용하였 다.
아마란스 발효물의 생균수 측정은 배양액 1 mL에 0.85% sodium chloride(Duksan pure chemicals, Ansan, Korea)용액 9 mL를 혼합하여 10배 희석법으로 희석한 다음, 각각의 희석액 100 μL를 nutrient agar(Difco)에 접종하였다. 배양기 에서 37℃, 24시간 배양한 다음 형성된 colony 수를 계측하 고 colony에 희석배수를 곱하여 시료 mL당 colony forming unit(CFU)로 나타내었다.
Protease 활성은 Kunitz법(14)을 변형하여 측정하였으며, 아마란스 발효물을 원심분리 후 여과한 상등액을 조효소액 으로 사용하였다. 시료 0.5 mL와 50 mM sodium phosphate 완충용액(pH 7.0)을 이용한 0.6% casein 용액(w/v, Duksan pure chemicals) 0.5 mL를 가하고 진탕 항온수조(BS-31, Jeio tech, Seoul, Korea)를 이용하여 37℃, 100 rpm 에서 30분간 반응시킨 후 0.44 M trichloroacetic acid(Acros organics, Geel, Belgium) 1 mL를 넣어 37℃에서 30분간 반응을 중지 시키고 반응액을 원심분리기(1236MG, GYROZEN Co., Daejeon, Korea)를 이용하여 3,000 rpm에서 10분간 원심분 리 하였다. 상등액 1 mL를 취하여 0.55 M sodium carbonate anhydrous(Duksan pure chemicals) 2.5 mL와 1/3 희석한 Folin Ciocalteu 용액(Sigma-Aldrich Co., St. Louis, MO, USA) 0.5 mL를 가하여 37℃에서 30분간 발색반응을 시킨 다음 분광광도계(Ultraspec-2100pro, Amersham Co., Uppsala, Sweden)로 660 nm에서 흡광도를 측정하였다. Protease 활 성은 tyrosine(Sigma-Aldrich Co.)을 정량하여 작성한 표준 곡선으로부터 계산하였으며, 활성단위(unit)는 1분당 1 μg 의 tyrosine을 생성하는 효소의 양으로 정의하였다.
총 폴리페놀함량 및 총 플라보노이드 함량은 아마란스 발효물 동결건조분말 0.2 g에 증류수 10 mL를 가하여 원심 분리 후 여과한 상등액을 시료로 이용하였다. 총 폴리페놀 함량은 Folin-Denis(15) 방법에 따라 시료 1 mL에 1 N Folin-Ciocalteu regent를 혼합하고 20% Na2CO3 0.5 mL를 첨가하여 실온에서 30분간 반응시킨 후 분광광도계 (Ultraspec 2100pro, Amersham Co., Uppsala, Sweden)를 이 용하여 725 nm에서 흡광도를 측정하였다. 이 때 총 폴리페 놀 함량은 tannic acid(Sigma-Aldrich Co., St. Louis, MO, USA)를 정량하여 작성한 표준곡선에 의하여 함량을 계산 하였다.
총 플라보노이드함량은 Jimenez 등(16)의 방법을 응용하 여 시료 100 μL에 1 mL diethyl glycol을 혼합하여 실온에서 5분간 반응 시킨 후 0.1 N NaOH 200 μL와 혼합하여 37℃에 서 1시간 반응시키고 420 nm에서 분광광도계로 흡광도를 측정하였다. 총 플라보노이드 함량은 rutin(Sigma-Aldrich Co., St. Louis, MO, USA)을 정량하여 작성한 표준곡선에 의하여 계산하였다.
총 단백질 함량 및 총 당 함량은 아마란스 발효물 동결건 조 분말에 증류수를 가하여 원심분리 후 여과한 상등액을 시료로 이용하였다. 총 단백질 함량은 Lowry 등(17)의 방법 으로 측정하였으며 BSA(bovine serum albumin, Sigma- Aldrich Co., St. Louis, MO, USA)를 정량하여 작성한 표준 곡선으로부터 계산하였다.
총 당 함량 분석은 Saha와 Brewer(18)의 방법에 따라 phenol-sulfuric acid법으로 실시하였다. 즉 5% phenol (w/v) 1 mL와 sulfuric acid 5 mL를 시료 1 mL와 반응시킨 후 분광광도계(Ultraspec 2100pro, Amersham Co., Uppsala, Sweden)를 사용하여 525 nm에서 흡광도를 측정하고 glucose(Sigma-Aldrich Co., St. Louis, MO, USA)를 정량하 여 작성한 표준곡선으로부터 계산하였다.
유리아미노산은 시료 0.2 g에 80% ethanol 20 mL를 가하 여 24시간 교반한 뒤 원심분리(4,000×g, 15분)하여 상층액 과 침전물을 분리하였다. 분리된 상층액을 45℃에서 감압 농축하였으며 농축한 시료는 0.02 N HCI 3 mL로 정용한 후 0.4 μm membrane filter로 여과하여 아미노산 자동분석기 (L-8900, Hitachi Co., Tokyo, Japan)로 분석하였다.
전자공여능은 Biois(19)의 방법에 따라 1,1-diphenyl- 2-picrylhydrazyl(DPPH)의 환원력을 이용하여 측정하였다. 즉, DPPH 용액은 DPPH 12 mg을 absolute ethanol 100 mL에 용해한 후 dH2O 100 mL 첨가하여 제조하였다. 아마란스 발효물 동결건조 분말을 증류수로 10배 희석하여 원심분리 한 상등액 시료 0.5 mL에 DPPH reagent 5 mL를 혼합하여 실온에서 15분간 반응시킨 후 분광광도계로 흡광도를 측정 하고 아래와 같이 계산하였다.
S : absorbance of sample at 517 nm
SB : absorbance of sample blank at 517 nm
C : absorbance of control at 517 nm
FRAP(ferric reducing antioxidant power) 측정은 Benzie와 Strain(20)의 방법에 따라 다음과 같이 측정하였다. FRAP reagent는 25 mL acetate buffer(300 mM, pH 3.6)를 37℃에서 가온한 후, 40 mM HCl에 용해한 10 mM 2,4,6-tris(2- pyridyl)-s-triazine(TPTZ, Sigma-Aldrich Co., St. Louis, MO, USA) 2.5 mL와 20 mM ferric chloride(FeCl3) 2.5 mL를 첨가 하여 제조하였다. 원심분리 한 시료 상등액 30 μL에 제조된 FRAP reagent 900 μL와 증류수 90 μL를 넣은 후 37℃에서 10분간 반응시킨 후 분광광도계를 이용하여 510 nm에서 흡광도를 측정하였다. FRAP는 FeSO4·7H2O(Sigma-Aldrich Co., St. Louis, MO, USA)을 정량하여 작성한 표준곡선으로 부터 계산하였다.
환원력은 Oyaizu(21)의 방법에 따라 다음과 같이 측정하 였다. 원심분리 한 시료 상등액 1 mL에 0.2 M phosphate buffer(pH 6.6) 2.5 mL와 1% potassium ferricyanide 용액 2.5 mL를 가한 후 50℃에서 30분간 반응시켰다. 반응 후 10% trichloroacetic acid 용액 2.5 mL를 가한 후 원심분리한 뒤, 상등액 2.5 mL에 증류수 2.5 mL와 0.1% FeCl3용액 0.5 mL를 가한 후 분광광도계를 이용하여 700 nm에서 흡광도 를 측정하였다.
α-Glucosidase 저해활성은 Watanabe 등(22)의 방법에 따 라 측정하였다. 원심분리 한 시료상등액 60 μL에 0.2 unit/mL α-glucosidase 효소액 50 μL, 0.1 M potassium phosphate buffer(pH 6.8) 50 μL를 혼합하여 37℃에서 20분 동안 전배양 한 후 3 mM ρ-nitrophenyl α-D-glucopyranoside (ρNPG) 50 μL를 첨가한 다음 37℃에서 20분간 반응시키고 0.1 M sodium carbonate 500 μL로 반응을 정지시켰다. 405 nm에서 흡광도를 측정하고 시료용액과 동량의 완충용액을 넣은 대조군을 기준으로 효소 저해활성을 아래의 식으로 계산하였다.
S : absorbance of sample at 405 nm
SB : absorbance of sample blank at 405 nm
C : absorbance of control at 405 nm
ACE(angiotensin converting enzyme) 저해활성은 Cushman 와 Cheung(23)의 방법을 일부 변형하여 측정하였다. 조효소 액은 rabbit lung acetone powder(Sigma-Aldrich Co., St. Louis, MO, USA)를 0.3 M NaCl을 함유한 0.1 M sodium borate buffer(pH 8.3)에 1 g/10 mL (w/v)의 농도로 4℃에서 24시간 추출한 다음, 4℃, 10,000 rpm으로 30분간 원심 분리 하여 상등액을 ACE 조효소액으로 사용하였다. 기질은 0.3 M NaCl을 함유한 0.1 M sodium borate buffer(pH 8.3)에 12.5 mM HHL(hippuril-L-histhdine-L-leucine, Sigma-Aldrich Co., St. Louis, MO, USA)로 녹여 기질로 사용하였다. ACE 저해활성은 원심분리한 시료 상등액 10 μL와 0.1 M sodium borate buffer(pH 8.3) 45 μL에 기질을 100 μL 첨가한 후, 37℃에서 30분간 반응시켰다. 반응 후 1 N HCI 250 μL를 사용하여 반응을 정지시키고 ethyl acetate 1.5 mL를 가하여 30초간 교반하여 3,000 rpm으로 5분간 원심분리 한 후 상등 액 1 mL를 취하였다. 이 상등액을 120℃에서 완전히 건조 시킨 후 증류수 1 mL를 넣어 용해시키고 228 nm에서 흡광 도를 측정하였다. 이때 ACE 저해활성은 시료첨가구와 무 첨가구의 흡광도 차이를 비교하여 백분율로 나타내었다.
S : absorbance of sample at 228 nm
SB : absorbance of sample blank at 228 nm
C : absorbance of control at 228 nm
결과 및 고찰
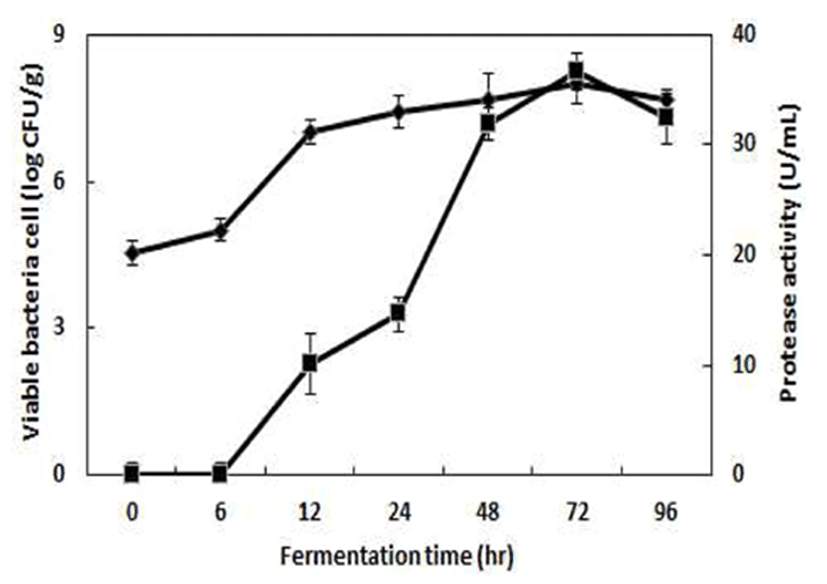
청국장으로부터 분리된 B. amyloliquefaciens 중 우수한 protease 활성을 가지는 B. amyloliquefaciens CGD3를 이용 하여 아마란스 분말을 발효한 다음 미생물 생장에 미치는 영향을 검토하기 위하여 96시간 발효 후 배양시간별 생균 수 및 protease 활성을 측정한 결과는 Fig. 1과 같다. 아마란 스 발효물의 생균수는 초기 0시간에서 4.54 log CFU/mL였 으며, 발효 12시간 이후에는 7.01 log CFU/mL 수준으로 0시간에 비해 2 log 이상 증가하였고 그 이후 발효시간에 따라 증가하여 72시간에서 8.01 log CFU/mL로 가장 높게 나타났다. Yang 등(24)의 연구에서 B. subtilis CBD2를 이용 한 곡류 발효물의 배양특성에서 미생물들이 곡류를 자기 증식에 효과적으로 이용함에 따라 96시간 발효하였을 때 6.89 log CFU/mL로 생균수가 증가하였다고 보고하여 본 연구결과와 유사하였다. 또한, 0~6시간 아마란스 발효물의 protease 활성은 측정되지 않았으며, 12~96시간 발효 시 10.12~36.70 unit/mL 증가하여 72시간 배양하였을 때 최대 로 높은 protease 활성을 나타내었고 이후부터는 감소하는 경향을 보였다.
아마란스 발효물의 총 폴리페놀 및 총 플라보노이드 함 량은 Table 1과 같다. 총 폴리페놀 함량은 0시간에서 412.14 mg/100 g으로 나타났으며, 12시간 이상 발효하였을 때 558.90 mg/100 g으로 0시간에서 보다 총 폴리페놀 함량이 35.61% 증가하였다. 발효시간이 증가할수록 총 폴리페놀 함량은 유의적으로 증가하는 경향을 나타냈으며, 96시간 발효하였을 때 582.07 mg/100 g 함량을 나타내었다. 아마란 스 발효물의 총 플라보노이드 함량은 아마란스 0시간에서 180.56 mg/100 g이었으며 발효 6시간까지는 유지되다가 12시간 발효하였을 때 254.95 mg/100 g으로 발효 초기에 비해 40.38% 증가하였다. 발효시간이 증가할수록 유의적 으로 증가하는 총 폴리페놀 함량 변화와 유사한 경향이었으 며, 총 폴리페놀 및 플라보노이드는 72시간 발효 하였을 때 각각 627.99 mg/100 g 및 442.32 mg/100 g으로 가장 높은 함량을 나타내었다. 이는 발효과정 중에 미생물 또는 가열반응에 의해 phenol ethyl 유도체 및 vinyl 유도체가 생성되어 폴리페놀 및 플라보노이드 함량이 증가한다는 연구(25)와 유사한 경향을 나타내었다.
아마란스 발효물의 총 단백질 및 총당 함량은 Table 2와 같다. 0시간 구간에서 0.09 g/100 g의 단백질 함량을 나타내 었고 아마란스 발효 시간이 증가할수록 단백질 함량이 높아 지는 경향을 보였으며 96시간 아마란스 발효 시 0.25 g/100 g으로 가장 높은 함량을 나타내었다. 이는 Ahn 등(26)이 비 발효 동충하초 분말보다 발효 동충하초 분말에서 단백질 농도가 약 2배 높게 나타났으며, Bacillus, Aspergillus와 같 은 미생물 유래 단백질 분해효소 분비에 의해 단백질 함량 이 증가하였다고 보고되어 본 연구에서도 protease 생산 균주인 B. amyloliquefaciens CGD3를 이용하여 발효함으로 써 단백질 함량이 증가 한 것이라 사료된다.
총 당 함량은 0시간에서 2,816.67 mg/100 g이었고 아마란 스 분말을 24시간 발효하였을 때 2,102.73 mg/100 g으로 0시간에서 보다 33.95%감소하였고, 48시간 발효 시 당 함량 이 1,643.31 mg/100 g까지 감소하였으며 48시간 발효 시간 이후에는 급격한 감소는 관찰되지 않았다. 이는 발효 중 환원당이 미생물의 작용으로 lactic acid, acetic acid 및 그 외 여러 물질들로 변하거나 미생물이 당을 분해해서 에너지 원으로 이용함으로써 환원당 함량이 감소한다는 보고 (27,28)와 유사한 경향을 보였으며, 본 연구에서 아마란스 를 시간별 발효과정을 거치면서 저분자의 단당류나 이당류 를 에너지원으로 이용한 것으로 사료된다.
아마란스는 균형잡힌 아미노산을 구성하고 있어 bioactive properties가 높아 다양하게 이용될 수 있는 새로운 곡물로 인식되고 있다(29). 아마란스를 발효함으로써 변화하는 유 리아미노산을 확인하고자 발효시간에 따른 아마란스 발효 물의 유리아미노산을 분석 하여 Table 3에 나타내었다. 실 험구 0시간에서의 유리아미노산 함량은 119.49 mg/100 g이 었으며 그 중 필수아미노산 함량은 62.49 mg/100 g으로 총 유리아미노산의 52.30%를 차지하였다. 발효시간이 증가함에 따라 유리아미노산 함량은 증가하는 경향을 나타내 었다. 또한 96시간 아마란스 발효물에서 유리아미노산 함 량은 886.94 mg/100 g으로 가장 높은 함량을 나타내었으며 필수아미노산 함량은 517.54 mg/100 g으로 유리아미노산 함량의 58.35%를 차지하였다. 발효 후 유리아미노산 중 leucine이 126.67 mg/100 g으로 가장 높게 나타내었고, valine 102.37 mg/100 g, phenylalanine 94.27 mg/100 g, isoleucine 70.02 mg/100 g 등의 함량 순이었다. Kim 등(30) 은 볏짚을 이용하여 제조한 청국장 발효제품의 유리아미노 산 함량이 원료콩의 것보다 많았다고 보고하여 본 실험과 유사한 경향을 나타내었으며, 아마란스 또한 발효를 통해 유리아미노산 함량이 증가한 것으로 사료된다. 식품으로 섭취된 단백질 등의 아미노산은 흡수된 후 생체 단백질을 합성하는 재료가 되는데 생체 단백질은 20여종이 일정한 순서에 따라 결합 및 합성되므로 그 중 1종류의 아미노산 이라도 부족하면 생체 단백질은 합성될 수 없다. 특히 isoleucine, leucine, lysine, phenylalanine, methionine, threonine, tryptophan, valine 등의 아미노산은 인간의 체내에서 합성 되지 않거나 합성되어도 수요량을 충족시키지 못하는 필수 아미노산으로 음식물을 통해서 필요량을 공급해 주어야만 하는 아미노산이다. 본 연구에서는 발효를 통해 필수아미 노산의 함량이 상당히 증가하여 아마란스 발효물을 식품소 재로 이용할 경우 영양학적 가치가 높을 것으로 판단된다.
아마란스 발효물의 전자공여능, FRAP 및 환원력은 Table 4에 나타내었다. 전자공여능을 분석한 결과 발효시간 이 증가함에 따라 전자공여능이 증가하였으며 아마란스 72시간 발효물이 84.46%로 가장 높은 활성을 나타내었다. 이는 발효 전에 비해 29% 정도 증가하였고 양성대조군인 ascorbic acid와 유사한 전자공여능을 나타내었다. FRAP를 분석한 결과 실험구 0시간에서 325.10 μM 으로 가장 낮은 활성을 나타내었고 72시간 발효물에서 551.91 μM로 가장 높은 FRAP 함량을 나타내었다. 환원력을 분석한 결과 아마 란스의 발효가 진행되지 않은 0시간에서 2.07로 가장 낮은 환원력을 나타내었고 72시간 발효물이 2.74로 가장 높은 환원력을 나타내었다. Kim 등(31)은 발효 미생물에 따른 포도가공 부산물의 항산화 활성을 나타낸 결과에서도 발효 한 포도박이 발효하지 않은 포도박의 대조군에 비해 높은 활성을 나타내었다고 보고하였는데, 이는 폴리페놀 화합물 함량과 관련이 있다고 보고하였다. Kang와 Kim(32)은 phenolic acid의 일종인 caffeic acid, p-courmaric acid 등과 flavonoid 일종인 catechin, quercetin, catechol 및 chlorogenic acid를 포함한 기타 페놀성 물질이 전자공여능에 관여하는 것으로 보고하여 본 연구에서 발효시간에 따른 항산화 활성 의 증가는 발효시간에 따라 phenolic acid와 flavonoid 함량 의 증가로 인한 것으로 사료된다.
식품으로부터 섭취한 다당류는 α-amylase에 의해 이당류로 분해되고, 최종적으로 α-glucosidase가 이당류를 단당류 로 분해함으로써 소장의 융털로 흡수된 후 혈관으로 이동되 므로, 이당류 분해 효소인 α-glucosidase의 저해활성은 당질 가수분해와 흡수를 지연시켜 식후 혈당농도가 급격하게 증가되는 것을 억제한다고 보고되고 있다(33). 본 연구에서 는 아마란스 발효시간에 따른 발효물의 α-glucosidase 저해 활성을 Fig. 2에 나타내었다. 아마란스를 0~72시간 발효하 였을 때 α-glucosidase 저해활성이 유의적으로 증가하다가 72시간 발효 시 81.41%로 가장 높은 저해활성을 나타내었 으며, 발효 96시간부터 감소하는 경향을 보였다.
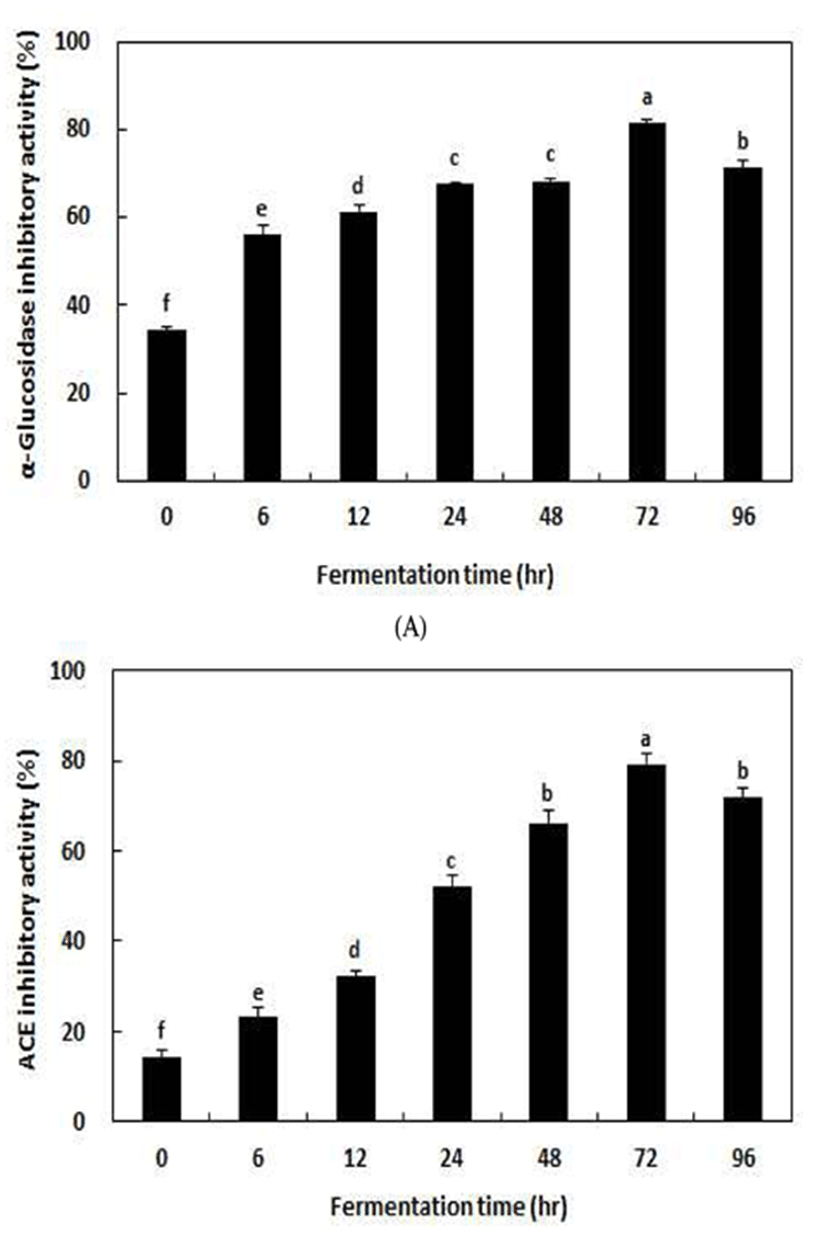
ACE(angiotensin coverting enzyme)는 renin에 의하여 생 성된 angiotensin Ⅰ으로부터 C- 말단 dipeptide(His- Leu)를 가수분해 시킴으로써 강력한 혈관수축작용을 나타내는 angiotensin Ⅱ를 생성한다. Angiotensin Ⅱ는 결과적으로 혈압을 상승시키므로, ACE 활성 저해를 통하여 혈관벽의 파괴나 뇌졸중 등의 질환 발생을 억제 할 수 있다. 본 연구에서는 protease 생산 균주인 B. amyloliquefaciens CGD3를 아마란스에 접종하여 발효시간에 따른 발효물의 ACE 저해 활성을 측정한 결과 발효시간이 증가할수록 ACE저해활성 이 증가하는 경향을 보였으며 72시간 발효하였을 때 발효 하기 전보다 5배 이상 증가하여 79.09%의 높은 저해활성을 보였다(Fig. 2). Jung 등(34)의 연구 결과, 발효시간이 길어짐 에 따라 높은 ACE 저해활성이 나타냈는데 본 연구와 일치 하는 경향을 나타내었다. 일반적으로 대두 등 일부 식품 성분 중의 단백질이 protease에 의해 가수 분해되어 유용 펩타이드를 생성시킴에 따라 ACE 저해활성을 나타낸다고 보고(35)되어 본 연구에서도 단백질이 가수분해되면서 발 효시간에 따라 ACE 저해활성이 증가한 것으로 사료된다.
요 약
청국장으로부터 분리된 B. amyloliquefaciens CGD3를 이 용하여 아마란스를 발효하였으며 발효시간에 따른 발효물 의 이화학적 특성 및 생리활성을 조사하였다. 아마란스 발 효 0시간에서의 생균수는 4.54 log CFU/mL로 나타났으며 72시간 발효물에서 8.01 log CFU/mL로 가장 높은 생균수를 나타내었고, protease 활성은 72시간 배양하였을 때 36.70 unit/mL로 가장 높았다. 총 폴리페놀 및 총 플라보노이드 함량은 발효시간이 증가함에 따라 증가하여 72시간 발효 시 각각 601.12 mg/100 g 및 442.32 mg/100 g으로 가장 높았으며 72시간 이후부터 감소하는 경향을 보였다. 총 단 백질 함량은 발효시간이 증가할수록 증가하여 96시간 발효 시 0시간 보다 2.7배 단백질 함량이 증가하였으며, 총 당 함량은 발효 12시간 이후부터 급격히 감소하는 경향을 보 였다. 유리아미노산 함량은 발효시간이 증가할수록 증가하 였는데 0시간에서 119.49 mg/100 g이었고 96시간 발효시 886.94 mg/100 g으로 증가하였다. 전자공여능, FRAP 및 환원력은 72시간 발효구간에서 각각 84.46%, 551.91 μM 및 2.74로 가장 항산화활성이 우수하였다. α-glucosidase 저 해활성 및 ACE 저해활성은 발효 72시간 구간에서 각각 81.41% 및 79.09%의 저해활성을 나타내어 발효최적 시간 임을 확인하였다.










