서 론
우리나라에서 즐겨먹는 수산가공품인 멸치는 일시 다획 성의 어류로 대부분이 염장품인 젓갈이나 건제품인 마른 멸치로 가공되고 있으며, 특히 마른 멸치는 조직 중의 자가 소화 효소를 실활시키고 부착 미생물의 사멸, 육단백질의 응고로 건조를 용이하도록 한 자건품의 형태가 총 생산량의 90%를 차지한다(1). 또한 멸치는 육질이 연하고 자가소화 효소 활성이 높아 단기간에 선도저하가 진행되므로 멸치 가공에 어려움이 크며, 처리시설 부족으로 사료화되는 경 향이 크다(2). 더욱이 다양한 유용 물질이 많아 경제적으로 나 환경적인 면에서 볼 때 높은 이익을 창출할 수 있어 유용물질의 효율적인 이용을 위한 대안이 요구된다. 따라 서 멸치의 가공 전 단계에서 품질열화를 감소시킬 수 있는 시스템의 마련이나, 저장 및 유통과정 중 지질 산화 등의 품질 저하에 대한 개선책 및 유용물질을 이용한 새로운 가공품으로 개발 등이 지속적으로 요구되고 있다.
멸치의 대표적인 유용물질인 칼슘은 타 영양소에 비해 흡수율이 낮아 최대 60% 미만이며 성인의 경우 체내 흡수 가 25~30% 수준으로 칼슘의 장내 흡수가 제한되는데(3), 섭취하는 식품 중 칼슘의 총량이나 생체 이용 효율이 칼슘 의 급원의 이용 효율성을 결정하는 중요 요인이 되고 있다 (4). 이와 같이 멸치는 칼슘의 급원으로써 대표적인 식품으 로 인지되고는 있으나, 통멸치로써의 섭취량에는 다소 한 계가 따른다.
최근 전기 분해수를 이용한 식품의 살균은 인체에 무해 한 살균기술로 부각되어 과일이나 채소의 신선도 유지, 살 균력 향상 및 유해 잔유물이 없어 인체에 해를 끼치지 않는 다는 장점에 의해 식품 가공에 폭넓게 적용되고 있다(5,6). 주로 배추, 양배추, 케일 등의 잎채소에 처리할 경우 표면 세정과 살균 효과를 동시에 얻을 수 있으며(7), 수산 가공현 장에서는 도마와 마쇄기의 세정과정에서 살균효과가 있다 는 것이 보고된 바 있다(8). 또한 어획 직후의 오징어를 산성 전해수 얼음으로 빙장한 결과 수도수 얼음의 사용에 비해 저장 중 휘발성 염기질소의 함량 증가가 작았으며, 오징어 표면의 명도 값이 높았다는 보고도 있다(9).
수산물의 가공 시 원재료의 색택 유지와 비린내 제거 등은 품질유지와 관련하여 중요한 문제로 지적되고 있는 데, 지금까지 산성 전해수가 채소류의 살균에 주로 사용되 어온 바 수산물에 대한 이용은 상당히 제한적이었으며, 멸 치의 자숙과정 시 산성 전해수의 사용에 관한 연구는 부족 한 실정이다. 이에 본 연구는 자건 멸치의 가공 시 산성 전해수로 자숙하므로서 멸치의 표면색 및 지질산화 정도를 측정하여 산성 전해수 처리에 의한 자건 멸치의 품질 개선 에 미치는 영향을 분석함으로써 향후 수산 가공품 제조 시 산성 전해수 처리에 대한 가능성을 제시하고자 하였다.
재료 및 방법
마른 멸치는 경남 남해군 ‘홍성수산’에서 제조한 것을 사용하였으며, 멸치의 자숙과정에서 수도수를 사용하여 자 숙 후 건조한 멸치를 대조구로 하였으며, 산성 전해수를 사용하여 자숙한 것을 산성 전해수 처리구로 하였다. 산성 전해수는 일반 수도수에 NaCl을 첨가하여 전기 분해조에서 전기분해하여 얻은 것으로(10), 이때 수도수의 pH는 6.10, 산성 전해수의 pH는 3.04였다. 멸치는 어획 직후 수도수와 산성 전해수가 담긴 자숙조에서 85~95°C로 3~5분간 자숙한 후 21~23°C의 냉풍건조 조건(CT, Cooltop, Cheonan, Korea) 에서 11~12시간 건조시킨 다음 일정 크기(체장: 5.5~6.8 cm, 체중: 1.7~2.5 g)로 선별하여 폴리에틸렌 팩에 100 g씩 넣고 함기 포장하였다. 멸치의 저장 조건은 실온(20°C), 냉 장(4°C) 및 냉동(–20°C) 등의 3가지 조건으로 설정하였으 며, 이에 따른 저장 기간을 고려해 보아 실온(20°C) 저장은 5주, 냉장(4°C) 저장은 10주, 냉동(-20°C) 저장은 5개월 동안 유지하면서 일정기간별로 시료를 채취하여 내장을 제거한 후 균질화(SMX-S1800, SHINIL, Hwaseong, Korea)한 후 40~60 mesh의 분말을 –40°C에 보관하면서 실험에 사용하 였다.
멸치의 일반성분은 AOAC법(11)에 따라 수분 함량은 105°C의 상압가열건조법, 회분 함량은 550°C 직접회화법, 조지방 함량은 soxhlet 추출법, 조단백질 함량은 semimicro Kjeldahl법으로 각각 정량하였다. 시료의 pH는 멸치 분말 10 g에 10배의 증류수를 가하여 30분간 추출한 후 여과액을 pH meter(410, Thermo Orion, Waltham, USA)로 측정하였 다. 염도는 상기의 여과액 10 mL에 10% K2CrO4 용액 1 mL를 혼합하여 0.1 N AgNO3 용액으로 적갈색이 사라지지 않을 때까지 소요된 AgNO3 용액의 양으로부터 산출하 였다.
멸치의 색도는 일정량의 멸치 분말을 취하여 색차계 (CR-301, Minolta Co., Osaka, Japan)로 5회 이상 반복하여 측정하였다. 색도로 명도(lightness)는 L값, 적색도(redness) 는 a값과 황색도(yellowness)는 b값으로 나타내었으며, 시 료간의 전체적인 색차(ΔE)를 비교하였다. 이때 표준색판의 L값은 97.12, a값은 0.73, b값은 0.67이었다.
멸치의 갈색도는 시료 분말에 4배량의 CM(chloroform: methanol=2:1, v/v)용액을 가하여 추출한 후 여과한 여액의 흡광도를 측정하여 지용성 갈색도로 하였으며, 상기의 CM 추출 후 잔사에 4배량의 증류수를 가하여 추출하여 여과한 여액의 흡광도를 수용성 갈색도로 하여 분광광도계 (Optizen 2120UV, Mecasys Co. Ltd., Daejeon, Korea)로 430 nm에서 각각의 추출 용매를 대조로 하여 측정한 흡광도 값으로 나타내었다(12).
멸치의 in vitro에서 칼슘 흡수율은 Miller 등(13)의 방법 에 따라 멸치 분말 10 g에 증류수 400 mL를 가한 후 6 M의 HCl을 가하여 pH 2로 조정한 후 37°C의 수욕상에서 30분간 반응시켰다. 여기에 10% pepsin(425 unit/mg, Sigma Co., St. Louis, MO, USA)용액 6 mL를 가하여 다시 2시간 동안 반응시킨 다음 여과하였다. 비이커에 여과액 20 mL를 취하여 0.1 M NaOH를 가하여 pH 7로 조정한 다음, 투석막 (D9652-100FT, Dialysis tubing cellulose membrane, Sigma Co.)에 증류수, 0.1 M NaOH 및 0.1 M NaHCO3를 각 15 mL씩 혼합하여 밀봉한 후 상기의 비이커에 담근 후 비이커 를 밀봉시켜 37°C의 수욕상에서 반응시켰다. 30분 경과 후 0.1 M NaHCO3로 용해한 2.5%의 bile salts 용액에 0.4 g의 pancreatin을 혼합한 용액 5 mL를 비이커 내에 첨가하고 다시 3시간 동안 상기와 동일하게 반응시켰다. 반응이 끝난 후 투석막내의 투석액을 회수하여 Chung 등(14)의 방법에 따라 진한 황산과 질산으로 분해한 후 Inductively Coupled Plasma(ICP, Optima 3300DV, Perkin-Elmer Co., Melville, NY, USA)로 칼슘의 함량을 정량하였으며, 투석 전·후의 칼슘 함량을 비교하여 칼슘 흡수율(%)로 계산하였다.
휘발성 염기질소(volatile basic nitrogen, VBN) 함량은 멸 치 분말 5 g에 증류수를 가하여 100 mL로 정용한 후 30분간 추출하여 여과하였다. Conway unit 내실에 0.01 N H3BO3 용액 1 mL와 지시약(0.066 g methyl red + 0.033 g bromocresol green in 100 mL ethanol solution)을 넣고, 외실에는 시료 여과액 1 mL 및 50% K2CO3 1 mL를 주입한 후 밀폐시킨 다음 37°C에서 90분간 반응시켰다. 반응이 끝난 후 내실의 H3BO3 용액을 0.02 N H2SO4 용액으로 적정하여 VBN 함량 을 계산하였다(15).
멸치 분말 5 g에 butylated hydroxytoluene(BHT) 50 μL 및 증류수 15 mL를 가한 후 2 mL thiobarbituric acid(TBA) /trichloroacetic acid(TCA) 혼합용액을 넣어 혼합한 다음 9 0°C의 항온 수조에서 15분간 열처리 후 냉각시켜 3,000 rpm 에서 10분간 원심분리(Mega 17R, HANIL, Incheon, Korea) 하였다. 상층액을 회수하여 531 nm에서 분광광도계 (Optizen 2120UV, Mecasys Co. Ltd.)로 흡광도를 측정하였 다. 이때 생성된 malondialdehyde 함량을 표준물질인 1,1,3,3-tetraethoxypropane(TEP)에 의한 표준 검량선에 의 하여 계산하였다.
결과 및 고찰
산성 전해수로 자숙한 전해수 처리 멸치의 이화학적 특 성을 대조구와 비교한 결과는 Table 1과 같다. 대조구와 전해수 처리 멸치간에 수분과 단백질 함량은 유의차가 없었 으나, 회분 함량과 염도는 전해수 처리 멸치, 조지방 함량과 pH는 대조구에서 통계적인 유의차에 의해 높았으나, 큰 차이는 아니었다. 특히 전해수 처리 멸치의 자숙과정에 사 용된 산성 전해수의 pH가 3.04인 것을 고려해 볼 때 자숙용 물의 pH에는 상당한 차이가 있었으나, 멸치 시료간에는 차이가 적어 전해수 자체의 pH가 자건 멸치제품의 pH에는 영향을 미치지 않는 것으로 판단된다.
국내산 마른 중멸치의 수분 함량은 25.2%, 회분은 14.8%, 조지방은 8.2%, 조단백질은 51.5%, 염도는 5.8%인 것으로 보고된 바 있는데(16), 본 연구결과 회분 함량과 염도는 상기 보고에 비해 다소 낮은 값이었다. 또한 자건 멸치의 수분은 15.6%, 소건 멸치는 17.5%로 어체의 크기에 관계없 이 소건 멸치에서 수분함량이 더 높았으며, 단백질은 55.9~58.8%, 조지방은 10.9~11.0%로 보고된 바 있는데, 이 는 수분을 제외한 성분에서 본 연구 결과보다 다소 높은 함량으로 시료 중 수분에 따른 상대적인 함량차이인 것으로 사료된다. 더욱이 멸치의 자숙과정에서 녹차를 함유한 물 의 사용은 자건 멸치의 일반성분에는 유의적인 차이를 보이 지 않았다는 보고(17)는 본 연구와 유사한 결과였다. 따라서 전해수 처리 멸치는 이화학적 특성면에서 대조구와 두드러 진 차이를 보이지 않아 자숙과정에서 전해수 처리가 자건 멸치의 품질에 큰 영향을 주지 않는 것으로 예상된다.
멸치의 색도는 시료의 표면색과 추출물의 갈색도로 각각 측정하였다. 멸치의 표면색은 전해수 처리 멸치에서 명도 값이 유의적으로 높아 표면색이 밝은 것으로 판단되었으 며, 적색도 값은 대조구에서 2.4배 높았으며, 황색도 값은 시료간에 유의차를 보이지 않았다. 전체적인 색차(ΔE)는 대조구에 비해 전해수 처리 멸치에서 5.08의 차이를 보였는 데, ΔE값의 변화를 NBS(National Bureau of Standards)의 기준에서 검토할 경우 대조구의 색을 “0”로 하였을 때 색차 가 3.0~6.0 범위일 경우 현저한 차이로 보고되어 있어(18), 본 연구 결과 전해수 처리 멸치는 대조구에 비해 표면색에 서 뚜렷한 차이를 보이는 것으로 판단된다.
멸치 추출물을 지용성 및 수용성 추출물로 구분하여 갈 색도를 측정한 결과, 지용성 갈색도는 전해수 처리 멸치에 서 유의적으로 높았으나, 시료간에 큰 차이는 아니었고, 수용성 갈색도는 시료간에 유의차를 보이지 않았다.
자건 샛줄멸치의 지용성 및 수용성 갈색도가 각각 0.26 및 0.01이었다는 보고가 있는데(19) 이는 본 연구에서 멸치 의 지용성 갈색도가 수용성 갈색도에 비해 월등히 높았던 것과 일치하는 결과였다. 멸치의 지용성 갈색도가 높은 것 은 멸치가 적색어류이며 지질 함량이 높기 때문으로 추정되 며, 이는 멸치의 저장이나 유통과정 중 지질 성분의 산화에 의한 갈변과도 관련성이 높을 것으로 생각된다(20). 오징어 의 경우 전해수 얼음으로 빙장하였을 때 수도수 얼음으로 빙장한 대조구에 비해 저장 초기에 시료 표면색의 명도 값은 낮았으나, 저장 4일 이후 16일까지 대조구에 비해 명도 값이 높게 유지된 것으로 보고된 바 있다(9). 자건 멸치는 일반적으로 소건 멸치에 비해 자숙과정에 의한 비늘의 탈락 우려가 높아 표면색이 다소 어두워지는 경향이 있는데(21), 본 연구에서 전해수 처리 멸치의 표면색이 대조구에 비해 밝은 것은 산성 전해수에 의한 시료의 탈색에 의한 것으로 추정된다(9). 따라서 전해수로 자숙시킨 자건 멸치제품의 구입 시 시각적인 측면에서 선호도를 증가시키는데 효과적 일 것으로 예상된다.
전해수 처리 멸치를in vitro에서 염산과 펩신으로 소화시 킨 후 투석막을 이용하여 칼슘 흡수율을 측정한 결과는 Fig. 1과 같다. 칼슘의 흡수율은 대조구에서 10.77±0.31%, 전해수 처리 멸치는 12.61±0.43%로 전해수 처리 멸치의 칼슘 흡수율이 유의적으로 높았다.
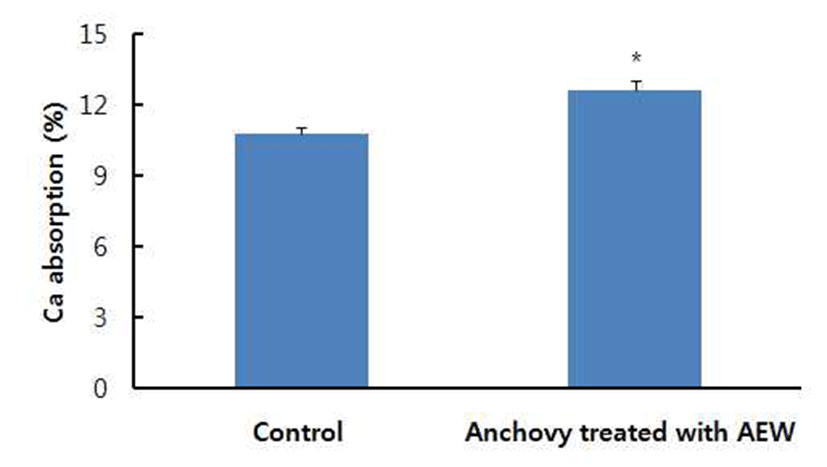
유당, 카제인 포스포펩타이드, 구연산 및 비타민 D 등은 체내 칼슘의 흡수 증진에 도움을 주는 요인으로 알려져 있다(22). 건조 대멸치의 경우 in vitro에서 칼슘 흡수율은 2.9%였는데 구연산을 처리한 경우 칼슘 흡수율이 4.2배 증가되었으며, 이는 흰쥐를 이용한in vivo에서 칼슘 흡수율 측정결과에서도 건조 대멸치는 10.5%, 구연산 처리구에서 는 21.4%로 구연산의 처리가 멸치의 칼슘 흡수율 증가에 효과적이었다는 보고가 있다(23). 반면에 참다랑어 골분은 구연산 처리의 유무에 따른 칼슘 흡수율에서 유의적인 차이 가 없었다고 보고된 바 있다(24). 쌀의 경우, 전해수 처리구 는 무처리구에 비해 수용성 식이섬유소 함량이 다소 높았으 나, 전반적인 영양성분의 함량에 차이를 보이지 않아 전해 수의 처리가 시료의 영양성분의 변화에는 두드러진 영향을 주지 않았다고 보고도 있다(5).
본 연구 결과, 산성 전해수 처리 멸치는in vitro에서 칼슘 흡수율이 대조구보다 높아 산성 전해수 처리가 구연산과 유사한 효과를 내는 것으로 추정되나(23), 명확한 기작에 관해서는 추후 연구가 필요할 것으로 생각된다.
전해수 처리 멸치의 저장 온도 및 기간에 따른 지용성 및 수용성 추출물의 갈색도 변화를 측정한 결과는 Fig. 2 및 3과 같다. 멸치 추출물의 지용성 갈색도는 Fig. 2와 같이 20°C에 저장했을 때, 대조구는 전해수 처리 멸치에 비해 유의적으로 높았으며, 대조구의 갈색도는 저장 1주경에 1.046이었으며, 저장 5주 동안 점차 증가되는 경향이었으며 저장 4주경에는 1.811로 가장 높은 값을 보였다. 전해수 처리 멸치는 1.009~1.174의 범위로 저장기간에 따른 두드러 진 증감현상을 보이지 않았다. 4°C에 저장한 경우 대조구와 전해수 처리 멸치의 지용성 갈색도는 6~8주경 전해수 처리 멸치에서 유의적으로 높았으나, 두드러진 차이는 아니었으 며, 기간의 경과에 따른 증가현상은 20°C에 저장 시와 유사 한 경향이었다. -20°C에 저장 시에는 대조구와 전해수 처리 멸치간에 비슷한 양상이었으며, 기간의 경과에 따른 두드 러진 증가현상을 보이지는 않았다. 따라서 멸치 추출물의 지용성 갈색도는 20°C에 저장한 시료에서 가장 높았으며, -20°C에 저장 시 가장 낮았는데, -20°C에서 5개월 동안 저장 한 시료는 20°C에서 5주 동안 저장한 시료에 비해 대조구는 53%, 전해수 처리 멸치는 41% 정도의 낮은 갈색도 값을 보였다.
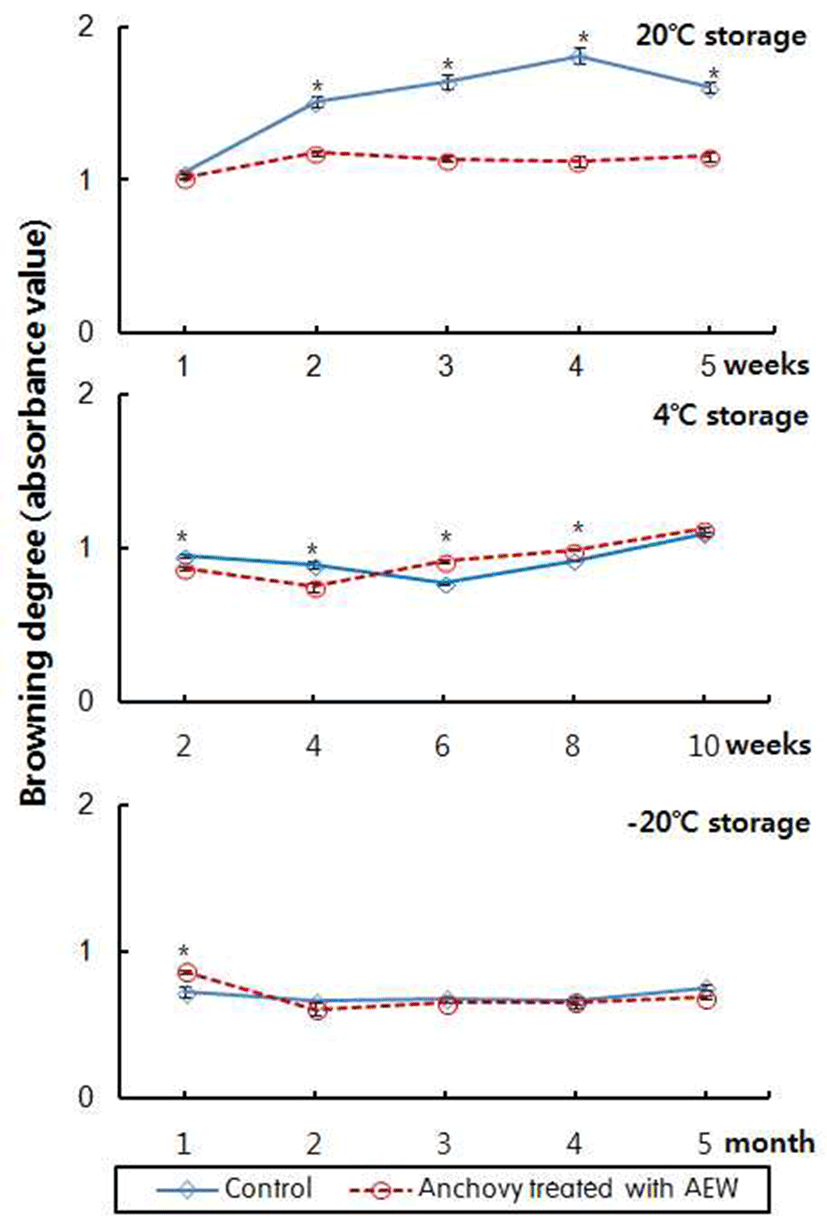
멸치 추출물의 수용성 갈색도는 Fig. 3과 같으며, 지용성 갈색도에 비해서는 월등히 낮은 값으로 모든 시료에서 저장 최종일에도 0.3이하의 값이었다. 20°C에 저장 시 저장 기간 이 경과함에 따라 대조구는 0.091~0.195, 전해수 처리 멸치 는 0.117~0.230의 범위로 시료간에 차이가 작았으나, 저장 5주경에는 전해수 처리 멸치의 갈색도가 다소 높았다. 이러 한 현상은 4°C에 저장한 시료에서도 같은 경향이었으며, –20°C에 저장한 경우에는 시료간에 차이가 작았다.
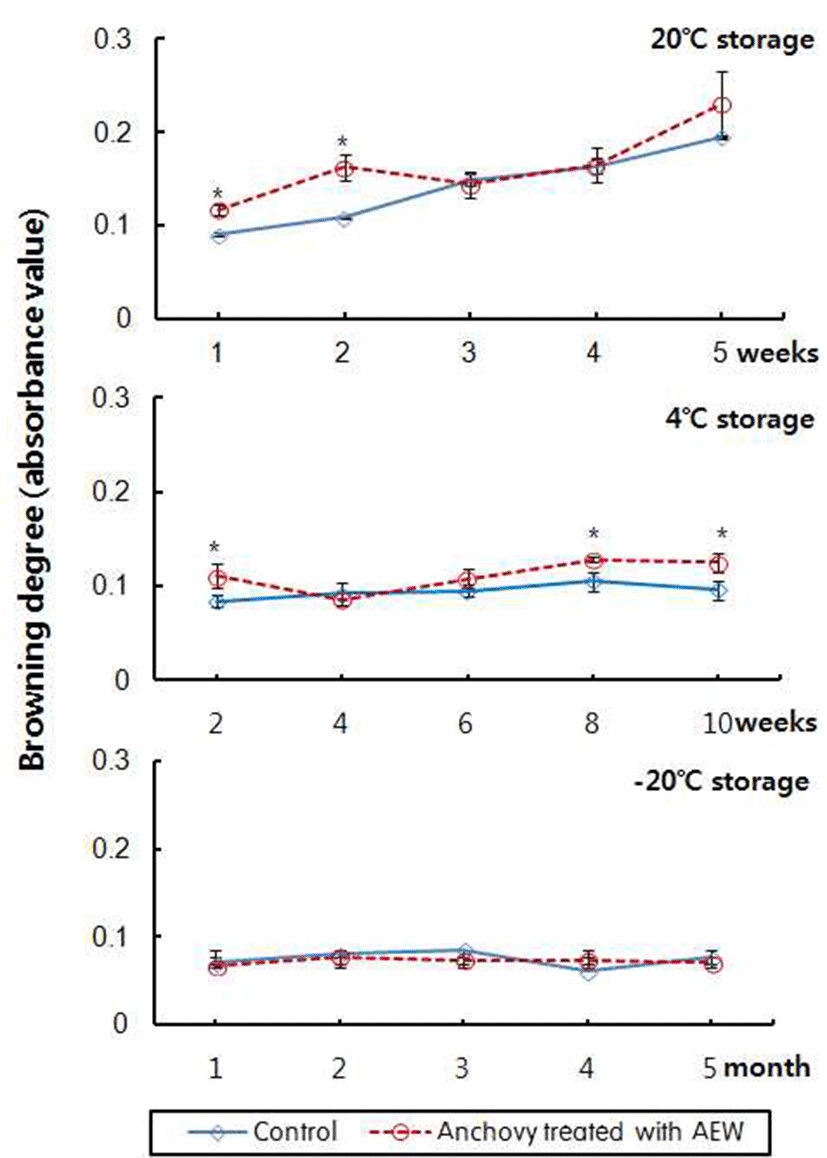
멸치 추출물의 지용성 갈색도가 높은 것은 시료의 지질 산화에 기인되므로 멸치의 저장 및 유통과정 중 진공포장, 탈산소제의 처리가 요구된다는 보고가 있다(20). 실온에 저장한 전해수 처리 멸치의 지용성 갈색도에서 저장기간의 경과에 따른 차이가 작은 것으로 보아 자숙과정 중 멸치 표면의 불순물이나 지질 성분의 제거에 산성 전해수가 관여 하였기 때문이라 추정된다. 녹차 추출물을 처리한 자건 멸 치의 저장성은 분무 처리보다 침지 처리한 경우 효과가 높았는데, 침지 과정이 시료 표면의 이물질 제거에 효과적 이었기 때문이라고 보고되어 있다(25). 또한 신선초의 세척 시 산성 전해수를 사용한 경우에도 분무 처리보다 침지 처리한 경우 일반 세균수를 유의적으로 감소시켜 녹즙의 저장성을 향상시켰다는 보고도 있다(26). 따라서 본 연구 결과 멸치의 자숙과정에서 산성 전해수의 사용은 수도수보 다는 멸치의 저장 중 갈변 반응을 지연시키는데 효과적일 것으로 생각된다.
멸치의 저장 기간에 따른 휘발성 염기질소(VBN)의 함량 을 측정한 결과는 Fig. 4와 같다. 대조구와 전해수 처리 멸치에서 저장 초기 VBN 함량은 12.60 mg%였으나, 저장기 간이 경과함에 따라 점차 증가되는 경향으로 20°C에 저장 시 저장 1주경에는 대조구와 전해수 처리 멸치의 VBN 함량 이 각각 21.49 mg% 및 17.15 mg%였으며 이는 저장 5주 경과 시 57.42 mg% 및 38.15 mg%로 각각 약 2.7배 및 2.2배 증가되었으나, 전해수 처리 멸치는 대조구에 비해서 유의 적으로 낮은 함량이었다. 4°C 저장 시에는 저장 2주경에 전해수 처리 멸치의 VBN 함량이 대조구에 비해 유의적으 로 높았다. -20°C에서는 5개월동안 저장한 경우 기간의 경 과에 따라 멸치의 VBN 함량이 증가되었는데, 저장 4개월 이후에는 대조구에 비해 전해수 처리 멸치에서 유의적으로 낮았으며, 저장 5개월경에는 각각 19.30 mg% 및 14.96 mg% 로 이는 20°C에서 1주 동안 저장된 시료보다 낮은 수준이 었다.
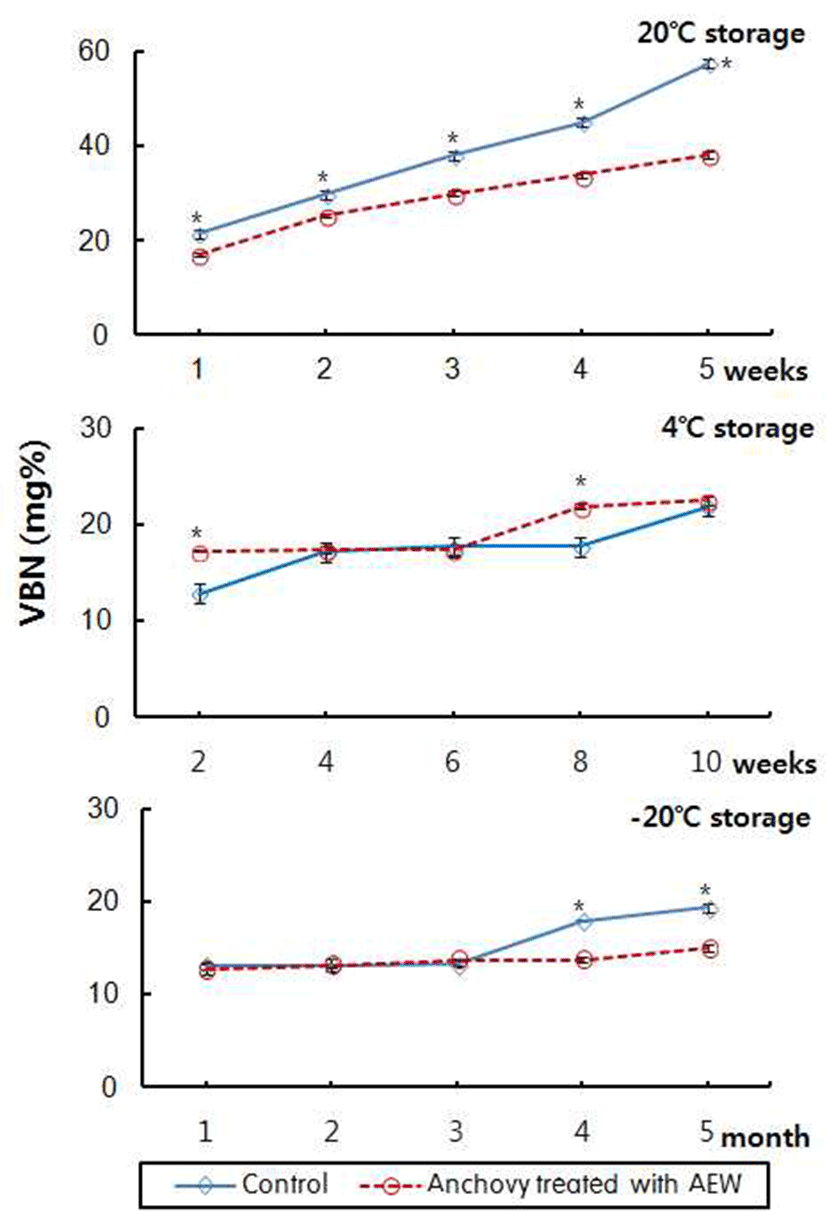
VBN은 어육이나 단백질 함량이 높은 식품이 부패될 때 생성되는 물질로 식품의 신선도 판정의 지표로 활용되며, 신선한 해산 어류가 건어류로 가공될 때 질소 화합물의 분해로 암모니아 및 여러 아민류의 생성에 의해 증가되며 자숙, 건조 등의 가공과정이나 저장 중 어체에 축적되는 것으로 알려져 있다(27). 이러한 단계적인 반응은 저장 온 도, 저장 기간, 미생물의 농도 등에 따라 영향을 받는데(28), 소매시장에서 판매되고 있는 건조 멸치의 VBN 함량은 대 멸치에서 27.43 mg%, 소멸치에서 11.37 mg%로 소매점에 서 판매되는 동안 공기 중의 산소, 미생물 등에 의해 VBN 함량이 빠르게 증가되었기 때문이라 보고된 바 있다(29). 더욱이 멸치의 자숙 과정에서 녹차 추출물의 처리는 멸치의 저장 중 VBN의 함량을 감소시킴으로써 멸치의 풍미 개선 및 저장기간 연장에 효과적이라고 보고되어 있다(25). 담수 얼음과 산성 전해수 얼음으로 오징어를 빙장한 경우 담수 얼음에서는 저장 6일 이후 초기 부패단계에 이르렀으나, 산성 전해수 얼음을 사용한 경우에는 저장 10일 이후에도 신선상태가 유지되었다는 보고가 있는데(9), 산성 전해수 자체의 살균력과 함께 산성 pH영역에서 부패세균의 증식 이 억제되었기 때문이라고 한 보고(30)는 본 연구와도 유사 한 결과라 사료된다.
상기의 결과에서 20°C에 저장한 시료에서 전해수 처리구 의 VBN 함량은 대조구에 비해 유의적으로 낮았는데, 이는 4°C 및 –20°C에 비해 저장 온도가 높아 시료의 변질이 빠르게 진행되는 것을 고려해 본다면 전해수 처리는 초기 저장 안정성에 효과적일 것으로 사료된다. 자건 멸치의 구 매 시 소비자는 주로 관능적인 기호도에 의존하게 되는데, 특히 수산 가공품에서 VBN 함량이 작을수록 선호도가 높 기 때문에(31), 본 연구 결과 전해수 처리 멸치에 대한 선호 도가 대조구에 비해 높을 것으로 예상된다.
자건 멸치의 저장 중 지질과산화물 함량을 측정한 결과 는 Fig. 5와 같다. 저장 초기 지질과산화물 함량은 대조구와 전해수 처리 멸치에서 각각 86.85 μM/100 g 및 73.51 μM/100 g이었는데, 20°C에 저장 시 저장 1주경에 각각 111.21 μ M/100 g 및 104.91 μM/100 g이었으며 저장 5주경에는 194.71 μM/100 g 및 188.11 μM/100 g으로 저장 1주에 비해 약 1.8배 증가되었으나, 유의적인 차이는 아니었으며, 전반 적으로 전해수 처리 멸치가 대조구에 비해 다소 낮은 경향 이었다. 4°C에 저장한 경우는 저장 2주경에 각각 94.42 μ M/100 g 및 94.58 μM/100 g이었는데, 저장 4~6주경에 대조 구가 전해수 처리 멸치에 비해 유의적으로 높았으나, 저장 8주 이후에는 시료간에 유의차가 없었다. -20°C 저장 시에 는 저장 1개월에 비해 저장 5개월에 약 1.4~1.5배 증가되었 으며, 저장 1~2개월경에는 대조구가 전해수 처리 멸치에 비해 유의적인 차이로 높았으나, 저장 3개월 이후에는 시료 간에 유의차가 없었다.
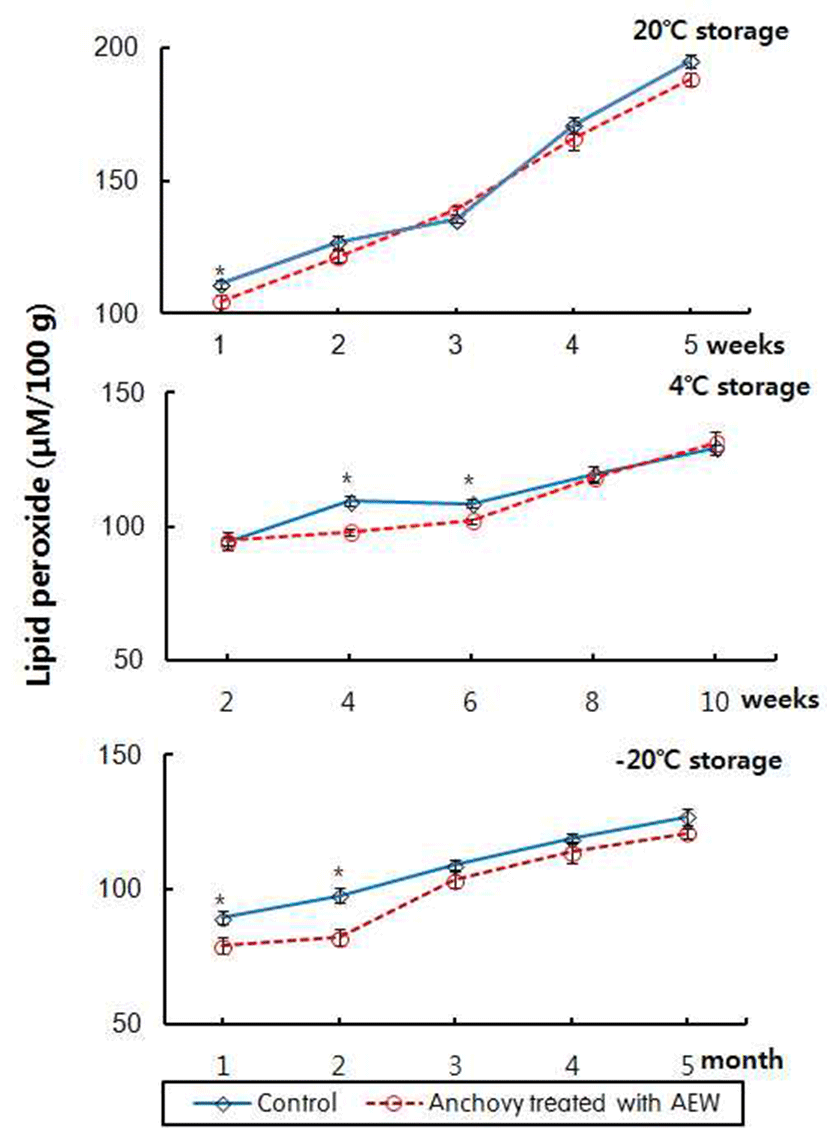
식품에 함유된 지질성분 중 불포화지방산은 산패됨에 따라 carbonyl 화합물의 일종인 malonaldehyde를 생성하는 데, 이는 TBA와 정색반응하여 붉은색의 복합물을 형성하 게 된다(32). Cha 등(33)은 해산 어패류 가공품에서 저장 중 불포화지방산의 산화 생성물인 malonaldehyde가 시료 중의 단백질이나 타 성분과 반응하기 때문에 TBA와의 반 응성이 감소되어 시료 중 지질과산화물 함량이 증가하였다 가 오히려 감소되는 현상을 보인다고 하였다. 본 연구에서 는 4°C에 저장 시 저장 4~6주 동안 지질과산화물 함량의 증가 현상이 다소 완만하였으나, 대부분의 시료에서 저장 기간이 경과됨에 따라 증가하는 경향이었다. 마른 멸치를 -20°C에서 150일간 저장하는 동안 지질과산화물 함량이 증 가되었는데, 이는 멸치에 항산화제로써 녹차 추출물을 분 무한 경우에도 유사한 경향이었으나, 항산화제 처리구는 무처리구에 비해서는 지질과산화물 함량의 증가가 적은 것으로 보고된 바 있다(25).
멸치는 생화학적인 특성상 단백질의 변성이나 지방산화 가 빠르고 특히 지질 성분은 장기간 저장 중 산패되거나 갈변현상을 초래하여 품질열화의 원인이 되므로 건제품의 경우 대부분이 냉동 저장하게 된다(34). 본 연구 결과 대조 구와 전해수 처리 멸치의 특성 차이가 주로 저장 초기에 나타난 것으로 보아 자건 멸치의 제조 과정에서 산성 전해 수를 사용하므로써 저장 초기의 성분변화를 지연할 수 있을 것으로 사료된다.
전기 분해수로 처리한 채소류는 저장 중 부패세균의 증 식 억제, 표면색 및 조직감 유지 등의 효과가 있음이 알려져 있으나, 수산물에 대한 적용은 미흡한 실정이었다. 본 연구 를 결과를 통해 산성 전해수로 자숙한 자건 멸치에서 저장 중 색택의 유지, 저장에 따른 VBN 및 지질과산화물 함량의 증가 지연 등의 효과를 확인함으로써 향후 수산물의 가공 시 산성 전해수의 적용은 저장성 및 안정성 확보에 효과적 일 것으로 기대된다.
요 약
자건 멸치의 제조 시 산성 전해수로 자숙함으로써 멸치 의 품질 개선에 대한 영향을 알아보고자 하였다. 멸치의 표면색은 전해수 처리 멸치에서 명도가 유의적으로 높았으 며, 전체적인 색차(ΔE)에서 전해수 처리 멸치는 대조구에 비해 5.08의 차이를 보였다. 추출물의 갈색도는 지용성 추 출물이 수용성 추출물에 비해 훨씬 높았다. In vitro에서 칼슘 흡수율은 대조구에서 10.77%였으며, 전해수 처리 멸 치는 12.61%였다. 저장 온도(20°C, 4°C 및 –20°C) 및 기간(5 주, 10주 및 5개월)을 달리하여 멸치를 저장하는 동안, 멸치 추출물의 지용성 갈색도는 20°C및 4°C저장 시 저장기간이 경과함에 따라 증가되는 경향이었으며, 20°C 저장 시에 전 해수 처리 멸치에서 유의적으로 낮았다. 휘발성 염기질소 (VBN) 함량은 저장기간이 경과함에 따라 증가되는 경향이 었으며, 20°C 저장 시에 전해수 처리 멸치는 대조구에 비해 VBN의 함량이 작았다. 지질과산화물 함량은 저장 온도에 관계없이 기간의 경과에 따라 증가되었는데, 전반적으로 전해수 처리 멸치에서 함량 증가가 작았다. 따라서 멸치의 가공과정에서 산성 전해수 처리는 멸치의 색택 개선, VBN 및 지질과산화물의 함량 변화를 감소시켜 품질개선이 가능 할 것으로 기대된다.










