서 론
인간이 살아가는데 필요한 에너지는 체내에서 끊임없이 일어나는 생화학적 산화반응을 통해 충족된다. 이때 여러 장기 및 조직에서 세포내로 산소를 받아들이면 미토콘드리 아 내에서 산소 대사과정이 일어나는데 이 과정에서 발생하 는 활성산소는 가장 안정한 형태의 산소인 삼중항산소(3O2) 가 산화·환원과정에서 생성되는 superoxide(1O2-)와 hydroxy radical(·OH)과 같은 짝 짓지 않은 상태의 free radical 및 과산화수소(H2O2)를 통칭한다(1,2). 이런 활성 산소종은 멜 라닌 생성을 촉진시키며 활성산소종과 그 유도체는 생체 내에서 많은 분자, 단백질, DNA 등을 공격하여 세포의 노 화, 변형 등 활성산소에 의해 생성되는 여러 가지 질병들 중 당뇨병의 유병율이 빠른 속도로 증가할 뿐만 아니라 유병 연령이 점차 낮아지고 있어 그 심각성이 대두되고 있다(3). 당뇨병은 고혈당을 특징으로 하는 일련의 대사 질환군으로 삶의 질을 떨어뜨리는 1위 질환으로서 전세계 인구의 3%가 당뇨병으로 고통 받고 있으며, 국내에서도 당뇨병 및 대혈관 합병증, 미세혈관합병증, 당뇨병성 신경 병증 및 신장질환 등과 같은 당뇨병 합병증으로 인한 사망 률이 전체 사인의 네 번째를 차지하는 것으로 보고되고 있다(4-6). 당뇨병은 인슐린 의존형인 제 1형과 인슐린 비의 존형인 제 2형 당뇨로 분류되고 우리나라의 경우 제 2형의 당뇨병 환자가 대부분을 차지하고 있다(7). 이러한 당뇨병 의 치료 및 합병증을 예방하기 위해서는 약물치료, 식이요 법, 운동요법에 의존하여 지속적으로 혈당을 유지할 수 있 도록 관리하는 것이 중요하다. 하지만 현재 약물 복용에 따른 독성문제와 환자의 내성문제 등 많은 부작용이 대두되 고 있으며 시판되고 있는 acarbose나 voglibose 등의 α -glucoside 저해제가 시판되고 있으나, 이들 약제를 장기간 복용할 경우 일부 환자에게서 복부팽만감, 구토, 설사 등 부작용이 나타날 수 있어 사용이 제한될 수 있다(8,9). 이러 한 부작용을 줄이고 혈당을 낮추는 효과를 가지는 약용식물 들에 대한 관심이 높아지면서 새로운 α-glucosidase나 α -amylase 저해물질을 찾는 연구가 꾸준히 진행되고 있으며, 특히 당뇨병과 항산화 작용이 밀접한 관계가 있는 것으로 알려지면서 약용 식물 추출물에 대한 항산화 및 항당뇨 연구가 활발히 수행되고 있다(10-12).
청미래덩굴(Smilax China L.)는 한국, 일본, 중국, 필리핀 및 인도차이나 등의 지역에 분포하며, 우리나라 대부분의 산야에서 서식하는 백합과(Lilaceae)에 속하는 덩굴성 관목 으로 지역에 따라 명감나무, 매발톱가시, 참열매덩굴, 종가 시덩굴 등 다양하게 불리고 있으며, 원예 분야에서는 멍개 나무 또는 망개나무로 잘 알려져 있다. 잎은 넓은 타원형으 로 광택이 있으며 두껍고, 5월에 황록색의 꽃이 피며, 9-10 월에 둥근 열매가 빨갛게 익는다. 어린순과 열매는 식용을 하고, 뿌리와 나무는 해열, 해독, 이뇨 등의 증상 완화, 체력 증강 및 피부염, 신장염, 방광염, 항균작용, 관절염, 유방암 등에 효과가 있다고 알려져 있다(13-15). 청미래덩굴의 함 유 성분으로는 pseudoprotodioscin, dioscin, protodioscin, sieboldogenin, spirostane 와 furostane의 glycoside 등이 있다. 또한 청미래덩굴(Smilax China L.)의 근경을 지칭하는 토복 령의 성분에 관한 연구는 아직 많지는 않지만 saponin, tannin 등이 주성분이라고 알려져 있으며, 뿌리에서 분리된 배당체 ophiopogonin과 점액성 물질이 많이 포함되어 인체 의 면역 증진과 각종 세균의 감염으로부터 장기를 보호하는 데 중요한 역할을 한다고 알려져 있으며 또한 중금속 중독 에 대한 해독 작용에 효과적이라고 알려져 있다(16,17). 따라서 본 연구에서는 청미래덩굴 추출물의 항산화 및 항당뇨 효과 연구를 통해 여러 분야에서 천연 항산화제 및 항당뇨 소재로서의 활용 가능성을 알아보고자 하였다.
재료 및 방법
본 실험에 사용된 청미래덩굴은 충북 괴산에서 2012년 봄에 생산 된 건채를 구입하여 에탄올과 열수 추출을 실시 하였다. 시료의 에탄올 추출물은 70% 에탄올을 시료의 10 배를 첨가하여 실온에서 24시간 침지하여 상등액과 침전물 을 분리하여 동일한 방법으로 3회 반복 추출하였고, 열수 추출물은 증류수를 시료의 10배를 첨가하여 80℃에서 3시 간가량 환류냉각 추출해 실온에서 24시간 침지하여 상등액 과 침전물을 분리하여 동일한 방법으로 3회 반복 추출하였 다. 각 시료 추출물은 여과지(Whatman No.2)를 이용하여 여과한 후 EYELA evaporator로 감압 농축하여 용매를 완전 히 제거한 후 동결 건조하여 파우더 상태로 -20℃에 보관하 면서 본 실험의 시료로 사용하였다.
실험에 사용된 시약인 folin-ciocalteu phenol reagent, 2,2-diphenyl-1-picrylhydrazyl(DPPH), potassium persulfate, xanthine, xanthine oxidase, pyrogallol, AlCl3, quercetin, tannic acid, pancreatin α-amylase(EC No. 232.565.6), α -glucosidase(EC No. 232.604.7), ρ-nitrophenol-α-D-glucophyansoside (PNPG) 등은 Sigma Chemical Co.(St. Louis, MO, USA)에서 구입하였으며, 2,2’-Azino-bis(3-ethylbenzothiazoline-6-sulfonic acid)는 Wako Pure Chemical Industries. Ltd.(Japan)에서 구 입하였다.
폴리페놀 정량은 AOAC(18)를 변형하여 정량하였다. 즉, 시료 용액 50 μL에 2 N Folin-Ciocalteu’s phenol reagent 50 μL를 가하고 실온에서 3분간 반응시킨 후 0.7 M Na2CO3 용액 50 μL를 넣어 실온에서 1시간 방치하고, 700 nm에서 흡광도를 측정한 후, 표준물질인 tannic acid로 미리 작성한 표준곡선의 흡광도 값과 비교하여 폴리페놀 함량을 산출하 였다.
총 플라보노이드 함량은 Zhuang 등(19)의 방법을 변형하 여 측정하였다. 즉, 시료 용액 100 μL에 2% AlCl3 ethanol solution 100 μL을 가하여 실온에서 1시간 방치한 후 420 nm에서 흡광도를 측정하였다. 표준물질로는 quercetin을 사용하였으며, 표준물질의 검량선과 비교하여 총 플라보노 이드 함량을 구하였다.
전자공여능(EDA: electron donating abilities)은 Blois의 방법(20)을 변형하여 측정하였다. DPPH용액(Sigma) 60 μL 와 농도별(50, 100, 500μg/mL) 시료를 120 μL씩 넣고 혼합 한 후 15분간 방치한 다음 microplate reader를 이용하여 517 nm에서 흡광도를 측정하였다. 전자공여능은 시료용액 의 첨가구와 무첨가구의 흡광도 감소율로 나타내었다.
ABTS radical을 이용한 항산화력 측정은 ABTS+ cation decolorization assay 방법(21)에 의하여 측정하였다. 7 mM 2,2-azino-bis(3-ethyl-benthiazoline-6-sulfonic acid)와 2.45 mM potassium persulfate를 혼합하여 실온에서 24시간 동안 방치하여 ABTS+를 형성시킨 후 ethanol로 희석하여 ABTS+ 100 μL에 농도별(50, 100, 500 μg/mL) 시료 100 μL 를 가하여 700 nm에서 흡광도를 측정하였다.
SOD 유사활성은 Marklund의 방법(22)을 변형하여 측정 하였다. 농도별(50, 100, 500 μg/mL) 시료용액을 20 μL에 tris-HCl 완충용액(50 mM Tris-HCl buffer, pH 8.5) 130 μL와 pyrogallol(7.2 mM) 20 μL를 취하여 혼합한 후 37℃에서 10 분간 반응시킨 후 산화된 pyrogallol양을 microplate reader 를 이용하여 흡광도 420 nm에서 측정하였다. SOD 유사활 성은 시료용액의 첨가구와 무첨가구의 흡광도감소율로 나 타내었다.
Xanthine oxidase 저해활성 측정은 Stirpe와 corte의 방법 (23)을 변형하여 측정하였다. 농도별(50, 100, 500 μg/mL) 시료용액 100 μL에 potassium phosphate 완충용액(0.1M potassium phosphate buffer, pH 8.0) 600 μL와 xanthine(2 mM)을 녹인 기질액 200 μL를 첨가하고, xanthine oxidase (0.2 U/mL) 100 μL를 가하여 37℃에서 15분간 반응시킨 후 1 N HCl 1 mL를 가하여 반응정지를 시키고 반응액중에 생성된 uric acid를 흡광도 292 nm에서 측정하였다. Xanthine oxidase 저해활성은 시료용액의 첨가구와 무첨가 구의 흡광도 감소율로 나타내었다.
ACE 저해효과 측정은 Cushman 등의 방법(24)에 의하여 행하였다. 즉, 반응구는 0.3 M NaCl을 함유하는 0.1M potassium phosphate buffer(pH 8.3)에 기질로 2.5 mM hippuryl-histidyl-leucine 용액 0.15 mL를 혼합하였으며, 대 조구는 추출액 대신 동일 buffer 0.1 mL를 첨가하여 37℃에 서 30분간 반응시키고 1 N HCl 0.35 mL 첨가로 반응을 중지시킨 뒤 3 mL의 EtOAc를 첨가하였다. EtOAc층만을 취한 다음 용매를 증류시킨 잔사에 2 mL의 증류수를 첨가 하여 효소에 의해 기질로부터 분리되어 추출된 hippuric acid를 280 nm에서 흡광도를 측정한 후 표준곡선에서 양을 환산하여 아래의 식에 의해 저해율을 계산하였다.
본 실험에 TBARS는 Burge와 Aust의 방법(25)에 따라 측정하였다. 1% linoleic acid와 1% tween-40으로 emulsion 을 만들고 emulsion 0.8 mL와 시료 0.2 mL를 섞은 후 50℃ water bath에서 10시간 반응시켰다. 반응 후 반응액 1mL에 TBA reagent 2 mL를 가하고 15분간 중탕한 다음 10분간 냉각시킨 후 15분간 1,000 rpm으로 원심분리 하였다. 원심 분리 한 액을 실온에서 10분간 방치 한 후 상등액을 532 nm서 흡광도를 측정하였으며, TBARS 값은 1mL 반응혼합 물에 대해서 생성된 1,1,3,3-tetraethoxy propane(TEP)의 함 량을 환산하여 [1-(반응구의 생성량/대조구의 생성량)] × 100 으로 항산화 활성을 나타내었다.
PF는 Andarwulan과 Shetty의 방법(26)으로 측정하였다. 10 mg의 β-carotene을 50 mL chloroform에 용해한 용액 1 mL를 evaporator용 수기에 넣고 40℃ water bath에서 chloroform을 증류시킨 후, 20 μL linoleic acid, 184 μL tween 40과 50 mL H2O2를 가하여 emulsion을 만들고, 5 mL emulsion을 농도별(50, 100, 500μg/mL) 시료용액 100 uL에 혼합하여 잘 섞어준 뒤 50℃에서 30분간 반응시켜 냉각시킨 다음, 470 nm에서 흡광도를 측정하였고, PF는 반응구의 흡 광도/대조구의 비로 나타내었다.
세포를 α-glucosidase 저해활성을 측정하기 위하여 Tibbot 등의 방법(27)에 따라 반응 혼합액은 50mM sodium succinate buffer(pH 4.2)에 p-nitrophenol-α-D-glucopyranoside (PNPG)를 용해시켜 1 mg/mL의 농도로 기질을 만들었다. 기질 1 mL와 효소액(30 unit) 0.1 mL를 혼합하고 대조구에 는 증류수 0.1 mL, 반응구에는 농도별(50, 100, 500 μg/mL) 시료 0.1 mL을 넣어 37℃에서 30분간 반응시킨 후 1N-NaOH 0.1 mL를 첨가하여 발색시켰다. 이때 생성된 p-nitrophenol(PNP)은 400 nm에서 spectro-photometer를 이 용하여 측정하였으며, 그 양은 표준물질 p-nitrophenol로 부 터 작성한 표준곡선으로부터 구하여 다음의 식으로 저해율 을 구하였다.
α-amylase 저해활성 측정은 agar diffusion 방법(28)을 이 용하여 측정하였다. Plate는 5 g의 agar와 5 g의 soluble starch를 500mL 증류수에 녹인 후 121℃, 15분간 감압 살균 하고 15mL씩 분주하여 제조하였고, 대조군의 경우 0.8 μL 의 증류수 0.2 μL의 효소(1,000 unit/mL)를 섞고 반응군은 증류수 대신 추출물을 효소와 섞어 plate에 놓인 disc paper 위에 각각 분주하고 37℃에서 3일간 배양한 후 I2/KI(5mM I2 in 3% KI) 5mL를 가하여 15분간 발색 후 다음의 식으로 효소 저해율을 구하였다.
결과 및 고찰
천연 항산화제로서의 기능이 잘 알려진 식물체에는 2차 대사산물의 하나인 페놀성 물질이 있으며, 이 물질은 콜레 스테롤저하작용, 항암 및 항산화 작용 등 다양한 항산화 생리활성 기능을 가지고 있다(29). 이에 tannic acid를 기준 물질로 하여 표준곡선을 그린 후 청미래덩굴 에탄올 및 열수 추출물의 폴리페놀 함량을 측정한 결과 Table 1과 같이 나타내었다. 청미래덩굴 에탄올 추출물은 108.4 mg/g, 열수 추출물은 44.6 mg/g으로 청미래덩굴 열수추출물보다 에탄올 추출물에 더 많은 폴리페놀이 함유되어 있음을 확인 할 수 있었다. 이는 Chung 등(30)의 구절초의 꽃, 잎 및 줄기, 뿌리 등 부위별 메탄올 추출물이 각각 17.16 mg/g, 14.75 mg/g, 13.50 mg/g의 폴리페놀을 함유하고 있다는 연 구결과와 비교하였을 때 청미래덩굴 추출물에 더 많은 폴리 페놀이 함유되어 있음을 확인할 수 있었다.
| Sample | Extract | Total phenolics (mg/g) | Total flavonoids (mg/g) |
|---|---|---|---|
| Smilax china L. | 70% EtOH | 108.4±0.83 | 76.2±4.78 |
| Water | 44.6±0.68 | 35.3±2.11 |
플라보노이드는 주로 anthocyanidins, flavonols, flavones, cathechins 및 flavonones 등으로 구성되어 있으며, 그 구조 에 따라 특정 flavonoid는 항산화, 항암, 항염증, 항노화 등 다양한 생리적 기능을 가지고 있는 것으로 보고되고 있다 (31,32). 따라서 quercetin을 기준물질로 하여 표준곡선을 그린 후 청미래덩굴 에탄올 추출물과 열수 추출물의 플라보 노이드 함량을 측정한 결과 Table 1와 같이 나타내었다. 청미래덩굴 에탄올 추출물은 76.2mg/g, 열수 추출물은 35.3 mg/g의 함량을 나타내었다. 이는 Lee 등(33)의 환삼덩굴의 메탄올 추출물이 13.61 mg/g의 플라보노이드를 함유하고 있음을 확인한 연구와 Kim 등(34)의 자생식물 26종과 생약 자원 추출물 14종 중 사상자와 흑두에서는 플라보노이드가 검출되지 않았고, 어성초는 1.40 mg/g, 쥐오줌풀은 6.40 mg/g의 플라보노이드를 함유하고 있음을 확인한 연구 결과 와 비교하였을 때 청미래덩굴 추출물에 더 많은 플라보노이 드가 함유되어 있음을 확인할 수 있었다.
전자공여능 측정에 사용된 1-1-diphenyl-2-picryl-hydrazyl (DPPH)는 짙은 자색을 띄는 비교적 안정한 free radical로서 cystein, glutathion과 같은 함 유황아미노산과 ascorbic acid, butylated hydroxyanisole(BHA) 등에 의해 환원되어 탈색되 므로 다양한 천연 소재로부터 항산화 물질을 검색하는데 많이 이용되고 있다(35). 청미래덩굴의 전자공여능을 측정 한 결과 Fig. 1과 같이 에탄올 추출물과 열수 추출물은 각각 500 μg/mL에서 43.5%, 35.1%의 활성을 나타내었다. 이는 Kim 등(36)의 천년초 추출물의 80% 에탄올 추출물이 19.7%, 열수 추출물이 6.03%의 활성을 나타내었다는 연구 논문과 비교하였을 때 청미래덩굴 에탄올 및 열수 추출물에 서 유의성 있는 결과를 확인할 수 있었다.
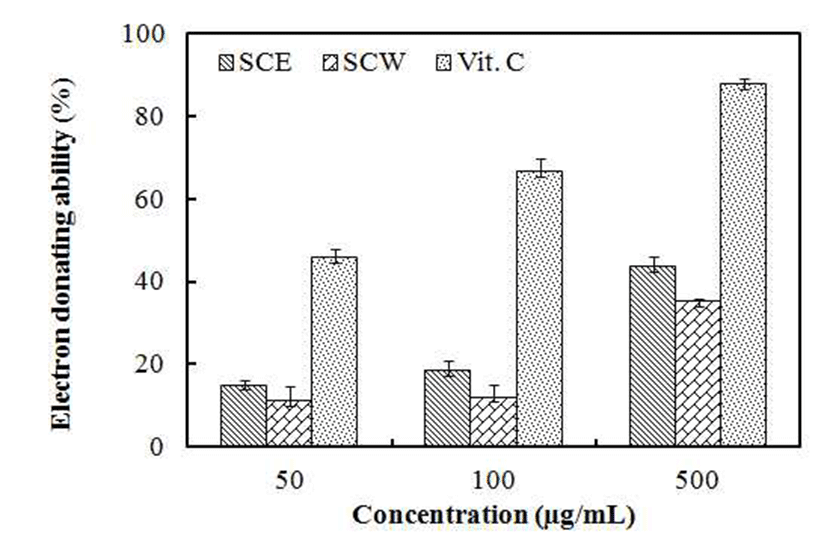
 SCE : Ethanol extract of S. china.
SCE : Ethanol extract of S. china.
 SCW : Water extract of S. china.
SCW : Water extract of S. china.
 Vit. C: ascrobic acid
Result are means±SD of triplicate data.
Vit. C: ascrobic acid
Result are means±SD of triplicate data.
ABTS radical cation 소거능은 ABTS diammonium salt와 potassium persulfate와의 반응에 의해 생성된 ABTS free radical이 추출물 내의 항산화 물질에 의해 제거되어 radical 특유의 색인 청록색에서 연한 녹색으로 탈색되는 것을 측정 하는 방법이다(37). 이러한 방법을 통해서 청미래덩굴 에탄 올 추출물과 열수 추출물의 ABTS 전자공여능을 측정한 결과 Fig. 2와 같이 나타내었다. 청미래덩굴 에탄올 추출물 과 열수 추출물은 각각 500 μg/mL에서 75.8%와 73.4%의 소거능이 있음을 확인하였다. 이는 Yu 등(38)의 연구에서 오가피 순 추출물이 0.1, 0.5, 1 mg/mL의 농도에서 각각 6.42%, 12.47%, 16.69%의 활성을 확인한 결과와 비교하였 을 때 청미래덩굴 에탄올 추출물과 열수 추출물 모두 ABTS radical 소거활성이 높은 것을 확인할 수 있었다.
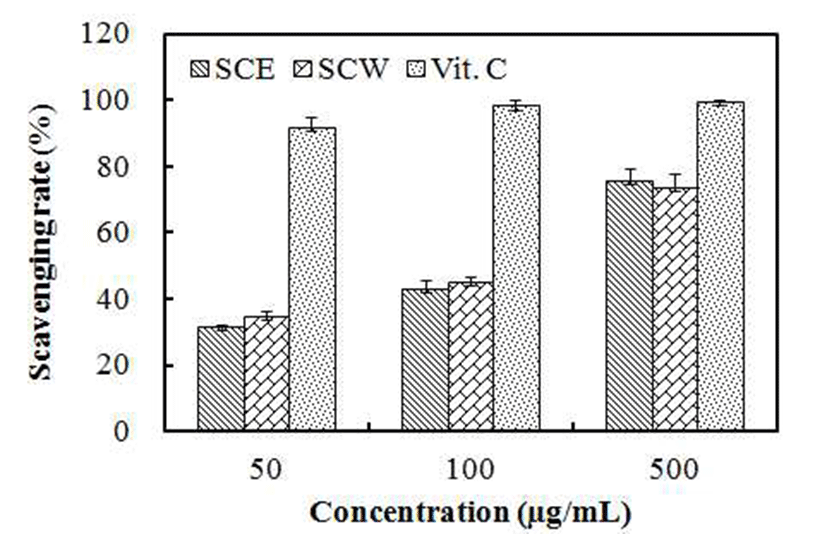
 SCE : Ethanol extract of S. china.
SCE : Ethanol extract of S. china.
 SCW : Water extract of S. china.
SCW : Water extract of S. china.
 Vit. C: ascrobic acid
Result are means±SD of triplicate data.
Vit. C: ascrobic acid
Result are means±SD of triplicate data.
Superoxide radical 유사활성능은 알칼리 상태에서 pyrogallol의 자동산화에 의한 발색을 이용한 측정방법으로 pyrogallol는 수용액에서 자동산화가 빠르게 일어나는데 여 기에는 superoxide가 관여한다고 알려져 있다(39). SOD는 다른 종류의 항산화제보다 우수한 효과를 나타내기 때문에 의약제제로서 많은 관심을 일으키고 있으며, 현재 항염증 제재나 피부노화방지를 위한 미용제재로 화장품 등에 많이 이용이 되고 있다. 이러한 방법으로 청미래덩굴 에탄올 추 출물과 열수 추출물의 SOD 유사활성능을 측정한 결과 Fig. 3과 같이 청미래덩굴 500 μg/mL에서 각각 26.3%, 16.8%의 유사활성능을 확인하였다. 이는 대조군인 Vit. C와 비교하 였을 때 비교적 낮은 수치였지만 Lee 등(40)의 연구에서 가죽나무 뿌리 추출물이 3.82%, Kim 등(41)의 갈근, 당귀, 감초, 산약 등에서 12.4%의 활성을 확인한 결과와 비교하였 을 때 청미래덩굴 추출물의 SOD 유사활성능이 유의한 결 과를 나타냄을 확인할 수 있었다.
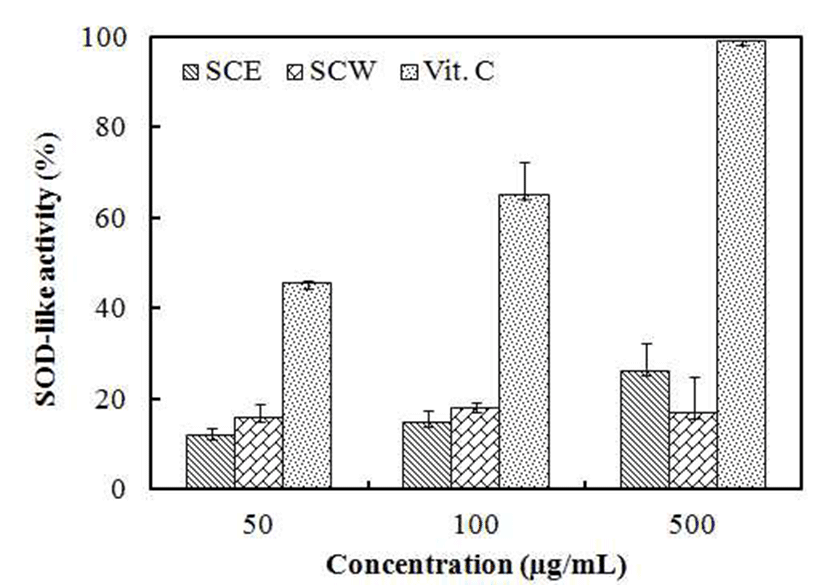
 SCE : Ethanol extract of S. china.
SCE : Ethanol extract of S. china.
 SCW : Water extract of S. china.
SCW : Water extract of S. china.
 Vit. C: ascrobic acid
Result are means±SD of triplicate data.
Vit. C: ascrobic acid
Result are means±SD of triplicate data.
Xanthine oxidase는 생체 내 유리기 생성계의 하나로 purine 대사에 관여하는 효소로서 xanthine 또는 hypoxanthine 으로부터 urate를 형성하며 urate가 혈장 내에 증가되면 골 절에 축적되어 심한 통증을 유발하는 통풍과 신장에 침착되 어 신장질환을 일으키는 효소로 알려져 왔다(42,43). 그 외 에 효소활성을 저해할 목적으로 천연물을 대상으로 하는 많은 연구가 진행되어 왔는데, 식물계에 존재하는 flavonoid 류는 hydroxyl기의 위치에 따라 xanthine oxidase 저해효과 가 다르며, galloyl기를 함유한 flavonoid 화합물이 xanthine oxidase 저해효과가 우수하였으며 경쟁적으로 저해한다는 사실을 보고하였다(44). 청미래덩굴 에탄올 추출물과 열수 추출물의 xanthine oxidase 저해효과를 측정한 결과 Fig. 4와 같이 500 μg/mL에서 55.2%, 32.6%로 청미래덩굴 에탄올 추출물이 열수 추출물보다 높은 활성을 보였다. 이는 Yoon 등(45)의 미숙, 완숙 및 과숙 뜰보리수 열수 추출물이 각각 32.8%, 11.2% 및 5.0%의 활성을 나타낸 연구결과와 비교하 였을 때 청미래덩굴 에탄올 추출물과 열수추출물의 활성이 우수함을 확인할 수 있었다.
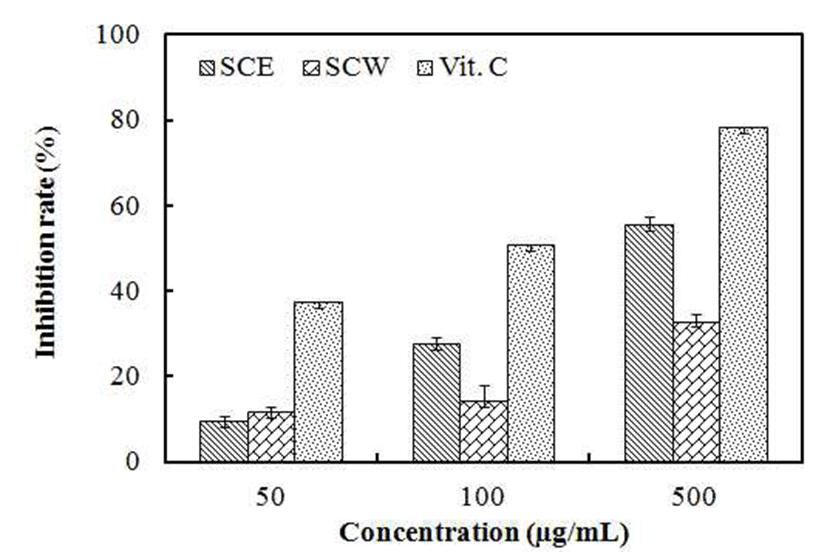
 SCE : Ethanol extract of S. china.
SCE : Ethanol extract of S. china.
 SCW : Water extract of S. china.
SCW : Water extract of S. china.
 Vit. C: ascrobic acid
Result are means±SD of triplicate data.
Vit. C: ascrobic acid
Result are means±SD of triplicate data.
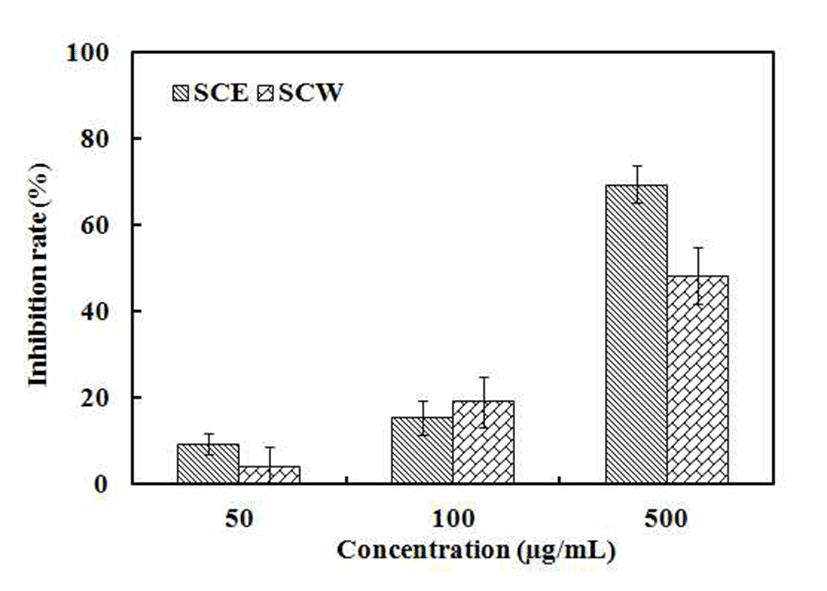
ACE은 angiotensinⅠ에서 혈관수축 작용을 갖는 octapeptide인 angiotensin Ⅱ로 변화하는 단계에 관여하는 효소이다. angiotensin Ⅱ는 A-Ⅱ 수용체와 결합하여 동맥과 소동맥을 수축시키고 부신피질을 흥분시켜 알도스테론의 유리를 촉진시켜 결과적으로 혈압의 증가를 가져온다. 따 라서 ACE 저해물질은 ACE의 활성을 억제함으로써 고혈압 을 직접적으로 억제할 수 있다(46). 청미래덩굴 에탄올 추출 물과 열수 추출물이 고혈압의 발생기작에서 ACE저해 작용 을 통한 고혈압 억제 활성을 측정한 결과 Fig. 5에서와 같이 청미래덩굴 에탄올 추출물과 열수 추출물은 500 μg/mL에 서 각각 69.4%, 48.3%의 저해율을 보였다. 이는 Choi 등(47) 의 연구에서 측정한 약용식물 중에서 행인, 백작약, 두충, 강활, 향부자등이 각각 21.3%, 16.9%, 28.4%, 18.9%, 8.89% 의 저해활성을 확인한 결과와 비교하였을 때 본 연구에 이용된 청미래덩굴 추출물의 ACE 저해활성이 우수함을 확인할 수 있었다.
 SCE : Ethanol extract of S. china.
SCE : Ethanol extract of S. china.
 SCW : Water extract of S. china.
Result are means±SD of triplicate data.
SCW : Water extract of S. china.
Result are means±SD of triplicate data.
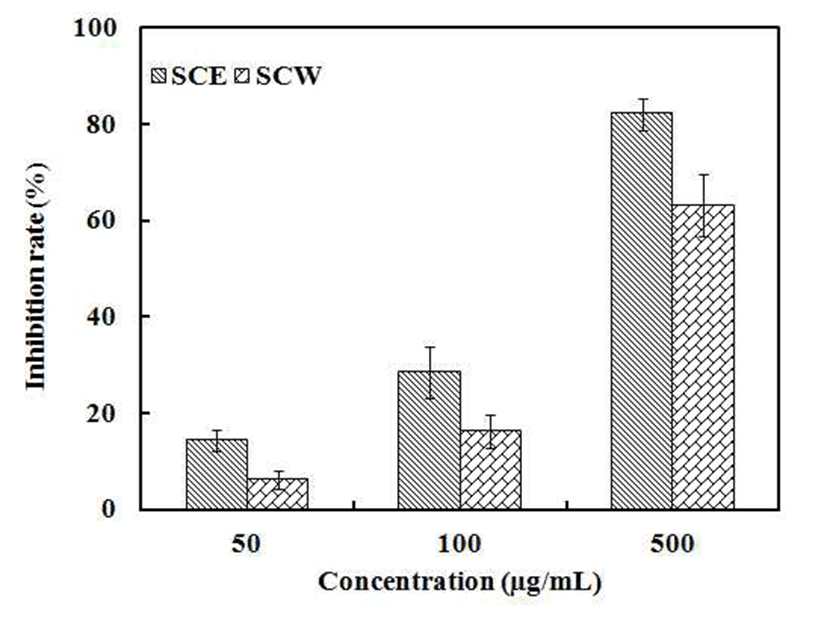
지방산패도를 나타내는 TBARs 값은 TBA시약과 반응하 여 붉은색을 띄는 malondialdehyde(MA)의 생성량을 나타 낸 것이다(25). 청미래덩굴 추출물을 첨가하여 TBARs를 측정한 결과 Fig. 6과 같이 청미래덩굴 에탄올 추출물과 열수 추출물은 500 μg/mL의 농도에서 각각 82.2%, 63.2%의 억제율을 확인하였다. 이는 Kim 등(48)의 연구에서 산삼배 양근의 열수 추출물 및 70%에탄올 추출물이 1∼20mg/mL 의 농도에서 열수 추출물은 4.74∼24.88%, 70% 에탄올 추 출물은 9.18∼66.59%의 억제능을 나타내었다는 결과와 비 교하였을 때 청미래덩굴의 지질산패 억제능이 높은 것을 확인할 수 있었다.
 SCE : Ethanol extract of S. china.
SCE : Ethanol extract of S. china.
 SCW : Water extract of S. china.
Result are means±SD of triplicate data.
SCW : Water extract of S. china.
Result are means±SD of triplicate data.
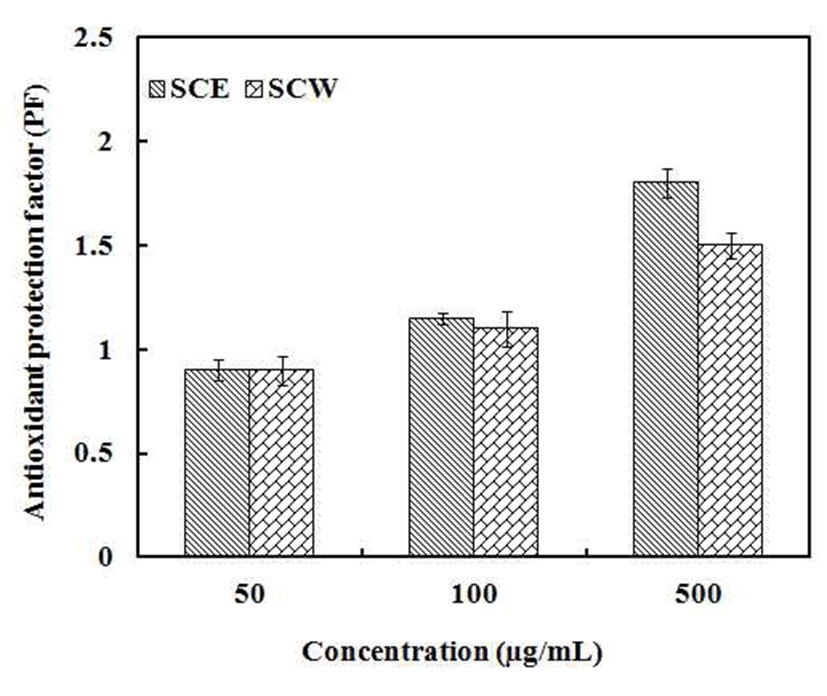
β-carotene은 주로 lipoprotein과 같은 지방친화성 구조의 내부에 존재하면서 지질 산화과정에서 생성되는 peroxy radical과의 반응으로 생성된 불활성물질로 인해 free radical 에 의한 연쇄반응을 중단시켜 singlet oxygen을 효과적으로 억제하는 것으로 알려져 있다(49). 청미래덩굴 추출물의 지용성 물질에 대한 항산화력을 측정하기 위해 PF를 측정 한 결과 Fig. 7에서와 같이 청미래덩굴 에탄올 추출물과 열수 추출물 500 μg/mL에서 각각 1.8 PF, 1.5 PF값을 나타내 었다. 이는 Kim 등(50)의 연구에서 진범의 에탄올 추출물과 열수 추출물이 500 μg/mL 이상의 농도로 첨가하였을 때 에탄올 추출물은 1.4∼1.49 PF, 열수 추출물은 1.27∼1.33 PF값을 나타낸 결과와 비교하였을 때 청미래덩굴 추출물의 지용성물질에 대한 항산화력이 우수하다는 것을 확인할 수 있었다.
 SCE : Ethanol extract of S. china.
SCE : Ethanol extract of S. china.
 SCW : Water extract of S. china.
Result are means±SD of triplicate data.
SCW : Water extract of S. china.
Result are means±SD of triplicate data.
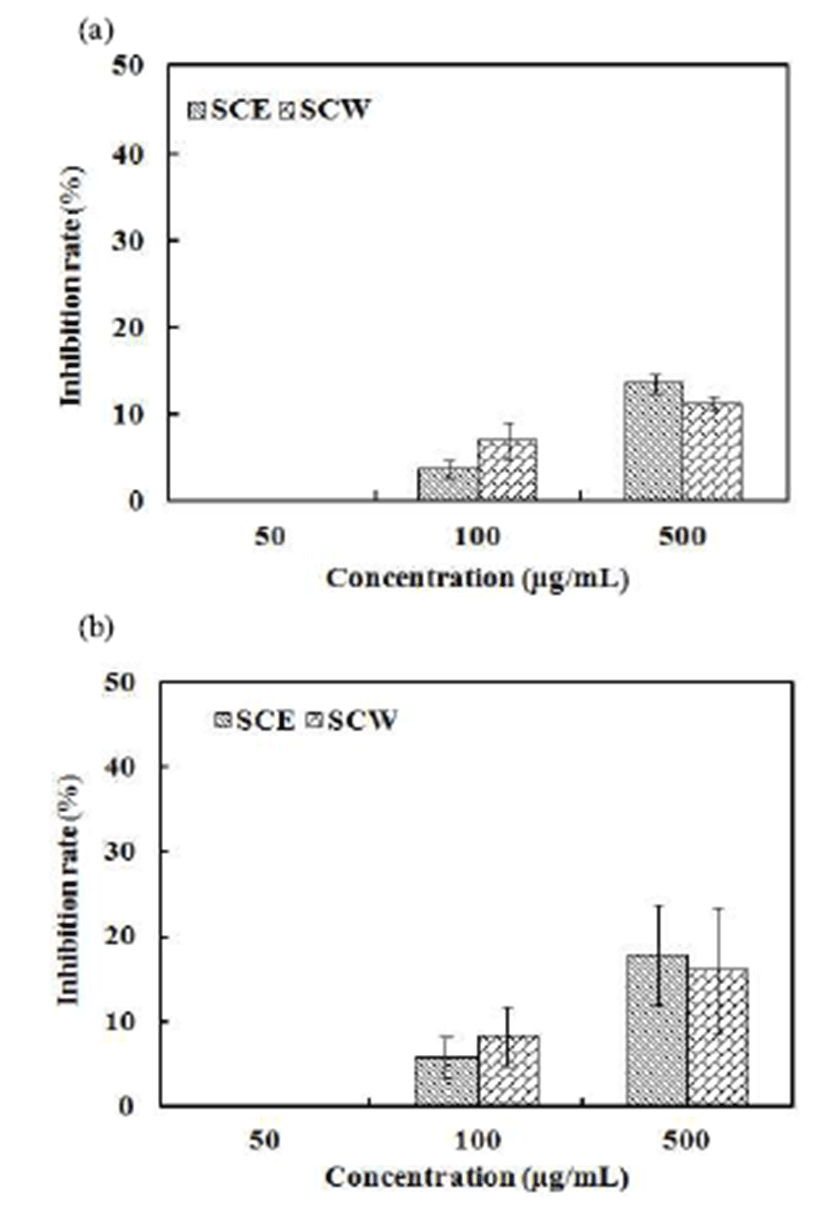
α-glucosidase는 소장점막의 미세응모막에 존재하는 효 소로서 다당류의 탄수화물을 단당류로 분해하는 탄수화물 의 소화와 흡수에 필수적인 효소로서 경구혈당강하제로 사용되고 있다(51). 이 효소의 활성을 저해시킴으로서 체내 의 포도당 흡수를 억제시켜 식후 혈당상승을 감소시킬 수 있으며, 저혈당의 부작용을 일으키지 않는 큰 장점을 가질 수 있어 α-glucosidase저해 물질의 탐색은 매우 유용하다 (52). 청미래덩굴 추출물의 α-glucosidase 저해활성을 측정 한 결과 Fig. 8(a)와 같이 에탄올 추출물과 열수 추출물은 500 μg/mL의 농도에서 각각 13.6%, 11.2%의 저해활성을 보였다. 이는 다소 낮은 활성이지만 Kim 등(53)의 강원도 자생 산채 추출물 중 홀아비꽃대, 국화수리취, 뻐꾹채, 사철 쑥의 에탄올 및 열수 추출물이 각각 8.1%, 4.0%, 2.8%, 4.5%, 8.3%, 11.1%, 7.9%, 9.9%의 저해율을 보인 연구결과와 비교 하였을 때 유사한 활성을 나타내었다.
사람이 탄수화물을 섭취하면 이를 분해하기 위해 가장 먼저 작용하는 소화효소가 타액의 α-amylase와 췌장내의 α-amylase로 탄수화물의 소화에 있어서 중요한 효소이다. 이 효소를 저해시킴으로서 탄수화물의 소화 속도를 지연시 켜 식후 혈당 상승을 억제할 수 있다(54). 청미래덩굴 추출 물의 α-amylase 저해활성을 측정한 결과 Fig. 8(b)와 같이 청미래덩굴 에탄올 추출물과 열수 추출물 500 μg/mL의 농 도에서 각각 17.9%, 15.9%의 저해활성을 나타내었다. Kim 등(53)은 모시대, 미역취, 만병초의 에탄올 추출물과 열수 추출물이 각각 5.2%, 3.7%, 15.5%, 10.1%, 26.8%, 17.4%의 저해율이 있다고 보고하였으며, 이는 청미래덩굴 추출물의 α-amylase 저해활성과 유사한 결과를 나타내었다.
 SCE : Ethanol extract of S. china.
SCE : Ethanol extract of S. china.
 SCW : Water extract of S. china.
Result are means ± S.D. of triplicate data.
SCW : Water extract of S. china.
Result are means ± S.D. of triplicate data.
요 약
본 연구에서는 백합과에 속하는 덩굴성 관목인 청미래 덩굴 70% 에탄올 추출물과 열수 추출물의 항산화 및 항당 뇨에 대한 활성을 연구하였다. 총 폴리페놀 함량 과 플라보 노이드 함량 측정, 전자공여능, ABTs 소거능, SOD 유사활 성능, xanthine oxidase 저해활성, ACE 저해활성, TBARs 측정, PF값 측정 및 α-glucosidase 와 α-amylase 의 저해활성 을 측정하였다. 그 결과 총 폴리페놀 함량과 플라보노이드 함량은 에탄올 추출물에 함유량이 더 많았으며, 전자공여 능, ABTs 소거능, SOD 유사활성능, xanthine oxidase 저해활 성, ACE 저해활성, TBARs 측정, PF값 측정 결과 모두 청미 래 덩굴 열수 추출물보다 에탄올 추출물의 활성이 우수하였 다. 또한 α-glucosidase 와 α-amylase 의 저해활성을 측정한 결과 에탄올 추출물의 활성이 열수 추출물보다 우수하였 다. 이상의 검증 결과를 종합하여 볼 때 청미래 덩굴의 에탄 올 추출물의 항산화 및 항 당뇨 활성이 우수하였고, 차후 항산화 및 항 당뇨 예방물질 소재로서의 활용이 가능할 것으로 판단된다.