1. 서론
현대인들은 다양하고 건강한 식이에 관심을 갖고 있다. 그중 과일은 비타민과 무기질을 공급하며, 식물성 에스트로겐, 항산화 및 항염증제, 기타 보호 메커니즘으로 기능하는 식물성 화학 물질의 공급원이다(Cosme 등, 2022). 이러한 과일은 식이섬유 특히 펙틴의 주요 공급원이며, 섬유질 섭취는 심혈관 질환과 비만의 발병률을 낮추는 것과 관련 있으며, 상업용 펙틴의 90% 이상이 과일 부산물에서 유래된다(Cui 등, 2021). 또한, 과일은 가식 부위 과육과 비가식 부위 껍질이나 씨로 나뉜다(Lee와 Yi, 2023).
과일 부산물은 산업적 가공 과정에서 많은 양으로 생산되며 환경에 해로운 위험을 초래할 수 있기 때문에 심각한 문제가 된다. 그러나 과일 껍질을 적절히 활용하면 많은 환경 문제를 해결할 수 있을 뿐만 아니라, 건강 기능 소재가 함유된 강화식품을 통해 건강을 개선할 수도 있다(Hussain 등, 2022).
한편, 감귤은 세계적으로 많이 섭취되고 있는 과일 중 하나로 유엔 식량농업기구에 의하면 매년 2,560만 톤 이상의 감귤이 생산되고 있다(Unugul과 Nigiz, 2020). 한국에서는 주로 제주도에서 감귤을 재배하고 있으며, 연간 약 56만 톤 이상 생산되고 있고 우리나라 전체 과실 생산량의 30% 이상을 차지하고 있다(Jang 등, 2004). 감귤 제품 가공 시 생성되는 껍질은 유기 폐기물로, 감귤주스 가공 과정 중 매년 15만 톤의 감귤 과피가 발생되고 있다(Hyon 등, 2010; Šafranko 등, 2021). 감귤 과피에는 폴리페놀, 비타민, 미네랄, 식이섬유 및 카로티노이드 등이 함유되어 있으며, 감귤 유래 플라보노이드 배당체 형태인 헤스페리딘과 나린진이 풍부한 것으로 알려져 있다(Lee 등, 2022). 감귤의 부산물인 감귤껍질은 천식, 위장장애, 감기 예방, 동맥경화 등의 효과가 있다(Park과 Lee, 2021; Yang 등, 2008; Zhang 등, 2019).
또한, 사과는 국내에서 가장 많이 생산되는 과일 중 하나이며, 사과껍질에는 퀘르세틴 함량이 높은 것으로 알려져 있다(Youn 등, 2017). 사과에 함유된 폴리페놀은 사과의 항산화 활성에 주요 역할을 하는 물질로, 식품으로부터 공급받는 항산화 물질 중 큰 비중을 차지하는 중요한 물질이다(Vinson 등, 2001). 이러한 폴리페놀 화합물은 과육보다 과피에 더 많이 함유되어 있다고 보고되어 과일 껍질의 기능성 및 활용 방안에 대한 관심이 증가하고 있다(Henríquez 등, 2003; Kubola와 Siriamornpun, 2011; Wolfe 등, 2003). 사과는 한국인들에게 섭취 빈도가 가장 높은 과일이며, 식물성 식품 자체(57.5%)로 직접 섭취하는 비율이 가장 높게 나타났다(Choi 등, 2021). 사과는 플라보노이드, 펙틴, 아스코르브산이 풍부하고 지방, 나트륨, 칼로리 함량이 낮은 영양가 있고 건강한 과일 중 하나로 인식되고 있다(Lončar 등, 2022).
포도의 경우 포도 찌꺼기의 약 50%는 포도 품종 및 토양 기후 조건에 따라 포도 껍질(GP)로 구성된다(Iuga와 Mironeasa, 2020). 포도 껍질은 폴리페놀 화합물과 식이섬유의 공급원이며(Iuga 등, 2017; Karovičová 등, 2015; Sant’Anna 등, 2014), 항산화 및 항균 작용을 할 수 있는 성분이다(Olejar 등, 2019; Troilo 등, 2021). 항산화 특성을 가진 가장 중요한 포도 껍질 성분은 안토시아닌, 히드록시신남산, 카테킨, 플라보놀이며, 이는 저밀도 지단백질(LDL)의 산화 과정 억제할 수 있다(Deng 등, 2011; Meini 등, 2019). 포도 껍질은 최대 60% (dm)의 식이섬유를 함유하고 있으며, 불용성 분획이 가장 많고, 다음으로 당류가 함유되어 있으며, 적용되는 양조 공정에 따라 최대 70%까지 함유될 수 있다(Deng 등, 2011). 푸드 업사이클링은 환경적 관점에서 폐기물 저감과 탄소중립 실현에 기여할 뿐만 아니라, 경제적 관점에서 새로운 부가가치 창출과 원가 절감 효과를 가져올 수 있다.
기존 과일껍질에 대한 연구는 단일 과일 껍질을 이용한 분석이 이루어졌으며 여러 가지 과일 껍질 분말(감귤, 사과, 포도)의 영양성분 및 항산화 활성에 대해 비교 분석한 연구는 이루어지지 않았다. 그러므로 3가지 과일 껍질 분말의 성분 및 항산화 활성을 비교 분석하고 이러한 과일 껍질을 건강 기능성 식품소재로 성분과 항산화활성의 고부가가치 소재로 이용할 수 있으므로 본 연구는 과일 껍질을 활용하여 제품을 개발하기 전에 과일 껍질의 영양성분과 항산화 활성을 측정하여 기초자료를 수집하고자 하였다.
2. 재료 및 방법
100% 제주산 감귤껍질 분말은 (주)맑은들(Hongcheon, Korea)에서 구매한 것으로 품종은 온주감귤종, 사과껍질 분말은 (주)에프엔디큐엘(Mungyeong, Korea)에서 구매한 것으로 경북문경 부사종, 포도 껍질 분말은 코랄카운티(Koyang, Korea)에서 구매한 것으로 헝가리 토가이지역 프르민트종을 사용하였다.
재료 분석에 사용된 시약은 지방산 분석은 chloroform과 methanol (HPLC grade, Daejung, Siheung, Korea), 그리고 14% BF3-methanol (Supelco, Bellefonte, PA, USA)을 사용하였다. 유기산 및 유리당 분석은 ethanol (≥99.5%, Daejung), p-toluenesulfonic acid, Bis-Tris, EDTA, arginine, boric acid (Sigma-Aldrich, St. Louis, MO, USA)를 사용하였다. 미네랄 분석은 65% 질산(Daejung)과 35% 과산화수소(Junsei Chemical Co., Tokyo, Japan)를 사용하였고, 모든 분석에 사용된 이동상 및 희석용 용매는 HPLC 등급의 시약과 초순수 증류수(Milli-Q, Millipore, Burlington, MA, USA)를 사용하였다.
일반성분 분석은 AOAC (2016) 방법에 따라 수행하였다. 수분 함량은 상압가열건조법, 조회분은 회화법을 사용하였고, 조단백질은 원소 분석기(vario Max Cube, DKSH Co., Korea)를 이용하여 시료의 총질소 함량을 분석한 후, 포도 껍질에는 환산계수 5.30, 사과껍질에는 5.64, 감귤껍질에는 6.25를 적용하여 계산하였다(Mariotti 등, 2008). 조지방 함량은 Soxhlet 추출법으로 측정하였다. 탄수화물 함량은 100%에서 수분, 조회분, 조단백질 및 조지방을 각각 차감하여 계산하였다.
과일 껍질 분말의 총식이섬유는 AOAC법(2016, 효소 ․ 중량법)을 약식 변형하여 측정하였다. 각 시료 1.0 g을 50 mM morpholino ethanesulfonic acid (MES) 완충액(pH 8.0) 40 mL와 혼합한 뒤 효소 처리하였다: (1) 고온 안정성 α-아밀라아제(Sigma-Aldrich, St. Louis, MO, USA) 50 μL, 100°C 30분 가열 교반 후, (2) pH 7.5로 조정 후 프로테아제(Sigma-Aldrich) 50 mg, 60°C에서 30분 방치 후, (3) pH 4.5로 조정 후 아밀로글루코시다아제(Sigma-Aldrich) 150 μL, 60°C에서 30분간 방치하고, 반응액을 100 mL까지 증류수로 정용한 뒤, 0.5 μm 글라스필터로 진공 여과하였다. 여과 잔사는 95% 에탄올 3회 세척 후 105°C에서 5시간 건조한 후, 525°C 회화하여 불용성 식이섬유를 구하였다. 여과액은 4배 부피(95% 에탄올)로 침전하고 60°C에서 60분간 방치 후 동일 방식으로 여과하고 건조 ․ 회화하여 수용성 식이섬유를 얻었다. 각 잔사의 질량에서 잔류 단백질(켈달 질소 × 시료에 따른 환산계수)과 회분을 공제한 값을 IDF, SDF로 환산하였으며 Total Dietary Fiber = Insoluble Dietary Fiber + Soluble Dietary Fiber로 계산하였다. 모든 분석은 3회 반복 측정하였다. 분석 정확도 검증을 위해 상용 표준물질(Wheat bran TDF, Megazyme, Wicklow, Ireland)을 동시 분석하였다.
시료 0.5 g에 6 N HCl 15 mL를 가하여 진공 상태에서 ampoule에 밀봉하였다. 이후 110°C에서 24시간 동안 가수분해 후 45°C에서 감압 농축하여 잔류 산을 완전히 제거하였다. 남은 가수분해 잔액은 구연산나트륨 완충용액(pH 2.2)을 이용하여 25 mL로 정용하였고, 이를 0.45 μm membrane filter로 여과하여 분석용 시료로 사용하였다(AOAC, 2006).
구성아미노산 분석은 형광 검출기가 장착된 자동 아미노산 분석기(Shimadzu Co., Kyoto, Japan)를 이용하였으며, O-phthalaldehyde (OPA) 유도체화 방법(Sumiyoshi 등, 1995)에 따라 수행하였다. 분석에는 Shim-pack AMINO-NA column (6.0×100 mm)을 사용하였고, 완충용액의 유속은 0.6 mL/min, OPA 시약의 유속은 0.3 mL/min으로 설정하였다. 형광 검출은 excitation 파장 350 nm, emission 파장 450 nm 조건에서 진행하였다.
지방산은 시료 5 g을 칭량 후 균질화하고, chloroform-methanol 혼합용액(2:1, v/v)을 시료 대비 10배량 첨가하여 지질 추출 후 여과하여 감압 농축 후 AOAC (2000)법에 따라 14% BF3-methanol 용액을 첨가하여 methylation을 수행하였다. 이 때 생성된 지방산은 Gas Chromatography (GC-2010, Shimadzu)로 분석하였다. GC 분석시 컬럼은 SP-2560 fused silica capillary column (100 m×0.25 mm i.d., 0.20 μm film thickness, Supelco Inc., Bellefonte, PA, USA)을 사용하였다. 오븐 온도는 초기 150°C에서 5분간 유지 후, 3°C/min의 속도로 상승시켜 250°C에서 5분간 유지하였다. 운반기체로는 helium을 사용하였고, 유속은 18 cm/sec, split 비율은 1:50으로 설정하였다. 검출기는 flame ionization detector (FID)를 사용하였으며, 주입구와 검출기의 온도는 각각 270°C 및 250°C로 설정하였다.
시료 5 g에 80% ethanol 20 mL를 가하여 tissue grinder (IKA, Staufen im Breisqau, Germany)로 균질화한 후, 플라스크에 옮기고 80% ethanol 80 mL를 추가하였다. 플라스크는 환류냉각기에 연결한 뒤, 80°C 수욕상에서 3시간 동안 환류 추출 후 650 ×g에서 30분간 원심분리 후, 상등액을 여과하였다. 이 액은 회전식 진공농축기(rotary evaporator, CCA 1110, Eyela Co., Tokyo, Japan)를 이용하여 ethanol을 완전히 제거하여 약 1 mL로 농축하였다. 농축액은 증류수를 이용해 10 mL로 정용한 뒤, 이 중 3 mL를 0.45 μm membrane filter로 여과하여 유기산 및 유리당 분석용 시료로 사용하였다.
유리당 분석은 환원당 시스템(Shimadzu Co., Kyoto, Japan)을 이용하여 형광 검출 기반 post-column 유도체화 방법으로 수행하였다(Shin 등, 2015). 분석 장비는 LC-20AD 펌프, SIL-20AC 오토샘플러, CTO-20AC 컬럼 오븐, RF-10Axl 형광 검출기(Excitation 320 nm, Emission 430 nm), CBR-6A 반응기, CBM-20A 컨트롤러 및 LC Workstation 소프트웨어로 구성되었다. 분리는 이온교환 컬럼 Shim-pack ISA-07 (4.0×250 mm)과 ISA-guard (4.0×50 mm)를 사용하였다. 이동상으로는 potassium borate buffer (A 용액: pH 8, B 용액: pH 9)를 사용하고 gradient 방식으로 적용하였다.
이동상의 유속은 0.6 mL/min, post-column 반응 시약의 유속은 0.5 mL/min으로 설정하였으며, 시료는 10 μL 주입하였다. 유도체화 반응은 1% arginine과 3% boric acid를 포함한 혼합용액을 반응 시약으로 사용하고, CBR-6A 반응기 내에서 150°C에서 수행하였다. 환원당 표준물질은 탈이온수에 용해하여 0.5-20 μg/mL 범위로 검량선을 작성하였으며, 피크 면적을 기준으로 정량 분석하였다.
유기산 분석은 환류 추출 및 여과 과정을 거친 시료를 유기산 분석 시스템(Shimadzu Co., Kyoto, Japan)을 이용하여 post-column 유도체화 방식으로 수행하였다(Shin 등, 2015). 분석 시스템은 LC-20AD 펌프, SIL-20AC 오토 샘플러, CTO-20AC 컬럼 오븐, 전도도 검출기(CDD-10A), CBM-20A 컨트롤러 및 LC Workstation으로 구성되었다. 분리는 이온교환 컬럼인 Shim-pack SPR-102H (7.8×250 mm)를 2개 직렬 연결하여 사용하였고, 전처리 컬럼으로 SPR-H guard column (7.8×50 mm)을 적용하였다. 이동상으로는 4 mM p-toluenesulfonic acid를 사용하였으며, 유속은 0.8 mL/min, 시료 주입량은 10 μL로 설정하였다.
Post-column 유도체화 반응에는 16 mM Bis-Tris 용액에 4 mM p-toluenesulfonic acid와 100 μM EDTA를 포함한 반응 시약을 사용하였다. 검출은 전도도 검출기(conductivity detector, CDD)를 이용하여 수행하였고, 총 분석 시간은 30분이었다. 유기산 표준물질은 탈이온수에 용해하여 0.1-30 μg/mL 농도로 희석하였으며, 피크 면적을 기준으로 정량하였다.
시료 약 0.5 g을 칭량하여 분해 용기에 넣고, 65% 질산 7 mL를 가한 뒤 반응 가스를 제거하고, 2 mL의 과산화수소를 첨가 후, 분해 장치에서 분해하였다. 분해 후 실온에서 냉각한 뒤 증류수로 희석하여 잔류 산을 제거하였다. 1% 질산을 이용하여 최종 부피가 10 mL가 되도록 정용하여 미네랄 분석에 사용하였다.
전처리 시료는 유도결합플라즈마 질량분석기(ICP-MS, NexION 300, Perkin Elmer Co., Waltham, MA, USA)로 분석하였다.
DPPH (2,2-diphenyl-1-picrylhydrazyl) 라디칼 소거능은 Brand-Williams 등(1995)의 방법에 기초하여 분석하였다. 0.1 mM DPPH 용액을 100% 메탄올에 녹인 후, 암 조건에서 30분간 안정화시켜 반응용액으로 사용하였다. 시료 추출액 100 μL와 DPPH 용액 900 μL를 혼합하여 실온 암실에서 30분간 반응시킨 뒤, 생성된 색 변화에 대해 517 nm에서 흡광도를 측정하였다. 공시료는 메탄올을 동일 조건으로 처리하여 사용하였으며, 측정된 항산화 활성을 Trolox 표준물질로 작성한 검량선을 기반으로 μmol Trolox equivalents로 환산하여 표시하였다.
ABTS [2,2’-azino-bis (3-ethylbenzothiazoline-6-sulfonic acid)] 라디칼 소거능은 Re 등(1999)의 방법을 바탕으로 일부 수정하여 적용하였다. 7 mM ABTS 용액과 2.45 mM potassium persulfate를 동일한 부피 비율로 혼합한 뒤 암실에서 16시간 반응시켜 ABTS+ 라디칼을 형성하였다. 생성된 라디칼 용액은 인산 완충용액(pH 7.4)으로 희석하여 초기 흡광도 값이 0.70± 0.020이 되도록 조절한 후 사용하였다. 시료 추출액 100 μL와 ABTS+ 용액 900 μL를 혼합하여 6분간 실온에서 암반응시킨 후, 734 nm에서 흡광도를 측정하였다. 결과는 Trolox 표준물질로부터 작성한 검량선을 기준으로 μmol Trolox equivalents로 환산하여 표시하였다.
FRAP 환원력 분석은 Benzie와 Strain (1996)의 방법을 기반으로 수행하였다. 분석용 반응액은 300 mM acetate buffer (pH 3.6), 10 mM TPTZ (Tri-pyridyl-s-triazine) in 40 mM HCl, 20 mM FeCl3 ․ 6H2O 용액을 10:1:1 비율로 혼합하여 준비하였다. 시료 추출액 100 μL와 FRAP 반응액 900 μL를 혼합하여 37°C에서 30분간 반응시킨 후, 생성된 푸른색 착색물의 흡광도를 593 nm에서 측정하였다. 측정값은 Trolox 표준물질을 사용한 검량선에 따라 μmol Trolox equivalents로 환산하여 표시하였다.
3. 결과 및 고찰
감귤, 사과, 포도 껍질 분말의 일반성분을 분석한 결과, 모든 시료는 수분 함량이 9% 내외로 나타났으며(Table 1), 이는 저장성과 품질 안정성 측면에서 바람직한 수준으로 판단된다. 특히 포도 껍질 분말의 수분은 9.26%로, 상업용 포도 섬유 제품에서 제시된 수분 기준치인 9% 미만과 유사하였다(Karovičova 등, 2015). 조단백질 함량은 포도 껍질이 8.74%로 가장 높았고, 감귤껍질 5.83%, 사과껍질 2.68% 순으로 나타났다. 포도 껍질의 경우, 상업적 포도 섬유 제품에서도 단백질 함량이 8.6-10.8%로 보고된 바 있어 본 연구 결과와 일치하였다(Karovičova 등, 2015). 반면 감귤과 사과껍질은 상대적으로 단백질 함량이 낮은 특징을 보였다.
조지방은 포도 껍질에서 5.73%로 가장 높았고, 감귤껍질 1.57%, 사과껍질 0.92% 순으로 나타났다. 감귤껍질의 경우 기존 연구에서 9.74% 수준의 지방 함량이 보고된 바 있으나(Ani와 Abel, 2018), 이보다 낮은 수치는 품종, 건조 조건, 시료의 세척 ․ 분쇄 여부 등에 따라 차이가 발생할 수 있는 것으로 보인다. 회분 함량은 포도 껍질이 11.37%로 가장 높고, 감귤껍질은 8.40%, 사과껍질은 3.44%로 유의한 차이를 보였다. 포도 껍질은 미네랄 함량이 높은 것으로 알려져 있으며, 감귤껍질 역시 Citrus 속 과피에서 회분이 2.5% 내외로 보고되었으나, 본 연구에서는 보다 높은 수준이 확인되었다(Ani와 Abel, 2018).
탄수화물 함량은 사과껍질이 83.62%로 가장 높았고, 감귤껍질은 74.67%, 포도 껍질은 64.93%로 나타났다. 이는 사과껍질이 상대적으로 식이섬유 외의 당질(예: 단순당 및 다당류)이 높은 수준으로 존재함을 시사한다. 실제로 사과 껍질은 일반성분 분석에서는 탄수화물 함량이 71.0±2.30%로 보고되었으며, 이는 본 연구의 사과껍질 결과보다 낮지만, peel 단일 시료의 높은 탄수화물 특성을 보인다(Saeed 등, 2023). 또한, 감귤껍질과 비교할 때 Citrus maxima Merr. peel extract의 탄수화물 함량은 71.57±0.83%로 보고되었으며(Ani와 Abel, 2018), 본 연구의 감귤껍질(77.67%)보다 다소 낮아, 품종, 건조 방식, 시료 전처리 조건 등에 따른 변이가 존재할 수 있음을 시사한다.
감귤껍질, 포도 껍질, 사과껍질의 총식이섬유소 함량을 분석한 결과, 감귤껍질과 포도 껍질은 각각 51.45 g/100 g, 52.37 g/100 g으로 매우 높은 수준을 보였으며, 사과껍질은 20.57 g/100 g으로 상대적으로 낮은 값을 나타냈다. 포도 껍질의 경우, 적포도 껍질(red grape skin) 유래 분말 또는 포도박(grape pomace) 기반 소재에서도 총식이섬유가 50% 이상 보고된 바 있으며, 본 연구의 결과와 유사한 수준이다(Covaliov 등, 2024). 한편, 감귤껍질은 citrus류 과피 중에서도 특히 높은 식이섬유소 함량을 나타냈으며, 이는 기존 문헌에서 제시한 건조 감귤껍질의 총식이섬유 함량(약 57%)과 유사하거나 약간 낮은 수준이다(Nunez-Gomez 등, 2024). 일반적으로 감귤류 껍질은 펙틴, 헤미셀룰로오스, 셀룰로오스 등으로 구성된 불용성 식이섬유와 일부 수용성 식이섬유가 혼합되어 존재하며, 이는 제과 ․ 제빵용 식이섬유 보강 소재로서의 활용 가능성을 시사한다.
이와 같이 감귤껍질과 포도 껍질은 높은 식이섬유 함량을 바탕으로 대사 건강, 장 건강 개선, 혈당 반응 완화 등 여러 생리적 기능을 유발할 수 있는 유망한 식품소재로 평가된다. 특히, 섬유의 점도, 소화 효소에 대한 저항성, 장내 미생물에 의한 발효를 통해 생성되는 단쇄지방산은 인슐린 민감도 향상, 체중 조절, 혈중 콜레스테롤 및 혈압 감소에 기여하는 것으로 보고되었다(Bulsiewicz, 2023). 반면, 사과껍질은 식이섬유 함량이 상대적으로 낮은 대신, 항산화 성분과 당질이 풍부하여(Leontowicz 등, 2003) 항산화 강화나 풍미 부여 목적의 소재로 접근할 필요가 있다.
감귤, 사과, 포도 껍질 분말의 구성아미노산을 분석한 결과(Table 2), 세 시료 모두 아스파르트산, 글루탐산, 류신, 알라닌, 프롤린, 발린, 라이신 등의 함량이 높은 편이었으나, 상대적인 조성과 총함량에는 뚜렷한 차이를 보였다. 총아미노산 함량은 포도 껍질이 8,811.03±199.19 mg/100 g으로 가장 높았으며, 감귤껍질(5,701.53±135.12 mg/100 g), 사과껍질(2,743.77±83.44 mg/100 g) 순으로 유의적인 차이를 나타냈다(p<0.05). 포도 껍질의 경우 글루탐산(1,741.07 mg), 류신(676.43 mg), 알라닌(474.10 mg), 글리신(696.43 mg) 등의 함량이 높은 것이 특징으로, 포도 껍질의 경우 총아미노산이 8,811.03±199.19 mg/100 g으로 가장 높았으며, 특히 글루탐산, 류신, 글리신, 알라닌, 아르기닌 등의 비율이 풍부하였다(Table 2). 이는 포도박(grape pomace)의 아미노산 프로파일 분석에서 아스파르트산, 글루탐산 및 아르기닌이 가장 주된 아미노산 검출되었다는 연구 결과와 일치하며, 해당 성분들은 항산화 및 생리활성 기능과도 관련이 있는 것으로 보고되고 있다(Hanušovsky 등, 2023)
감귤껍질에서는 아스파르트산(1,099.57±32.41 mg/100 g), 글루탐산(631.47± 15.85 mg/100 g), 류신(398.23±9.81 mg/100 g), 알라닌(333.17±8.85 mg/100 g), 프롤린, 글리신 등이 주요 아미노산으로 확인되었다(Table 2). 이는 다양한 citrus peel 시료에서 프롤린, 아스파르트산, 알라닌, 세린, 아스파라진, 아르기닌 등이 가장 풍부한 주요 성분으로 보고된 기존 분석 결과와 일치한다(Wu 등, 2023). 이러한 아미노산 조성은 감귤류 특유의 산미와 풍미 형성에 기여할 뿐 아니라, 프롤린과 아르기닌은 피부 보습, 콜라겐 합성 촉진 등 화장품 및 생리활성 펩타이드 제조에도 활용 가능한 성분임을 시사한다(Koochi 등, 2023).
사과껍질은 전체적으로 아미노산 함량이 가장 낮았으며, 이는 원재료 자체의 단백질 농도가 상대적으로 낮고 열풍건조 과정에서 일부 아미노산이 열변성되거나 손실되었을 가능성도 있다는 점으로 설명될 수 있다. 본 연구에서는 아스파르트산(894.87±21.40 mg/100 g), 글루탐산(359.83±11.37 mg/100 g), 류신(133.77± 2.63 mg/100 g)이 주요 아미노산으로 나타났는데, 이는 리투아니아에서 재배된 10개 사과 품종의 peel 시료에서 자유형 아스파르트산이 약 370.78±18.54 μg/g dw(약 37 mg/100 g dw) 수준으로 다른 부위보다 낮게 존재하고, 전체 껍질의 아미노산 함량이 과육이나 전체 과일보다 낮았다는 보고와 유사하였다(Bračiulienė 등, 2025).
필수아미노산 중 류신, 발린, 아이소류신 등의 함량은 포도 껍질에서 각각 676.43 mg, 509.63 mg, 423.13 mg/100 g으로 가장 높았고, 감귤껍질도 비교적 높은 수준이었다(Table 2). 이들 분지 아미노산(BCAAs)은 특히 류신이 mTORC1 신호 전달을 활성화하여 근골격근 단백질 합성을 직접적으로 촉진하는 주요 유도 물질로 작용한다. 실제로 류신은 다른 필수아미노산보다 근육 단백질 합성을 더 강하게 유도하며, 운동 후 단백질 합성률을 유의하게 증가시키는 것으로 보고되었다(Zhao 등, 2021). 이를 포함한 BCAAs는 노인에서 근육량 감소(사코페니아) 예방 및 기능적 유지에 기여한다는 결과도 보고되었다(Ebrahimi-Mousavi 등, 2022). 특히 아르기닌은 포도 껍질에서 548.60 mg으로 가장 높았으며, 감귤껍질은 275.57 mg, 사과껍질은 94.60 mg으로 확인되었다. 아르기닌은 혈류 개선, 면역 조절, 성장 호르몬 촉진 등 생리활성이 높은 아미노산으로 기능성 식품 및 특수영양식에 적합한 성분이다(Al-Farsi와 Lee, 2008).
감귤, 사과, 포도 껍질 분말의 지방산 조성을 분석한 결과(Table 3), 각 시료는 포화지방산(SFA), 단일불포화지방산(MUFA), 다가불포화지방산(PUFA)의 비율에서 뚜렷한 차이를 나타냈다(Table 3). 먼저, 총포화지방산 함량은 감귤껍질이 24.07 ±0.51%, 사과껍질 23.70±0.53%, 포도 껍질 23.40±0.52%로 유사한 수준이었다. 이 중 palmitic acid (C16:0)는 세 시료 모두에서 가장 높은 비율의 포화지방산으로 검출되었으며, 특히 사과껍질(19.37±0.38%)이 감귤(18.47±0.23%)과 포도(16.10± 0.35%)보다 유의하게 높게 나타났다(p<0.05). Palmitic acid는 식물성 유지 및 세포막 구성에 필수적인 지방산으로, 식이성 지방산의 주요 구성 요소 중 하나로 알려져 있다(Saini와 Keum, 2018).
단일불포화지방산(MUFA) 함량은 감귤껍질(28.37±0.67%)이 가장 높았고, 사과껍질(27.00±0.72%), 포도 껍질(26.47± 0.49%) 순이었다. 주요 MUFA로는 oleic acid (C18:1n9)가 지배적 역할을 했으며, 감귤껍질의 경우 27.33±0.87%로 특히 비율이 높았다. Oleic acid는 심혈관 건강 증진 및 항염증 작용이 잘 알려져 있으며, 다양한 과피와 종자유에서도 주요 MUFA로 확인된 바 있다(Martin 등, 2020).
다가불포화지방산(PUFA) 중 linoleic acid (C18:2n6)는 전체 PUFA의 상당 부분을 구성하며, 포도 껍질에서 47.93±1.05%로 가장 많이 검출되었다. 사과껍질은 45.63±1.15%, 감귤껍질은 40.00±0.95%로 나타났다(p<0.05). Linoleic acid는 오메가‑6 계열의 필수지방산으로, 세포막 유동성 유지, 염증 반응 조절, 에이코사노이드 전구체로의 기능 등 생리활성 유지에 필수적인 역할을 수행한다(Innes와 Calder, 2018; Martin 등, 2020). 특히 감귤껍질은 α‑linolenic acid (C18:3n3) 함량이 7.57±0.21%로, 분석된 세 시료 중 가장 높은 수준을 보였다. 이러한 조성은 다양한 감귤류 껍질 오일에서 오메가‑3 지방산이 상대적으로 풍부하게 존재한다는 실증 분석 결과와 일치하며, 이는 체내 염증 반응 완화, 혈관 기능 개선, 세포막 유동성 조절 등 항염증 및 심혈관 보호 작용과 관련이 높으며, PUFA 내 오메가-3 비율을 향상시키는 소재로서 감귤껍질의 기능성이 강조될 수 있다(Innes와 Calder, 2018).
총다가불포화지방산(Total PUFA) 함량은 포도 껍질이 53.27± 1.21%로 가장 높았고, 사과껍질(49.23±1.07%), 감귤껍질(47.57± 1.29%) 순으로 확인되었다. 포도 껍질은 총지방산 중 불포화지방산 비율이 높고, linoleic acid 및 arachidic acid 함량이 상대적으로 우수하여, 항산화 및 항염 기능성 식품소재로서 활용 가치가 높을 것으로 판단된다. 결과적으로, 포도 껍질은 총불포화지방산 비율이 가장 높고, linoleic acid 중심의 조성이 돋보여 항산화 및 기능성 식품소재로서의 가치가 크다. 감귤껍질은 oleic acid 및 α‑linolenic acid가 균형 있게 존재하여 심혈관 건강과 항염 기능을 기대할 수 있으며, 사과껍질은 palmitic acid와 linoleic acid 중심의 조성으로 식이 지방 공급원으로 활용 가능하다.
과피껍질(감귤, 사과, 포도)의 유리당 함량 측정 결과는 Table 4와 같다.
총유리당 함량은 사과껍질이 43.00±1.06 g/100 g으로 가장 높았으며, 감귤껍질은 15.03±0.33 g/100 g, 포도 껍질은 13.57± 0.37 g/100 g로 유의미하게 낮았다(p<0.05). 이러한 사과껍질의 높은 유리당 함량은 apple peel extract가 대사증후군 동물모델에서 혈당 조절 및 지질 개선에 긍정적인 효과를 나타냈다는 보고와도 일치한다(Popiolek-Kalisz 등, 2023). 특히 사과껍질의 과당(fructose) 함량은 26.17±0.64 g/100 g, 포도 껍질은 8.63±0.25 g/100 g, 감귤껍질은 7.53±0.15 g/100 g으로, 과당이 다른 당류보다 월등히 많았다. 일반적인 사과 품종에서도 과당이 가장 높은 자유당으로 나타난다는 연구 결과와 일치하며, 이는 본 연구 결과의 신뢰성을 높인다(Miuţa 등, 2016).
포도 껍질은 자당(sucrose)이 거의 검출되지 않았고, 과당과 포도당(glucose, 4.63±0.12 g/100 g)이 주요 단당류였다. 이는 포도 박(peel) 또는 pomace에서 자당은 invertase에 의해 과당과 포도당으로 대부분 분해된다는 일반적인 식물 내 당 대사 특성과 일치한다(Ma 등, 2020). 감귤껍질에서도 과당(fructose)과 포도당(glucose)이 주요 유리당으로 존재하였으며, 이는 citrus peel 특유의 신선한 단맛과 산미의 균형을 형성하여 풍미를 조절하는 주요 성분으로 작용할 수 있다. 실제로 orange peel이나 grapefruit peel에서는 glucose, fructose, sucrose 등이 주요한 수용성 당으로 구성되며, 특히 sucrose 함량이 상대적으로 낮고 glucose와 fructose의 비율이 높은 경향이 있다는 보고가 있다(Rivas 등, 2020).
그 외 셀로비오스(cellobiose), 만노오스(mannose), 갈락토오스(galactose), 리보스(ribose) 등은 일부 시료에서 미량 수준(trace)으로만 검출되었고, 락토스(lactose)는 어느 시료에서도 검출되지 않았다. 이는 이러한 당류들이 주로 식물 세포벽 구성 다당류의 가수분해 부산물로 존재하거나, 자연 상태에서는 극미량 존재하는 구조당임을 시사한다(Willats 등, 2001). 사과껍질은 유리당 조성이 풍부하여 풍미 개선 및 감미 보완 소재로 활용 가능성이 높고, 감귤과 포도 껍질은 저당 기능성 음료나 제과 등 당류 조절 식품의 소재로 응용 가능성이 있다. 특히 감귤껍질은 산미와 단맛의 균형을 제공하는 감미 및 풍미 조성 소재로 주목되며, citrus peel powder는 제과 제품에서 감미와 향미를 동시에 강화시키는 데 활용된 바 있다(Popiolek-Kalisz와 Glibowski, 2023).
감귤, 사과, 포도 껍질 분말의 유기산 함량 분석 결과(Table 5), 총유기산 함량은 사과껍질에서 975.90±19.14 mg/100 g으로 가장 높았으며, 감귤껍질은 876.17±21.54 mg/100 g, 포도 껍질은 468.17±12.04 mg/100 g 순으로 나타났다(p<0.05). 각 시료별로 특징적인 유기산 조성이 관찰되었으며, 이러한 유기산은 풍미 형성 외에도 항산화, 보존성 향상, 대사조절 등 기능성 효과를 지닌다. 감귤껍질에서는 구연산(508.20±11.48 mg/100 g)가 가장 높은 비율을 차지하였으며, 사과산(217.53±6.04 mg), 수산(49.83±1.10 mg), 젖산(19.47±0.51 mg), 초산(21.37 ±0.45 mg)이 뒤를 이었다. 이러한 조성은 citrus peel을 대상으로 한 기존 연구에서도 구연산과 사과산이 우세하게 존재하며 수산, 호박산, 구연산 등도 검출되었다는 보고와 일치한다(Rivas 등, 2020; Bar-Ya’akov 등, 2019).
사과껍질의 유기산 조성을 분석한 결과, 총유기산 함량은 975.90±19.14 mg/100 g으로 감귤껍질(876.17±21.54 mg/100 g)과 포도 껍질(468.17±12.04 mg/100 g)보다 유의하게 높게 나타났다(p<0.05). 그 중 사과산이 875.87±17.61 mg/100 g으로 전체 유기산의 90% 이상을 차지하였으며, 이는 사과의 주요 산미 성분으로서의 사과산의 주된 성분임을 알 수 있다. 사과산은 자연적으로 존재하는 유기산 중 하나로, 특히 사과, 자두, 살구 등에서 산미의 핵심을 구성하며, 식품 내에서 신맛의 강도, pH 조절, 킬레이트 형성능 및 저장 안정성에도 영향을 준다. 사과껍질에 포함된 사과산은 단순한 풍미 조성 이외에도, 위액 분비 촉진, 금속 이온 킬레이션, 항피로 작용, 운동 후 회복 기능 등의 생리적 효능이 보고되어 있다(Sharma 등, 2016). 또한, 사과의 유기산 조성은 품종, 재배지 고도, 성숙도 및 저장조건에 따라 크게 달라질 수 있다. 특히 유럽에서 재배된 재래 사과 품종을 분석한 Oszmianski 등(2020)의 연구에서도, 사과산이 총유기산의 대부분을 차지하며, 일부 품종에서는 구연산 및 구연산이 미량으로 동반되는 양상을 보였다. 이와 같은 경향은 본 연구의 사과껍질 시료에서도 유사하게 확인되었다(Oszmiański 등, 2020). 초산도 사과껍질에서 62.97±1.50 mg/100 g으로 검출되었는데, 이는 발효 관련 작용 또는 생합성 경로에서 형성된 이차 유기산일 가능성이 있다. 특히 apple cider production에서 흔히 검출되는 휘발성 유기산 중 하나로, 풍미 및 산미 조절에 기여할 수 있다. 반면, 사과껍질에서는 수산, 호박산, 젖산, 아디프산(adipic acid) 등이 감귤이나 포도 껍질에 비해 거의 검출되지 않거나 검출한계 이하였으며, 이는 사과의 유기산 조성이 특정 산에 매우 집중되어 있음을 시사한다. 또한, 유기산의 절대량뿐만 아니라 비율 역시 기능성 소재 개발 시 중요하게 고려되어야 한다. 사과산 중심의 조성은 강한 산미보다 완만한 신맛을 유도하며, 이는 가공식품의 신맛 조절이나 음료류의 산미 밸런스에 있어 유리한 특성이다.
포도 껍질에서 확인된 주요 유기산은 아디프산(134.57±3.10 mg/100 g), 초산(80.50±2.52 mg/100 g), 사과산(125.83±3.59 mg/100 g), 구연산(45.97±1.11 mg/100 g) 등이었다. 특히 adipic acid와 초산은 다른 과일 껍질에 비해 높은 수준으로 검출되었으며, 이는 포도 껍질이 숙성과 저장 또는 자연 발효 과정을 거치면서 다양한 유기산이 축적되기 때문인 것으로 보인다. 사과산과 구연산은 포도류 과일에서 산미 형성과 저장 중 pH 안정성에 관여하는 대표적인 산으로, wine과 grape juice의 품질 결정에 핵심적인 영향을 미치는 성분이다(Tikhonova 등, 2021). Tikhonova 등(2021)의 연구에 따르면, 다양한 유럽 품종의 grape pomace에서도 구연산이 주요 유기산으로 검출되며, 그 외에도 사과산, 초산, 호박산, 구연산 등이 품종별로 상이한 비율로 존재하였다. 이러한 유기산의 다양성과 농도 차이는 포도 껍질의 항산화 능력, 풍미 형성, 미생물 저해력 등 기능성 특성에 영향을 준다. 특히, 유기산은 polyphenol과 상호 작용하여 식품 내 pH 조절, 색소 안정화, 항균 작용 등 다중 기능을 발휘하며, 자연 유래 식품 보존제, 발효 음료용 산미 조절제, 기능성 첨가 소재로의 응용 가능성이 제시되고 있다(Tikhonova 등, 2021).
포도 껍질은 단독으로도 다양한 유기산을 함유하고 있지만, 사과껍질과의 복합 활용(co-fermentation)을 통해 풍미와 기능성을 더욱 강화할 수 있다. Wang 등(2025)은 사과 및 포도 pomace를 혼합하여 발효시켰을 때, 포도는 주로 색소와 구연산, 사과는 사과산과 향미 물질을 제공하여 최종 발효제품의 품질과 안정성을 향상시킨다고 보고하였다. 이처럼 껍질 기반 바이오소재의 복합 활용은 기존 단일 과일 기반 소재에 비해 유기산 스펙트럼과 감각적 특성을 넓힐 수 있어, 발효 음료, 발효소스, 저당 발효식품 등 다양한 가공식품에서의 활용 가치가 매우 높다.
감귤, 사과, 포도 껍질 분말의 미네랄 조성을 비교한 결과(Table 6), 총미네랄 함량은 감귤껍질이 138.48±3.16 mg/100 g, 포도 껍질이 138.03±2.00 mg/100 g, 사과껍질이 83.80±1.84 mg/100 g으로 나타났으며, 감귤과 포도는 유의적 차이 없이 높은 수준이었고 사과는 상대적으로 낮았다(p<0.05). 칼륨(K) 함량은 포도 껍질이 114.29±1.45 mg/100 g으로 가장 높았고, 감귤(85.19 mg), 사과(72.51 mg) 순이었다. 칼륨은 체내 나트륨-칼륨 펌프 조절과 혈압 조절, 수분 균형 유지 등에 필수적인 미네랄로, 특히 포도 껍질은 고칼륨 식품소재로서의 활용 가능성이 높다. 이는 포도 껍질이 와인 제조 후 남는 잔여물임에도 불구하고 주요 미네랄이 풍부하게 유지된다는 보고와 일치한다(Ribereau-Gayon 등, 2006). 칼슘(Ca)의 경우 감귤껍질이 41.82± 0.93 mg/100 g으로 가장 높았고, 포도 껍질(9.78 mg), 사과껍질(4.21 mg)은 상대적으로 낮은 함량을 보였다. 감귤류 과피는 펙틴, 식이섬유, 플라보노이드와 함께 칼슘 결합 능력이 높은 것으로 알려져 있으며, 이로 인해 제과류나 기능성 음료에서 천연 칼슘 강화소재로 응용될 수 있다(Sharma 등, 2016).
마그네슘(Mg)은 포도 껍질에서 11.79±0.28 mg, 감귤에서 7.92 mg, 사과에서 3.63 mg으로 분석되었으며, 이 역시 포도 껍질이 가장 높은 함량을 나타냈다. 마그네슘은 ATP 대사, 신경전달, 근육 수축, 단백질 합성 등에 관여하는 필수 미네랄로, 심혈관계, 골격계 및 면역기능 유지에 중요하며, 고기능성 식품소재 개발 시 유리한 성분이다(Volpe, 2013). 철(Fe) 함량은 포도 껍질이 1.40±0.03 mg/100 g으로 가장 높았으며, 감귤과 사과는 각각 0.28, 0.24 mg 수준이었다. 포도 껍질은 red grape 품종에서 안토시아닌 및 폴리페놀 함량뿐만 아니라 철, 아연, 마그네슘 등 미량 미네랄도 풍부하다는 특성이 있어, 철분 보충용 자연식 소재로의 가능성이 있다(Maier 등, 2009; Llobera와 Canellas, 2007). 아연(Zn)은 포도 껍질이 0.09±0.01 mg/100 g, 사과 및 감귤껍질이 각각 0.04 mg 수준으로 나타났다. 아연은 면역 조절, 세포 성장, 상피조직 유지 및 수많은 효소의 보조인자로 작용하는 필수 미량원소이며, 특히 어린이 성장, 감염 예방, 피부 회복 등과 관련해 기능성 음료 및 강화 식품소재로 주목되고 있다(King 등, 2015). 특이하게도, 사과껍질에서는 망간(Mn)과 구리(Cu)가 각각 미검출(ND) 및 극미량(trace) 수준으로 분석되었으며, 이는 시료 품종, 재배 토양의 미네랄 농도, 성숙도, 수확 시기, 또는 열풍건조 등 가공 공정에 따른 미량원소의 손실로 해석된다(Kalt, 2005).
종합적으로 볼 때, 감귤껍질은 Ca 중심의 미네랄 강화 소재, 포도 껍질은 K, Mg, Fe, Zn 등 다양한 미네랄을 함유한 복합 기능성 소재, 사과껍질은 풍미나 다른 기능성 성분에 비중을 둔 소재로 분류할 수 있다. 따라서 미네랄 기능성을 보강하고자 하는 목적에 따라 껍질의 종류를 달리 적용하는 전략이 유효하다.
Fig. 1은 감귤, 사과, 포도 껍질 분말의 항산화 활성을 DPPH 라디칼 소거능, ABTS 라디칼 소거능, FRAP 환원력지표로 μmol TE 단위로 제시한 것이다. 모든 시료에서 FRAP 값이 DPPH와 ABTS보다 뚜렷하게 높아 환원력(single electron transfer, SET기반) 지표가 라디칼 소거(hydrogen atom transfer, HAT/SET 혼합) 지표보다 민감하게 반응했음을 시사한다(Munteanu와 Apetrei, 2021; Sadeer 등, 2020). 또한 과일의 종별 순위는 DPPH에서는 사과 > 감귤 > 포도 순이었고, ABTS에서는 사과가 가장 높으며 포도는 중간 수준으로 사과 ․ 감귤과 부분적으로 겹치는 군을 형성하였다. 반면 FRAP에서는 감귤과 포도가 최상위(a), 사과가 상대적으로 낮게 나타났다(p<0.05). 이는 DPPH ․ ABTS ․ FRAP의 반응기작 차이(지질/수용 상용성, 라디칼 접근성, 전자공여 능력)와 각 과피의 주요 항산화 조성 차이를 반영하는 결과로 해석된다(Munteanu와 Apetrei, 2021; Sadeer 등, 2020).
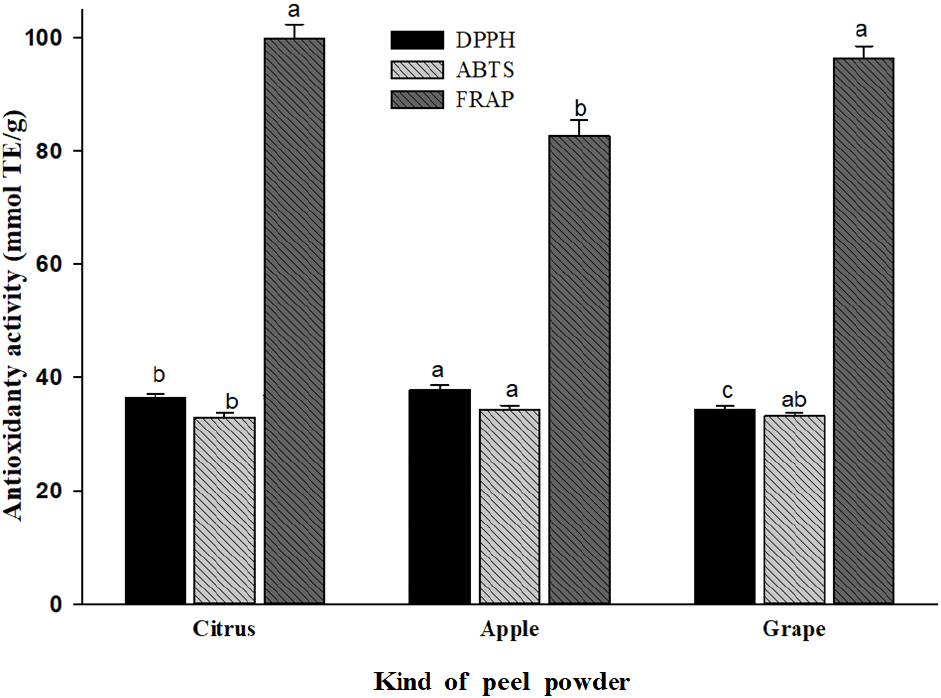
감귤 껍질은 FRAP에서 포도와 같이 가장 높게 나타나 강한 전자공여 ․ 환원력을 나타냈다. 감귤 과피에는 hesperidin ․ narirutin과 같은 플라바논 배당체와 폴리메톡시플라본이 풍부하며, 총페놀 및 주요 플라보노이드가 ABTS ․ DPPH ․ FRAP와 높은 양의 상관을 보인다는 보고가 다수 제시되어 본 연구의 패턴과 부합하였다(Kovačević 등, 2023). 특히 만다린계 과피에서 플라보노이드가 과육보다 높은 수준으로 축적되고, 환원력 지표에 크게 기여한다는 점이 확인되어 왔다(Kovačević 등, 2023).
사과 껍질은 DPPH와 ABTS에서 가장 높게 나타났다. 사과 과피에는 퀘르세틴 배당체(플라보놀)와 디하이드로칼콘(플로리진)이 과육보다 현저히 높게 존재하며, 라디칼 소거 중심 지표에서 우수한 활성을 보인다고 보고되었다(Asma 등, 2023; Butkeviciute 등, 2022). 본 연구에서 사과의 FRAP가 감귤 ․ 포도보다 낮은 양상은, 사과 과피의 주된 플라보놀류가 전자공여(SET) 지표보다는 라디칼 소거 지표에서 더 강하게 반응하는 경향과 일치하였다(Asma 등, 2023).
포도 껍질은 FRAP에서 가장 높게 나타났지만, DPPH에서는 상대적으로 낮게 나타났다. 적색 포도 과피는 안토시아닌(malvidin-3-glucoside)과 flavonols (quercetin derivatives), 일부 stilbenes (resveratrol)의 저장고로 알려져 있으며, 과피 분획은 환원력 지표(TEAC/FRAP)에서 높게 나타난 것으로 보고되었다(Chengolova 등, 2023; Zhou 등, 2022).
4. 요약
본 연구에서 감귤(citrus), 사과(apple), 포도(grape) 껍질 분말의 일반성분 분석 결과, 세 시료 모두 수분 함량이 9% 내외였으며, 포도 껍질은 조단백질(8.74%)과 조지방(5.73%)이 가장 높았고, 감귤과 포도 껍질은 식이섬유 함량이 50 g/100 g 이상으로 확인되었다. 아미노산 조성에서는 포도 껍질이 총8,811.03 mg/100 g으로 가장 높았으며, 류신, 발린, 글루탐산 등의 함량이 풍부하였다. 지방산은 세 시료 모두 불포화지방산이 우세하였고, 감귤껍질은 α-linolenic acid 함량이 가장 높았다. 유리당 분석에서는 사과껍질이 총당 43.00 g/100 g으로 가장 많았으며, 과당 중심의 조성을 보였다. 유기산은 사과껍질은 사과산, 감귤껍질은 구연산, 포도 껍질은 adipic 및 구연산이 높았다. 미네랄 조성은 포도 껍질이 K, Fe, Zn이 풍부하였고, 감귤껍질은 Ca 함량이 높았다. 감귤, 사과, 포도껍질 분말의 항산화 활성(DPPH, ABTS, FRAP) 의 경우 모든 시료에서 FRAP 값이 DPPH ․ ABTS보다 높았으며, 사과는 DPPH ․ ABTS에서, 감귤과 포도는 FRAP에서 높았다. 전체적으로 감귤껍질은 식이섬유와 칼슘이 높았으며, 사과껍질은 탄수화물과 유기산이 풍부하였고, 포도 껍질은 영양소 함량과 항산화 활성이 우수하게 나타나 3가지 과일 껍질(감귤, 사과, 포도) 모두 영양성분을 다량 함유하며, 항산화 활성이 높은 소재이므로 이들을 활용한 고부가가치 식품 개발이 가능함을 시사한다. 본 연구의 한계점으로 단지 분석 결과를 서술하였으며, 다변량 통계를 통한 3가지 샘플간의 의미 있는 패턴을 분석하지 못하였다. 향후 패턴분석을 통하여 목적에 따라 과일껍질의 종류를 달리 적용하는 전략이 유효할 것으로 사료된다.
