Article
뽕나무 버섯균에 의한 꾸지뽕 열매의 액체발효 중 영양성분 및 생리활성 성분의 변화
Changes in nutritional and bioactive constituents of liquid fermentation of kujippong (Maclura tricuspidata) fruits by Armellaria mellea
Dae-Woon Kim
1
, Tae-Young Kim
1
, Young-Hoi Kim
1
, Myung-Kon Kim
1,*
1Department of Food Science and Technology, Jeonbuk National University, Jeonju 54896, Korea
2Hansan F&G, Suwon 16433, Korea
Citation: Kim DW, Kim TY, Kim YH, Kim MK. Changes in nutritional and bioactive constituents of liquid fermentation of kujippong (Maclura tricuspidata) fruits by Armellaria mellea. Korean J Food Preserv, 29(2), 208-221 (2022)
Copyright © The Korean Society of Food Preservation. This is an Open-Access article distributed under the terms of the
Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/4.0/) which permits
unrestricted non-commercial use, distribution, and reproduction in any
medium, provided the original work is properly cited.
Received: Oct 13, 2021; Revised: Nov 26, 2021; Accepted: Dec 06, 2021
Published Online: Apr 30, 2022
4. 요약
꾸지뽕 열매를 이용하여 건강기능성 소재로 개발 가능성을 탐색하기 위하여 꾸지뽕 열매를 뽕나무 버섯균으로 10일간 액체발효시키면서 발효기간에 따른 일반성분 및 생리활성성분의 변화를 조사하였다. 꾸지뽕 열매를 뽕나무버섯균으로 발효시켰을 때 pH는 거의 변화가 없었으나, 가용성 고형분, 유리당(glucose, fructose) 및 유리 아미노산 함량은 발효기간이 경과함에 따라 지속적으로 감소된 반면, 총아미노산 함량은 뚜렷한 변화가 없었다. HPLC 분석에서 검출된 5종의 phenolic acid 및 flavonoid류 중에서, 양적으로 많이 함유된 chlorogenic acid는 발효가 진행됨에 따라 큰 폭으로 감소한 반면, chlorogenic acid의 가수분해 생성물인 caffeic acid 함량은 증가하였다. Parishin A, B 및 C의 함량은 발효시작 후 4일이 경과할 때까지는 큰 변화가 없었으나, 6-10일이 경과한 시점에서는 큰 폭으로 감소하였다. Parishin A, B 및 C가 가수분해되어 생성되는 gastrodin은 발효 6일까지 뚜렷한 변화가 없었지만 발효 10일까지는 약간 감소하였으며, gastrodin이 가수분해되어 생성되는 6일 이후에 4-HBA가 뚜렷하게 증가하였다. 뽕나무 버섯균에 의한 꾸지뽕 열매의 발효과정에서 parishin 유도체들의 생물변환 메카니즘을 구명하기 위하여, 뽕나무버섯 배양액에서 분리한 조효소 및 Rhizopus oryzae에서 유래하는 esterase를 parishin A와 반응시킨 결과, parishin A는 뽕나무버섯균이 분비하는 esterase의 작용에 의해 parishin B와 parishin C를 거쳐 gastrodin으로 변환된 다음, β-배당체인 gastrodin도 역시 뽕나무버섯균이 분비하는 β-glucosidase에 의해 가수분해되어 4-HBA로 생물변환되는 것으로 규명되었다. 특히 4-HBA는 인체 중추신경계에 긍정적인 효과를 주는 것으로 밝혀져 있을 뿐만 아니라, 비만과 관련된 효소들의 활성억제 효과도 있는 것으로 보고되어 있어서, 뽕나무 버섯균에 의한 발효 꾸지뽕 열매의 기능성과 이용성에 대한 추가 연구가 필요할 것으로 판단된다.
Abstract
Ripe fruit of Maclura tricuspidata has been traditionally used as a raw material for the preparation of fermented foods such as wine and vinegar in Korea. This studies were carried out to investigate changes of nutritional (soluble solids, free sugars and free and total amino acid composition) and bioactive constituents (phenolic compounds and parishin derivatives) during the liquid fermentation of M. tricuspidata fruits with Armillaria mellea (honey mushroom). The soluble solid, free sugars and free amino acids were gradually decreased during fermentation while meaningful changes of pH and total amino acids did not observed even after 10 day fermentation. The content of phenolic acids, particularly chlorogenic acid and parishin derivatives were decreased while that of caffeic acid and 4-hydroxybenzyl alcohol (4-HBA) were increased during the 10 day fermentation period. The crude enzyme preparation from liquid culture of A. mellea biotransformed parishin A into 4-HBA via parishin B, parishin C and gastrodin with high transformation ratio. Based on the results above, we discovered that parishin A and its derivatives are transformed into 4-HBA via parishin B, parishin C and gastrodin by esterase and β-glucosidase secreted by the mushroom mycelia during fermentation.
Keywords: Maclura tricuspidata fruits; Armillaria mellea; liquid fermentation; parishin derivatives; 4-hydroxybenzyl alcohol
1. 서론
뽕나무과에 속하는 꾸지뽕나무[Maclura tricuspidata (Carr.) Bureau ex Lavallee= formerly Cudrania tricuspodata]는 모든 부위(잎, 뿌리, 껍질, 목질부 및 열매)를 오래전부터 약용 또는 식용으로 이용하여 왔다. 민간처방에서 꾸지뽕나무의 잎은 습진, 폐결핵, 관절염, 만성 요통 등의 치료에 이용됐으며, 껍질과 열매는 강장, 중풍, 이뇨, 진해 등의 완화 또는 개선 제로 이용되어 왔다(Choi 등, 2013; Park 등, 1992). 그동안 꾸지뽕나무의 효능과 생리활성 성분에 관하여 많은 연구가 수행됐으며, 다양한 구조를 가진 prenylated xanthone 계열 화합물들이 함유되어 있는 것으로 밝혀졌다(Han 등, 2009; Xin 등, 2017; Zou 등, 2005). 또한, 꾸지뽕나무의 추출물이나 추출물에서 분리한 성분들의 생리활성과 관련하여 prenylated xanthone 계열 화합물들의 α-glucosidase 저해 활성(Seo 등, 2007), 항산화 활성(Jeong 등, 2009; Lee 등, 2009), 항균활성(Fukai 등, 2005; Kim 등, 2008), 간 보호 효과(Tian 등, 2005), 혈중 지질 감소효과(Cha 등, 2000)에 관한 연구결과들이 보고되었다. 또한, 꾸지뽕나무 열매(이하 꾸지뽕 열매)의 생리활성과 관련해서는 꾸지뽕 열매 추출물의 항산화 활성(Kang 등, 2011), angiotensin Ⅰ-converting enzyme(ACE)에 대한 저해활성(Youn과 Kim, 2012), prenylated isoflavone류의 monoamine oxidase 저해활성(Han 등, 2005), 당단백질들의 알레르기성 염증인자인 histamine 및 cycloocygenase(COX)-2 활성 억제효과(Oh 등, 2009)에 관한 연구결과들이 보고되어 있다.
또한, 완숙한 꾸지뽕 열매는 선명한 붉은색을 띄면서 유리당 함량이 높을 뿐만 아니라, 다양한 휘발성 성분들로 구성된 독특한 향기를 지니고 있어, 적절한 방법으로 가공한다면 기능성 소재로써 이용성을 증대시킬 수 있는 잠재력을 지니고 있다(Kim 등, 2019). 이와 같은 꾸지뽕 열매의 이용성 증대를 목적으로 여러 가지 방법들이 검토가 되었으나, 그 중에서도 특히 각종 미생물에 의한 발효를 통한 품질 및 생리활성 증대를 위한 연구들이 많이 수행되었다(Kang 등, 2011; Kim 등, 2020; Yim 등, 2015). 최근에 보고된 연구 결과에서, 효모(Saccharomyces cerevisiae)에 의한 꾸지뽕 열매의 알코올 발효 및 초산균에 의한 초산발효 제품이 세포 내 지방축적 억제와 항당뇨 활성을 지니고 있다는 것이 밝혀졌으며(Park 등, 2020), 특히 지방축적 억제 및 항당뇨 효과와 관련된 효소들의 활성을 억제하는 성분 중의 하나가 gastrodigenin이라고도 부르는 4-hydroxybenzyl alcohol(4-HBA)이다(Choi 등, 2018). 4-HBA는 꾸지뽕 열매에서 유리형으로 일부 존재하지만, 그 외 대부분은 글루코스와 결합한 배당체인 gastrodin[4-(β-D-glucopyranosyloxy) benzyl alcohol] 또는 gastrodin 3분자가 유기산인 citric acid와 에스테르 결합한 parishin A[tris(4-(β-D-glucopyranosyloxy)benzyl)citrate] 및 그 외 유도체 형태로 존재한다는 것이 밝혀져 있다(Kim 등, 2019). 4-HBA, gastrodin 및 parishin 유도체들은 생약재인 천마에 많이 함유되어 있으면서 천마의 약리효과와 밀접한 관련이 있는 주요 생리활성 물질들이다(Jia 등, 2014: Taguchi 등, 1981; Tang 등, 2014). 천마는 한방에서 전통적으로 두통, 현기증, 항경련, 수족마비, 중풍 등 신경계 질환의 예방과 치료를 목적으로 이용이 되어 왔는데, 이러한 활성은 주로 천마에 함유된 parishin 유도체들과 그의 가수분해 생성물인 gastrodin과 4-HBA에 기인한다(Chen과 Sheen, 2011; Jang 등, 2015). 이러한 parishin 유도체들은 유산균, 효모, 초산균과 같은 미생물에 의한 발효과정에서 용이하게 가수분해되어 아글리콘인 4-HBA를 생성한다(Kim, 2021; Song 등, 2017).
한편, 담자균류에 속하는 버섯균이나 버섯균에서 분리한 효소들도 생리활성 물질의 생물변환에 자주 이용된다(Bentil 등, 2021; Olicon-Hernandez 등, 2017). 이와 같은 버섯균들은 식물 다당체나 페놀화합물들을 가수분해, 산화 및 생물변환시킬 수 있는 다양한 효소류를 분비한다(Buswell 등, 1996; Kulikova 등, 2011; Kulikova 등, 2014; Singh과 Singh, 2014). 특히 뽕나무 버섯균은 활성이 강한 esterases와 glycoside hydrolase들을 분비한다(Bragaloni 등, 1997; Ertunga 등, 2014). 따라서 본 연구에서는 꾸지뽕 열매의 이용성 증대를 목표로 꾸지뽕 열매를 뽕나무 버섯균으로 액체발효를 시키면서 발효과정에서 일반성분(가용성 고형분, 유리당, 아미노산) 및 생리활성 성분들(polyphenols, parishin 유도체)의 변화를 조사코자 하였다. 특히 최근에 꾸지뽕 열매에는 분자구조 내에 아글리콘으로서 4-HBA를 함유하는 다수의 parishin 유도체들이 함유가 되어 있는 것으로 밝혀졌기 때문에, 발효과정에서 parishin 유도체들이 4-HBA로 생물변환 구조를 구명하고자 하였다.
2. 재료 및 방법
2.1. 재료
본 실험에서 사용한 꾸지뽕 열매는 2018년 10월 전북 순창지역에서 재배한 것을 구입하여 사용하였다. 시료는 이물질을 제거하고 과육이 골고루 완숙한 것만을 선별하여 동결건조한 다음 분쇄한 후, −20°C 이하의 냉동실에 보관하면서 사용하였다.
2.2. 시약
분석용 표준품으로 사용한 당류(glucose, fructose, maltose, sucrose), phenolic acid 및 flavonoid류(gallic acid, protocatechuic acid, chlorogenic acid, caffeic acid, isovanillic acid, p-coumaric acid, ferulic acid, trans-coumaric acid, trans-cinnamic acid, quecertin, kaempferol), 4-HBA 및 Rhizopus oryzae esterase는 Sigma-Aldrich사(St. Louis, MO, USA) 제품을 구입하여 사용하였다. Gastrodin과 parishin 유도체(parishin A, B, C 및 E)는 Chengdu Biopurify Phytochemicals Ltd(Chengdu, Sichuan, China)에서 구입하여 사용하였다. 아미노산 표준품 혼합물(physiological fluids standard mixture)은 Sykam GmbH (Eresing, Germany)사에서 구입하여 사용하였다. HPLC용 용매로써 deionized water, acetonitrile, ethanol(EtOH), methanol (MeOH)은 J. T. Baker사(Avantor Performance Materials, LLC, Radnor, PA, USA) 제품을 사용하였고, 기타 시약은 특급을 Daihan Scientific Co., Ltd.(Wonju, Kangwon, Korea)에서 구입하여 사용하였다.
2.3. 뽕나무 버섯균에 의한 꾸지뽕 열매의 발효
꾸지뽕 열매 발효를 위한 뽕나무 버섯 종균은 다음과 같이 준비하였다. 즉, 미리 당화시킨 맥아배지(11 °Brix) 약 400 mL를 2 L 용량의 삼각 플라스크에 넣고, 한천배지에서 고체배양한 뽕나무 버섯 종균(Armellaria mellea)을 접종한 다음 25-26°C에서 10일간 진탕배양하여 액체 종균을 준비하였다. 이어서 냉동한 생 꾸지뽕 열매를 실온에서 해동시킨 시료(1 kg)에 물 3 L를 가하고, 가정용 믹서(Shinil Industrial Co., Ltd. Cheonan, Chungnam, Korea)로 30초간 마쇄한 시료 200 mL씩을 500 mL 용량의 삼각 플라스크에 넣고 멸균(121°C, 20분)하였다. 멸균한 시료는 상온으로 냉각하고, 미리 준비한 액체배양 종균을 시료에 대해서 각각 5%씩 접종한 다음, 상온에서 10일간 배양하면서 2일 간격으로 시료를 채취하였다. 채취한 시료는 동결건조 및 분쇄한 다음, −20°C에서 보관하면서 이후 실험에 사용하였다.
2.4. 뽕나무 버섯균 배양액에서 조효소의 분리
미리 당화시킨 맥아배지(11 °Brix) 약 400 mL를 2 L 용량의 삼각 플라스크에 넣고 뽕나무버섯 종균을 접종한 다음 25-26°C에서 10일간 진탕배양하였다. 배양액은 균사체와 육즙을 분리하지 않고 가정용 믹서로 30초간 마쇄한 다음 원심분리(12,000 ×g, 20분)하였다. 이어서 상등액은 Upadhyaya 등(2015)의 방법에 따라서 30-80% 범위의 ammonium sulfate 침전 분획만을 분리한 후, 초산 완충용액(10 mM, pH 7)을 외액으로 하여 24시간 투석시킨 다음 원심분리(12,000 ×g, 20분)하였다. 상등액만을 취하여 동결건조한 다음 −70°C의 냉동고에 보관하면서 실험에 사용하였다.
2.5. 유리당 조성 분석
동결 건조한 각각의 발효시료 분말 1 g과 60% EtOH 10 mL를 cornical tube(15 mL)에 넣고 20분간 초음파 처리한 다음 원심분리하여 상등액을 회수하였다. 이어서 잔사는 동일한 방법으로 2회 더 추출하여 얻어진 상등액을 합하여 감압농축한 다음, 증류수 10 mL에 용해시킨 후 membrane filter(0.45 μm)로 여과하여 분석에 사용하였다. 유리당 조성은 HPLC를 이용하여 분석하였다. HPLC 기기는 Waters사(Waters Corp., Milford, MA, USA) HPLC system (510 pump, 717 plus autosampler, 410 differential refractometer, column heater module)을 사용하였고, 칼럼은 Supelcosil LC-NH2(250 mm×4.6 mm, 5 μm)를 사용하였다. 이동상은 acetonitrile:water(80:20, v/v) 혼합액을 사용하여 isocratic mode로 분석하였다. 분석 온도는 40°C, flow rate 0.8 mL/min, 주입량은 20 μL로 하였다. 유리당 함량은 표준품의 희석액(10-1,000 μg/mL)으로 작성한 검량선을 이용하여 정량하였다.
2.6. 아미노산 조성 분석
유리 아미노산은 동결 건조한 분말시료 1 g에 80% EtOH 20 mL를 가하고 30분간 초음파 처리 후 원심분리하여 상등액을 취하였다. 이 조작을 3회 반복하여 얻어진 상등액을 합하여 45°C 이하에서 감압농축한 다음 아미노산용 dilution buffer(pH 2.2) 5.0 mL에 용해시키고, membrane filter(0.45 μm)로 여과 후 아미노산 분석용 시료로 하였다. 총아미노산은 시료 1 g과 6 N HCl 용액 10 mL를 마개 부착 시험관에 취하고, 상층을 질소로 치환시킨 다음 110°C에서 24시간 동안 가수분해하였다. 가수분해액은 감압농축한 다음 농축액에 다시 소량의 증류수를 가하고, 감압농축하는 과정을 2회 반복하여 HCl을 휘산시킨 다음 농축된 잔사는 아미노산용 dilution buffer(pH 2.2) 10 mL에 용해시키고, 여과 후 분석에 사용하였다. 아미노산 분석기는 Sykam사(Gewerbering, Germany, S7130 amino acid reagent organizer, S5200 sample injector와 S2100 solvent delivery system을 사용하였으며, 칼럼은 cation separation column LCA K06/NA(250 mm×4.6 mm)를 사용하여 분석하였다. 이동상의 유속은 0.45 mL/min, ninhydrin은 0.4 mL/min으로 하여 분석하였다. 아미노산 함량은 Sykam사(Gewerbering, Germany)에서 구입한 아미노산 표품품 혼합액(100 μg/mL)을 동일조건에서 분석한 다음 각 peak area를 기준으로 자동계산 프로그램을 사용하여 정량하였다.
2.7. Phenolic acids 및 flavonoids 분석
건조시료 1.0 g을 취한 다음 70% MeOH 수용액 10 mL를 가하고, 실온에서 30분간 초음파 처리한 후 원심분리하여 상층액을 취하였다. 이 조작을 3회 반복하여 얻어진 상등액을 합하여 45°C 이하에서 감압농축한 다음, 70% MeOH 수용액 5 mL에 용해시키고, membrane filter(0.45 μm)로 여과한 후 분석용 시료로 사용하였다. Phenolic acid와 flavonoid 조성은 HPLC를 사용하여 분석하였다. HPLC 기기는 Waters 2690 saparation module과 996 photodiode array detector(PDA)를 사용하였다. 칼럼은 Agilent사(Agilent Technologies, Santa Clara, CA, USA)의 Eclipse XDB C18 RS(250 mm×4.6 mm ID, 5 μm)와 C18 guard column(20 mm×4.6 mm, 5 μm)을 사용하였다. 성분 분리는 gradient mode로 하였으며, 이동상 A는 0.1% formic acid를 함유하는 10% acetonitrile 용액, 이동상 B는 0.1% formic acid를 함유하는 90% acetonitrile 용액을 사용하여 분석하였다. 분석은 상온에서 실시하였으며, 유량은 1.0 mL/min, 주입량은 20 μL, 검출기 파장은 280 nm로 분석하였다. 용매의 구배조건은 5 min 100/A 0/B, 10 min 83/A 17/B, 30 min 80/A 20/B, 35 min 100/A 0/B, 45 min 100/A 0/B로 하였다. 성분의 정량은 phenolic acid 및 flavonoid 표준품 혼합물의 희석액(2.5-500 μg/mL)을 사용하여 작성한 검량선을 사용하여 정량하였다.
2.8. Parishin 유도체 분석
시료의 추출, 사용 HPLC 및 칼럼은 phenolic acid 및 flavonoid류 분석을 위하여 사용한 조건과 동일하게 하였다. 이동상은 0.1% formic acid를 함유하는 deionized water(A)와 0.1% formic acid를 함유하는 MeOHl(B)을 사용하였다. 이동상의 구배조건은 0분 85/A 15/B, 5분 85/A 15/B, 20분 45/A 55/B, 35분 85/A 15/B, 45분 85/A 15/B로 하였으며, 검출기(PDA) 파장은 220 nm로 하였다. 성분의 정량은 parishin 표준품 혼합물의 희석액(5.0-1,000 μg/mL)을 사용하여 작성한 검량선을 사용하여 정량하였다.
2.9. 뽕나무 버섯 배양액 분리효소에 의한 parishin A 분해
Parishin A 표준품 5.0 mg을 초산 완충용액(0.1 M, pH 4.8) 10 mL에 용해시킨 다음, 뽕나무 균사체에서 분리한 조효소 분말 5.0 mg을 첨가하고, 왕복진탕기(37°C, 24 h)에서 반응시키면서 주기적으로 시료를 채취하였다. 채취한 반응액은 비등 수욕조에서 10분간 가열한 다음, 감압농축 후 70% MeOH에 용해시켜 HPLC로 분석하였다. 또한, 대조구로서 동일한 조성의 반응액에 Rhizopus oryzae esterase(20 U)를 첨가한 다음 동일한 조건으로 반응시켜 생성물을 HPLC로 분석하였다.
2.10. 통계분석
각 실험은 3회 반복하여 얻은 결과를 평균±표준편차로 나타내었다. 또한, 실험에서 얻어진 결과 값은 Statistical Package for the Social Sciences(SPSS, IBM 20, NYC, USA) 프로그램을 이용하여 Duncan 다중범위 검정법 (Duncan’s multiple range test)으로 p⟨0.05로 유의성을 검정하였다.
3. 결과 및 고찰
3.1. pH 및 고형분 함량
꾸지뽕 열매 마쇄액에 뽕나무 버섯균을 접종 후 발효과정에서 pH 및 고형분 함량 변화를 조사한 결과는 Table 1에 나타내었다. 발효 초기에는 pH 5.1±0.1이었으나 발효 후 10일이 경과하였을 때에는 pH 4.8±0.1로서 뚜렷한 pH 변화는 보이지 않았으며, 뽕나무 버섯균을 접종하지 않고 동일한 조건으로 10일간 배양했을 때의 pH는 5.1±0.1로서 발효 초기 pH와 동일하였다. 또한, 가용성 고형분 함량(°Brix)은 발효 초기 4.2±0.1에서 발효 10일 후에는 2.5±0.1로서 약 40%가 감소하였으며, 역시 버섯 종균을 접종하지 않고 동일 조건에서 10일 경과한 고형분 함량은 4.0±0.1로서 발효시작 전의 고형분 함량과 유사하였다. 이와 같이 발효과정에서 가용성 고형분 함량이 감소하는 것은, 발효과정에서 꾸지뽕 열매에 함유된 유리당의 일부가 발효과정에서 뽕나무 버섯 증식을 위한 영양원으로 이용된 것으로 판단된다.
Table 1.
Changes in pH, soluble solid and free sugar during liquid fermentation of M. tricuspidata fruits with A. mellea
The values were expressed as mg/g and mean±SD (n=3). Different superscripts in the same row indicate significant differences (p⟨0.05) by Duncan’s multiple range test.
|
|
Fermentation time (day) |
|
0 |
2 |
4 |
6 |
8 |
10 |
101)
|
|
pH |
5.1±0.1c
|
5.1±0.1c
|
4.9±0.1b
|
4.6±0.1a
|
4.7±0.1a
|
4.8±0.1b
|
5.1±0.1c
|
|
°Brix |
4.2±0.1e
|
4.1±0.1d
|
4.0±0.1d
|
3.5±0.1c
|
3.1±0.1b
|
2.5±0.1a
|
4.0±0.1d
|
|
Fructose |
89.2±5.1b
|
117.7±11.2f
|
108.4±8.1e
|
96.1±6.5c
|
94.3±5.7c
|
70.1±4.6a
|
98.6±7.3d
|
|
Glucose |
105.2±6.3d
|
113.9±10.8e
|
102.1±9.9d
|
98.1±3.6c
|
84.2±4.7b
|
73.1±5.5a
|
116.5±3.2e
|
Download Excel Table
꾸지뽕 열매 중에서 유리당은 Table 1에서 보는 바와 같이 주로 glucose와 fructose가 주로 검출되었으며, 이러한 결과는 Jung 등(2013)이 꾸지뽕 열매에서는 유리당으로 glucose와 fructose만 검출되었다고 보고한 결과와 일치한다. Glucose와 fructose는 발효 2일 이후 약간 증가를 보인 다음, 그 이후는 발효기간이 경과함에 따라 감소하기 시작하여, 발효 10일이 경과하였을 때 fructose 함량은 발효 전에 비하여 약 21%가 감소하였고, glucose 함량은 약 31%가 감소하였다. 발효시작 후 2일이 경과한 시점에서 glucose와 fructose 함량이 증가한 이후에 발효가 진행됨에 따라 점차 감소하는 것은, 발효 초기에 꾸지뽕 열매 중에 함유된 전분과 같은 다당류가 유리당으로 가수분해된 다음, 유리당이 뽕나무 버섯균의 생육을 위한 영양원으로 이용되기 때문으로 판단된다. 또한, 뽕나무 버섯균을 접종하지 않고 동일한 조건으로 10일간 배양했을 때의 glucose와 fructose 함량은 발효 시작 전과 뚜렷한 차이를 보이지 않았다.
3.2. 유리 및 총아미노산 조성
발효과정에서 유리 아미노산의 조성 변화를 분석한 결과는 Table 2와 같다. 발효가 진행되기 전인 대조구의 꾸지뽕 열매 중의 유리 아미노산 함량은 2,635.3±40.5 mg/100 g이었고, 발효 시작 후 4일이 경과할 때까지는 큰 변화를 보이지 않다가 그 이후부터 급격히 감소하여 10일이 경과한 후에는 1,143.6±40.6 mg/100 g으로 대조구 대비 약 40% 수준으로 감소하였다. 이러한 결과는 버섯군의 생육주기와 관련이 있을 것으로 판단된다. 버섯의 생육단계는 다른 미생물과 마찬가지로 유도기(lag phase), 대수증식기(exponetial phase), 정지기(stationary phase) 및 사멸기(death phase)로 구분할 수가 있는데, 유도기에는 세포가 새로운 배지에서 증식하는 데 필요한 RNA, 효소 및 기타 물질들을 생합성하기 위한 준비단계로써 세포는 커지지만 분열은 일어나지 않는다. 반면에 대수증식기에 접어들게 되면 세포가 최대의 속도로 분열하면서 각종 대사활동이 활발하게 일어난다(Vrabl 등, 2019). 따라서 유도기에 해당하는 4일 이내에서는 유리 아미노산 함량 변화가 일어나지 않은 반면, 대수증식기에 해당하는 4-10일 사이에는 각종 대사활동과 함께 균사체 증식을 위하여 아미노산 소비량이 증가하기 때문인 것으로 판단된다. Yang과 Zhang (2009)은 영지버섯균으로 두유(soymilk)를 발효시켰을 때 총아미노산 함량은 발효 전에는 7.51 mg/mL이었으나, 96시간 발효 후에는 4.71 mg/mL로 감소하였다고 보고하였다. 또한, 개별 유리아미노산 함량도 48시간까지는 뚜렷한 변화가 없지만 96시간 발효 후에는 대부분의 유리 아미노산이 감소하였으며, 이러한 감소는 영지버섯균 균사체의 성장과 대사를 위하여 유리 아미노산을 이용하기 때문이며, 유리 아미노산은 버섯균의 성장을 위한 좋은 영양원이다 (Chang 등, 2006; Yand와 Zhang, 2009). 개별 유리 아미노산 함량도 전반적으로 감소하는 경향을 보였지만, 그중에서도 특히 양적으로 많이 검출된 aspartic acid, serine, asparagine, γ-aminobutyric acid 및 arginine 등의 감소하는 폭이 큰 반면, citrulline은 오히려 발효기간이 경과함에 따라 함량이 증가하는 경향을 보였다. Citrulline과 arginine은 생화학적 대사의 관점에서 밀접한 관련이 있는데, NADPH의 도움을 받은 nitric oxide(NO) synthase에 의하여 arginine 분자가 산소분자와 반응하여 NO를 유리시킨 다음 citrulline으로 변환되는 것으로 알려져 있기 때문에 발효과정에서 arginine의 일부가 citrulline으로 변환되었을 가능성도 있다(Morris, 2004).
Table 2.
Changes in free amino acid content during liquid fermentation of M. tricuspidata fruits with A. mellea
The values were expressed as mg/100 g and mean±SD (n=3). Different superscripts in the same row indicate significant differences (p⟨0.05) by Duncan’s multiple range test.
|
Amino acid |
Fermentation time (day) |
|
0 |
2 |
4 |
6 |
8 |
10 |
101)
|
|
Aspartic acid |
104.3±5.1f
|
77.0±3.0e
|
63.3±3.5d
|
7.3±2.0a
|
21.3±2.3c
|
13.3±2.5b
|
103.6±4.0f
|
|
Serine |
236.3±2d
|
234.6±3.5d
|
249.0±6.5e
|
31.6±3.5a
|
40.3±3.5b
|
48.0±2.6c
|
238.3±4.5d
|
|
Asparagine |
303.0±4.3e
|
278.0±4.0d
|
298.6±3.5e
|
205.3±2.5c
|
127.3±3.7a
|
134.6±3.5b
|
303.0±3.0e
|
|
Glutamic acid |
205.6±2.0e
|
190.0±3.0d
|
188.6±3.2d
|
148.0±2.0b
|
137.6±4.5a
|
154.0±4.0c
|
207±3.6e
|
|
Glycine |
69.6±2.5d
|
71.0±3.6d
|
59.6±2.5c
|
62.6±2.5c
|
31.0±2.6a
|
51.0±3.6b
|
72.3±4.9d
|
|
Alanine |
20.3±3.2bc
|
23.3±3.5c
|
19.6±1.5bc
|
11.3±1.5a
|
18.6±1.5b
|
22.6±2.5bc
|
19.3±1.5bc
|
|
Citrulline |
403.6±3.2b
|
450.0±5.0d
|
478.0±2.6e
|
433.3±5.6c
|
501.6±3.2f
|
512.0±6.2g
|
397.0±2.6a
|
|
Valine |
30.3±2.5b
|
38.0±2.0c
|
40.6±3.0c
|
13.0±1.0a
|
16.3±1.5a
|
16.6±1.5a
|
27.3±2.0b
|
|
Cystine |
13.0±1.0bc
|
14.0±1.0bc
|
15.6±2.0cd
|
17.6±1.5d
|
4.6±2.0a
|
10.3±2.5b
|
15.3±3.5cd
|
|
Methionine |
7.6±1.5cd
|
6.6±1.5bc
|
5.3±0.5abc
|
6.6±2.0bc
|
5.0±1.0ab
|
3.3±0.5a
|
9.3±1.5d
|
|
Isoleucine |
55.3±1.5d
|
66.6±2.0e
|
66.6±4.1e
|
15.0±2.0a
|
22.0±2.0b
|
25.3±2.5b
|
50.6±2.0c
|
|
Leucine |
60.0±2.0d
|
70.3±1.5e
|
74.3±1.5e
|
5.3±0.5a
|
15.0±2.6b
|
14.3±3.0b
|
51.3±4.1c
|
|
Tyrosine |
25.3±1.5cd
|
28.3±1.5de
|
31.6±1.5e
|
9.0±1.0a
|
14.3±3.2b
|
16.0±2.6b
|
23.0±1.0c
|
|
Phenylalanine |
47.0±1.0e
|
60.0±2.0f
|
62.6±2.5f
|
8.0±1.0a
|
14.6±0.5b
|
20.6±2.0c
|
42.3±2.5d
|
|
γ-Aminobutyric acid |
906.6±3.2g
|
870.6±3.0e
|
601.3±1.5d
|
462.3±2.0c
|
110.3±1.5b
|
94.6±3.5a
|
878.3±1.5f
|
|
Lysine |
42.3±2.0cd
|
49.0±1.0e
|
45.0±1.0d
|
8.6±0.5a
|
20.3±1.5b
|
21.0±1.7b
|
40.6±2.0c
|
|
Arginine |
104.6±1.5f
|
102.0±1.0f
|
89.0±1.0d
|
56.6±1.5c
|
43.0±3.0b
|
26.3±1.5a
|
99.0±1.0e
|
|
Total |
2,635.3±40.5d
|
2,629.6±42.3d
|
2,389.3±42.4c
|
1,502.0±33.2b
|
1,143.6±40.6a
|
1,184.3±46.7a
|
2,578.0±45.7d
|
Download Excel Table
한편, 총아미노산 조성 변화를 분석한 결과는 Table 3과 같다. 총아미노산 조성은 유리 아미노산과는 다른 경향을 보였는데, 양적으로는 arginine, γ-aminobutyric acid (GABA), glutamic acid, aspartic aid, leucine, isoleucine, lysine 등이 많이 검출되었다. 그중에서 GABA는 발효가 진행됨에 따라 크게 감소했지만, serine, glutamic acid, glycine, alanine, isoleucine, leucine, phenylalanine 및 lysine 함량은 증가하는 경향을 보였으며, amino acid들의 총량은 발효가 진행됨에 따라 약간 증가하는 경향을 보였다. 이러한 경향은 발효가 진행됨에 따라 꾸지뽕 열매 중에 함유되어 있는 아미노산류는 감소될 것으로 예상되지만, 발효기간이 증가할수록 뽕나무 버섯 균사체 생성량은 증가하고, 버섯 균사체에는 각종 아미노산이 골고루 함유되어 있는 것으로 알려져 있기 때문에, 발효기간 증가에 따라 총아미노산 함량이 증가하는 것은 주로 버섯 균사체에 함유된 단백질이 산 가수분해과정에서 유리 아미노산으로 변환된 것으로 판단된다.
Table 3.
Changes in total amino acid content during liquid fermentation of M. tricuspidata fruits with A. mellea
The values were expressed as mg/100 g and mean±SD (n=3). Different superscripts in the same row indicate significant differences (p⟨0.05) by Duncan’s multiple range test.
|
Amino acid |
Fermentation time (day) |
|
0 |
2 |
4 |
6 |
8 |
10 |
101)
|
|
Aspartic acid |
765.1±10.1e
|
817.0±5.5f
|
889.6±5.7g
|
647.0±8.5c
|
621.0±5.2a
|
633.6±11.0b
|
698.6±1.1d
|
|
Threonine |
209.1±5.2a
|
215.6±6.0a
|
241.0±1.7b
|
263.6±1.1c
|
311.6±17.6d
|
306.3±6.5d
|
216.6±2.3a
|
|
Serine |
313.3±12.5a
|
330.0±8.0b
|
367.3±1.1c
|
303.3±3.5a
|
332.6±2.3b
|
329.0±6.5b
|
341.0±8.7b
|
|
Glutamic acid |
959.3±4.1a
|
1,049.3±24.1b
|
1,047.3±6.6b
|
1,146.6±21.7c
|
1,058.6±41.6b
|
1,115.6±13.6c
|
959.0±7.8a
|
|
Proline |
113.6±3.1c
|
124.0±3.4d
|
138.3±5.7e
|
122.6±9.2d
|
97.3±1.1ab
|
91.3±2.3a
|
104.3±3.1b
|
|
Glycine |
217.1±5.5a
|
253.3±12.5c
|
268.6±2.3d
|
274.0±6.9d
|
304.0±6.9e
|
303.6±6.3e
|
240.0±6.0b
|
|
Alanine |
231.1±5.2a
|
249.3±8.1b
|
272.3±4.0c
|
294.6±2.8d
|
313.0±9.4e
|
309.3±9.3e
|
237.6±4.0a
|
|
Valine |
186.1±5.2a
|
193±7.2a
|
211.3±2.3b
|
209.6±0.5b
|
215.6±4.0b
|
236.6±6.3c
|
192.6±4.0a
|
|
Cystine |
7.6±1.5a
|
8.6±0.5a
|
14.6±0.5b
|
8.3±0.5a
|
31.0±1.7c
|
8.3±0.5a
|
7.6±0.5a
|
|
Methionine |
8.3±1.5a
|
23.0±2.0b
|
52.3±1.1c
|
61.6±2.8e
|
54.3±2.3d
|
54.0±1.7d
|
8.4±1.3a
|
|
Isoleucine |
327.6±14.1a
|
358.6±6.0b
|
384.3±22.3d
|
372.0±15.1c
|
460.3±14.0f
|
418.3±12.8e
|
358.3±12.8b
|
|
Leucine |
360.6±16.1a
|
384.0±13.6b
|
421.0±31.7c
|
416.3±15.7c
|
470.6±24.0e
|
461.0±15.1d
|
389.3±21.1b
|
|
Tyrosine |
73.6±2.3a
|
84.3±1.1b
|
91.6±2.8c
|
91.6±2.8c
|
121.3±2.3e
|
103.6±2.3d
|
82.0±1.7b
|
|
Phenylalanine |
271.3±1.5a
|
297.0±13.5cd
|
325.0±13.4e
|
301.3±12.3d
|
281.6±16.3b
|
328.6±12.3e
|
291.3±12.8c
|
|
γ-Aminobutyric acid |
461.1±14.1d
|
476.3±2.8d
|
465.3±0.5d
|
40.3±4.0a
|
115.6±18.4b
|
62.6±4.6a
|
427.3±4.6c
|
|
Carnosine |
53.3±2.5b
|
63.0±2.6c
|
61.3±2.3c
|
61.6±2.8c
|
43.6±2.3a
|
44.0±1.7a
|
76.0±1.7d
|
|
Ornithine |
34.6±2.8d
|
15.0±2.0b
|
14.3±1.1b
|
25.0±3.4c
|
22.3±1.1c
|
37.0±1.7d
|
7.6±0.5a
|
|
Lysine |
388.1±10.1a
|
423.6±4.7b
|
483.6±6.3c
|
515.6±4d
|
568.6±2.3e
|
582.3±4.6f
|
417.3±4.6b
|
|
Arginine |
618.1±6.2a
|
658.6±6.6c
|
751.6±2.8f
|
722.3±9.8e
|
681.0±3.4d
|
671.6±5.7d
|
633.0±8.6b
|
|
Total |
5,598.6±104.1a
|
6,024.0±110.9c
|
6,501.3±55.1d
|
5,878.0±98.4b
|
6,104.6±131.0c
|
6,097.3±88.5c
|
5,926.3±60.9b
|
Download Excel Table
3.3. Phenolic acids 및 flavonoids 변화
뽕나무 버섯균으로 꾸지뽕 열매를 발효시키는 과정에서 phenolic acid 및 flavonoid 조성변화를 HPLC로 분석한 결과는 Table 4와 같다. 뽕나무 버섯균을 접종하지 않고 동일 조건에서 10일간 배양한 시료에서는 대조구(0일) 대비 개별 phenolic acid 및 flavonoid의 함량은 뚜렷한 변화를 보이지 않았다. 반면에, 뽕나무 버섯균을 접종한 시료에서는 발효기간이 경과함에 따라, 양적으로 많이 함유된 chlorogenic acid 함량은 발효 시작 전에는 1,165.1±22.3 μg/g이었으나, 발효 10일 후에는 157±8.1 μg/g으로 약 87%가 감소하였으며, protocathuic acid도 감소한 반면에, caffeic acid 및 p-hydroxybenzoic acid는 오히려 증가하였다. 뽕나무 버섯균에 의한 꾸지뽕 열매가 발효하는 동안 chlorogenic acid의 감소는 뽕나무버섯 균사체가 분비하는 chlorogenic acid 가수분해 효소와 관련이 있을 것으로 판단된다. Chlorogenic acid는 quinic acid와 caffeic acid가 ester 결합한 성분이고 chlorogenic acid는 관련 효소인 chlorogenic acid hydrolase(CAH) 또는 chlorogenic acid esterase에 의해 가수분해될 수 있다. Cocoletzi-Flores 등(2020)은 커피 제조과정에서 부산물로써 산출되는 펄프를 흑국균인 Aspergillus niger로 발효시켰을 때, 펄프에 함유된 chlorogenic acid가 caffeic acid로 용이하게 생물변환되며, 이는 Asp. niger에서 분비되는 CAH의 작용에 기인한다고 보고하였고, Wang 등(2020)은 녹차를 효모(Saccharomyces cerevisiae)로 발효시켰을 때, chlorogenic acid는 유의적으로 감소하고 caffeic acid는 증가하였는데, 이는 효모가 분비하는 CAH의 작용에 기인한다고 보고하였다. 또한, 본 실험결과에서도 발효과정에서 caffeic acid의 증가 폭보다 chlorogenic acid의 감소 폭이 컸는데 이러한 현상은 chlorogenic acid뿐만 아니라, chlorogenic acid가 가수분해되어 생성된 caffeic acid의 일부가 뽕나무버섯 균사체가 분비하는 polyphenol oxidase에 의해 산화되어 감소한 것으로 판단된다. 실제로 뽕나무 버섯을 포함한 담자균류에는 활성이 강하면서 기질 특이성이 넓은 polyphenol oxadase들이 함유된 것으로 보고되어 있다(Martínková 등, 2016).
Table 4.
Changes in the composition of phenolic compounds during liquid fermentation of M. tricuspidata fruits with A. mellea
The values were expressed as μg/g and mean±SD (n=3). Different superscripts in the same row indicate significant differences (p⟨0.05) by Duncan’s multiple range test.
|
Compounds |
Fermentation time (day) |
|
0 |
2 |
4 |
6 |
8 |
10 |
101)
|
|
Protocatechuic acid |
414.3±19.3d
|
308.4±20.9b
|
305.5±12.3b
|
312.6±14.3b
|
321.0±12.4c
|
294.9±13.2a
|
416.0±12.1d
|
|
p-Hydroxybenzoic acid |
18.4±1.2a
|
79.5±3.3e
|
78.6±3.4e
|
53.7±2.3d
|
40±1.2c
|
23.8±3.2b
|
18.5±1.2a
|
|
Chlorogenic acid |
1,165.1±22.3c
|
281.4±11.1b
|
179.7±13.2a
|
172.7±9a
|
164±9.3a
|
157±8.1a
|
1,147.4±19.8c
|
|
Caffeic acid |
25.2±0.2a
|
55.9±0.9b
|
86±0.8d
|
84.6±0.7d
|
86.5±0.6d
|
74.8±0.5c
|
25.3±0.4a
|
|
Quercetin |
49.1±0.2b
|
49.8±0.3b
|
75±0.4d
|
55.5±0.7c
|
47.6±0.8b
|
38.8±0.4a
|
50.5±0.3b
|
|
Total |
1,673.1±21.9d
|
775.7±15.1c
|
721.6±14.3c
|
676.4±13.4b
|
656.5±15.4b
|
587.7±12.3a
|
1,653.5±19.5d
|
Download Excel Table
3.4. Parishin 유도체의 변화
최근에 꾸지뽕 열매에는 다수의 parishin 유도체 및 그의 아글리콘인 4-HBA가 함유되어 있다는 것이 규명되어 졌고, 이 성분들은 꾸지뽕 열매의 생리활성과 밀접한 관련이 있다는 것이 보고된 바 있다(Choi 등, 2018; Choi 등, 2020). 뽕나무 버섯균에 의해 꾸지뽕 열매가 발효되는 동안 parishin 유도체 및 4-HBA 변화를 Table 5에 나타내었다. 발효기간이 경과함에 따라 parishin A, B, C 및 parishin의 가수분해 중간 생성물인 gastrodin은 감소하는 반면 4-HBA는 증가하였으며, 특히 발효 8일 차가 되는 시점부터 증가 폭이 크게 나타났다. Gastrodin은 4-HBA에 글루코스 1분자가 베타형으로 결합된 배당체이고, parishin 유도체는 유기산인 citric acid에 1-3개의 gastrodin이 ester 결합한 화합물들이다. 따라서 발효과정에서 parishin 유도체들은 감소하는 반면, 4-HBA의 함량이 증가하는 현상은 뽕나무 버섯균이 증식하는 과정에서 분비된 esterase와 β-glucosidase의 작용에 의해 parishin 유도체들이 gastrodin을 거쳐 4-HBA로 가수분해되기 때문으로 판단된다. 또한, parishin 유도체와 gatrodin의 감소량은 큰 데 비하여 4-HBA는 증가 폭은 크지 않은 편이었는데, 이러한 이유는 4-HBA도 역시 페놀성 화합물로 일부는 뽕나무버섯 균사체가 분비하는 polyphenol oxidase에 의해 산화되어 다른 성분으로 생물변환된 것으로 판단된다.
Table 5.
Changes in the composition of parishin compounds during liquid fermentation of M. tricuspidata fruits with A. mellea
The values were expressed as μg/g and mean±SD (n=3). Different superscripts in the same row indicate significant differences (p⟨0.05).
|
Compounds |
Fermentation time (day) |
|
0 |
2 |
4 |
6 |
8 |
10 |
101)
|
|
Gastrodin |
3,762.4±40.6d
|
3,509.6±30.2c
|
3,502.0±22.3c
|
3,441.3±23.3c
|
2,586.7±11.2b
|
1,658.7±24.4a
|
3,461.4±44.0c
|
|
4-HBA2)
|
135.2±1.2a
|
151.1±1.3a
|
147.1±1.0a
|
215.7±1.3b
|
460.9±6.2c
|
449.0±3.0c
|
131.2±3.1a
|
|
Parishin E |
475.2±3.2d
|
395.3±6.3a
|
419.3±6.2b
|
443.2±7.1c
|
403.3±5.6a
|
427.2±4.7b
|
456.2±2.2c
|
|
Parishin B |
1,243.7±11.1d
|
1,227.8±9.8d
|
1,161.8±7.7c
|
1,037.7±7.8b
|
940±5.6b
|
676.0±6.6a
|
1,283.7±10.1d
|
|
Parishin C |
704.1±5.5c
|
655.2±3.4c
|
508.7±2.2b
|
69.0±1.2a
|
65.7±1.0a
|
56.0±0.7a
|
724.1±4.5c
|
|
Parishin A |
799.7±4.5d
|
810.5±4.3d
|
721.6±2.3c
|
713.5±4.3c
|
622±2.1b
|
484.7±2.1a
|
810.7±3.2d
|
|
Total |
7,120.6±92.3e
|
6,749.7±52.3d
|
6,460.8±51.4d
|
5,920.7±32.3c
|
5,078.8±30.3b
|
3,751.8±11.1a
|
7,006.6±98.9e
|
Download Excel Table
3.5. 조효소에 의한 parishin의 생물변환
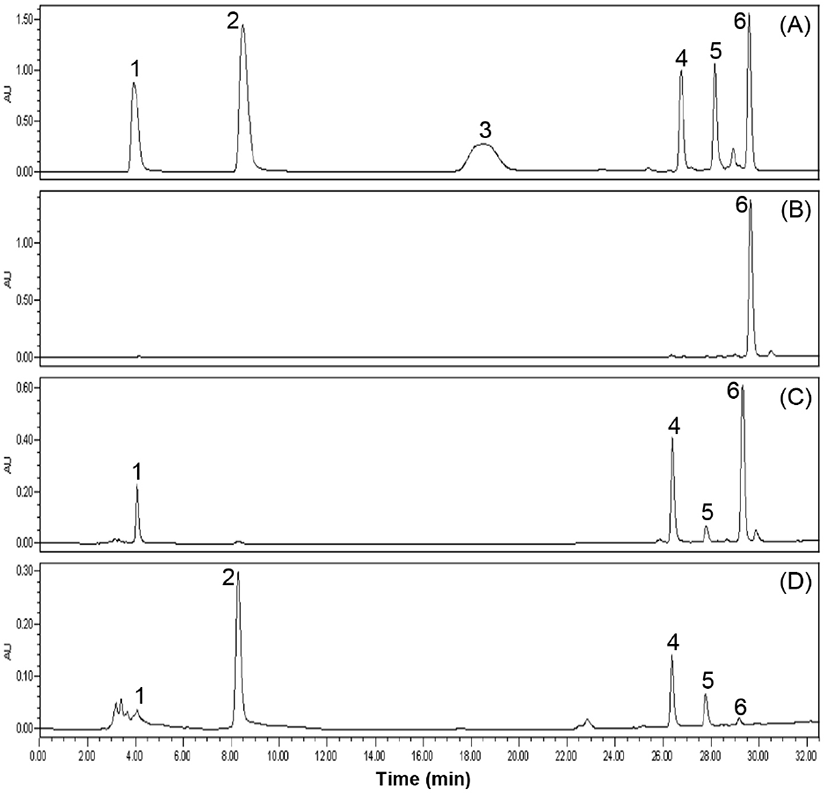
뽕나무 버섯균에 의한 발효 동안 꾸지뽕 열매에 함유된 parishin 유도체들이 실제로 gastrodin을 경유하여 4-HBA로 생물변환되는지를 확인하기 위하여, 표준품 parishin A를 함유하는 반응액에 시판품인 Rhizopus oryzae esterase 또는 뽕나무 버섯 균사체에서 분리한 조효소 분말(30-80% ammonium sulfate 침전)을 첨가한 후, 24시간 반응시켜 HPLC로 분석한 결과는 Fig. 1과 같다. R. oryzae esterase로 반응시켰을 때, gastrodin 3분자가 ester 결합해 있는 parishin A가 1차적으로 가수분해되어 gastrodin 2분자가 결합한 형태인 parishin B 또는 parishin C로 가수분해된 다음 최종적으로 gastrodin이 생성되었으나, gastrodin의 β-배당체 결합이 가수분해되어 생성되는 aglycone인 4-HBA는 생성되지 않았다(Fig. 1(C)). 이러한 결과는 R. oryzae esterase는 순수하게 정제된 단일 효소로써 β-glucosidase 활성은 없는 것으로 여겨진다. 반면에 parishin A를 함유하는 반응액에 뽕나무버섯 배양액에서 분리한 조효소를 첨가 후 반응시켰을 때에는 기질로 사용한 parishin A의 대부분은 가수분해되어 소실된 반면, peak 2의 4-HBA가 크게 증가하였고, parishin A가 4-HBA로 생물변환되는 과정에서 중간물질들인 parishin B, parishin C 이외에도 gastrodin이 검출되었다(Fig. 1(C)).
Fig. 1.
Comparison of hydrolysis of parishin A with Rhizopus oryzae esterase and crude enzyme preparation from A. mellea mycelia.
A, standard mixture of parishin derivatives; B, parishin A standard; C, hydrolysate of parishin A by Rhizopus oryzae esterase; D, hydrolysate of parishin A by crude enzyme preparation from A. mellea mycelia for 24 h. 1, gastrodin; 2, 4-HBA; 3, parishin E; 4, parishin B; 5, paroshin C; 6, parishin A.
Download Original Figure
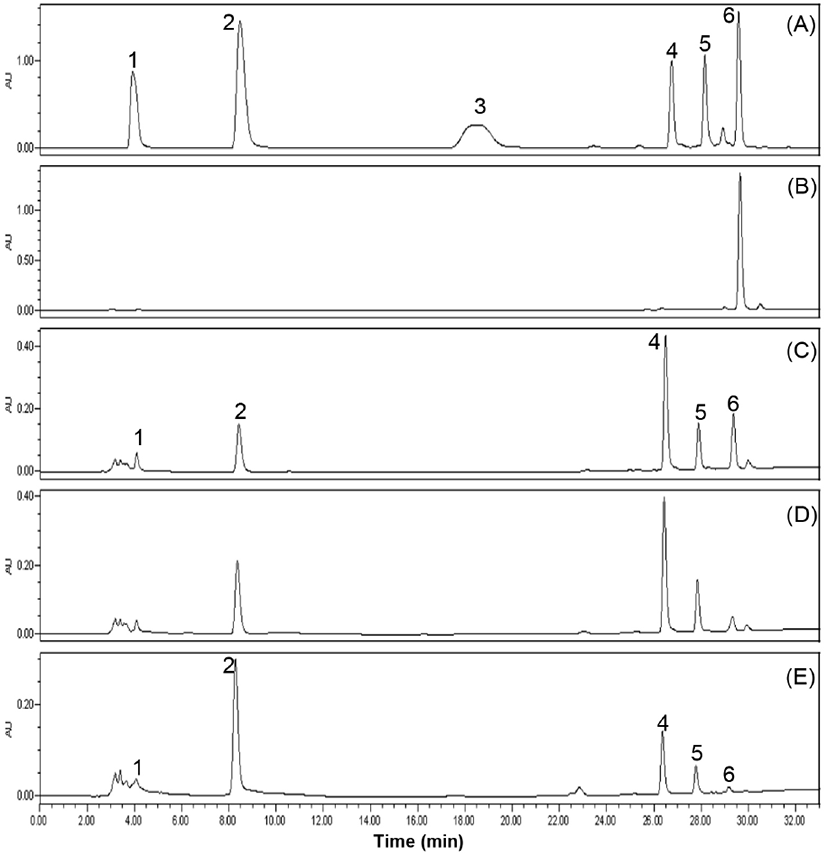
또한, parishin A를 함유하는 반응액에 뽕나무 버섯 배양액에서 분리한 조효소를 첨가 후 반응시간 경과에 따른 parishin A의 분해 양상을 Fig. 2에 나타내었다. Fig. 2(C)를 보면 발효시작 시점에서 parishin A 일부분이 parishin B, parishin C 또는 gastrodin으로 변환되었고, 이 중의 일부가 4-HBA로 생물변환되었다. Gastrodin의 변화는 큰 차이가 나지 않는데, 이러한 이유는 esterase와 버섯에서 생성된 β-glucosidase에 의해 빠르게 분해된 것으로 판단된다. 24시간(Fig. 2(E)) 후에는 parishin A, B, C 및 gastrodin의 대부분이 4-HBA로 변환되었다. 이러한 결과는 parishin A 및 그의 유도체들이 Fig. 3과 같은 경로를 거쳐 4-HBA로 생물변환된다는 것을 나타내주고 있다. 또한 이러한 결과는 꾸지뽕 열매를 뽕나무버섯균으로 발효시키게 되면 균사체가 증식하는 과정에서 parishin A, B 또는 parishin C의 ester 결합을 분해시킬 수 있는 esterase 이외에도 β-배당체인 gastrodin의 β-glucoside 결합을 가수분해하여 4-HBA를 생성할 수 있는 β-glucosidase를 분비하는 것을 나타내고 있다. 생성된 4-HBA는 불면증 개선, 수면유도, 진정효과 등 인체 중추신경계에 긍정적인 효과(Kim 등, 2007; Kim 등, 2012; Lim 등 2007; Zhu 등, 2018) 이외에도 최근에는 비만과 관련된 효소들의 활성을 억제하여 직접 또는 간접적으로 항비만 활성도 지니고 있는 것으로 보고되어 있다(Choi 등, 2018).
Fig. 2.
Time course of hydrolysis of parishin A with crude enzyme preparation from mellea mycelia.
A, standard mixture of parishin derivatives; B, parishin A standard; C, hydrolysate of parishin A by crude enzyme preparation from A. mellea mycelia for 4 h; D, 8 h; E, 24 h. 1, gastrodin; 2, 4-HBA; 3, parishin E; 4, parishin B; 5, paroshin C; 6, parishin A.
Download Original Figure
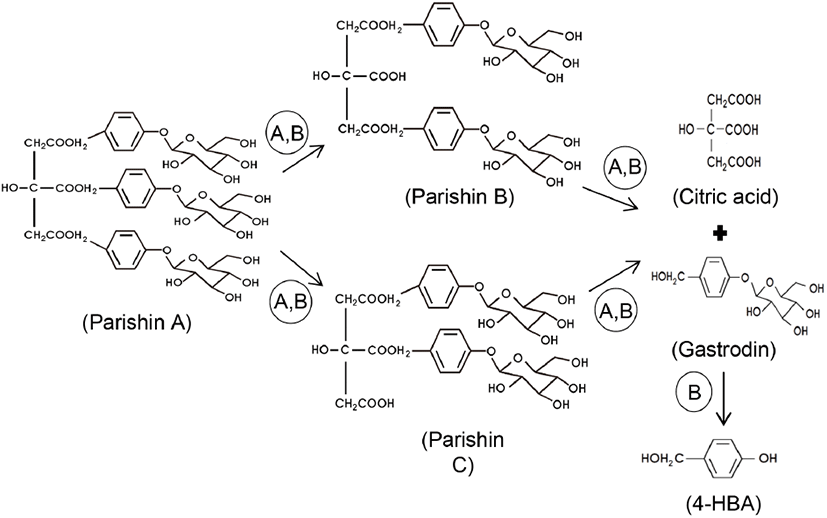
Fig. 3.
Hydrolysis pathway of parishin A by Rhizopus oryzae esterase and crude enzyme preparation from A. mellea mycelia.
A, Rhizopus oryzae esterase; B, crude enzyme from A. mellea mycelia.
Download Original Figure
감사의 글
본 연구는 산림청(과제번호 2021381A00-2123-BD02) 지원에 의한 연구과제의 일부로 이에 감사드립니다.
References
Bentil JA. Biocatalytic potential of
Basidiomycetes: Relevance, challenges and research interventions in industrial processes. Sci Afr, 11, e00717 (2021)


Bragaloni BM, Anselmi N, Cellerino GP. Identification of European
Armillaria species by analysis of isozyme profiles. Eur J For Path, 27, 147-157 (1997)


Buswell JA, Cai YJ, Chang ST, Peberdy JF, Fu SY, Yu HS. Lignocellulolytic enzyme profiles of edible mushroom fungi. World J Microbiol Biotechnol, 12, 537-542 (1996)

,


Cha JY, Kim HJ, Jun BS, Cho YS. Effect of water-extracted of leaves from
Morus alba and
Cudrania tricuspidata on the lipid concentrations of serum and liver in rats. J Korean Soc Agric Chem Biotechnol, 43, 303-308 (2000)

Chang MY, Tsai GJ, Houng JY. Optimization of the medium composition for the submerged culture of
Ganoderma lucidum by Taguchi array design and steepest ascent method. Enzyme Microb Techn, 38, 407-414 (2006)


Chen PJ, Sheen LY.
Gastrodia rhizoma (tiān mǎ): A review of biological activity and antipressant mechanisms. J Tradit Complement Med, 1, 31-40 (2011)


Choi HJ, Kim CT, Do MY, Rang MJ. Physiological activities of
Cudrania tricuspidata extracts (Part Ⅰ). J Korea Acad-Indus Coop Soc, 14, 3907-3915 (2013)


Choi JH, Kim MK, Yeo SH, Kim S. Short‑term
Cudrania tricuspidata fruit vinegar administration attenuates obesity in high-fat diet-fed mice by improving fat accumulation and metabolic parameters. Sci Rep, 10, 21102 (2020)

,

,


Choi JH, Yeo SH, Kim MK, Lee HJ, Kim S.
p-Hydroxybenzyl alcohol inhibits four obesity related enzymes
in vitro. J Biochem Mol Toxicol, 32, e22223 (2018)

,


Cocoletzi-Flores MA, Sanchez-Minutti L, Tellez-Giron JD, Ortega-Sanchez E, Garcia-Davila J. Fungal biotransformation of chlorogenic acid to caffeic acid from coffee pulp. Int J Appl Microbiol Biotechnol Res, 8, 15-20 (2020)

Ertunga SN, Turan A, Akatin MY, Keskin S. Partial purification and characterization of
Armillaria melleaβ-glucosidase. Inter J Food Prop, 17, 678-689 (2014)


Fukai T, Oku Y, Hou AJ, Yonekawa M, Terada S. Antimicrobial activity of isoprenoid-substituted xanthones from
Cudrania cochinchinensis against vancomycin-resistant
Enterococci. Phytomedicine, 12, 510-513 (2005).

,


Han XH, Hong SS, Hwang JS, Jeong SH, Hwang JH, Lee MH, Lee MK, Lee D, Ro JS, Hwang BY. Monoamine oxidase inhibitory constituents from the fruits of
Cudrania tricuspidata. Arch Pharm Res, 28, 1324-1327 (2005)

,


Han XH, Hong SS, Jin Q, Li D, Kim HK, Lee J, Kwon SH, Lee D, Lee CK, Lee MK, Hwang BY. Prenylated and benzylated flavonoids from the fruits of
Cudrania tricuspidata. J Nat Prod, 72, 164-167 (2009)

,


Jang JH, Son J, Kang SS, Bae CS, Kim JC, Kim SH, Shin T, Moon C. Neuropharmacological potential of
Gastrodia elata Blume and its components. Evi Based Complement Alternat Med, Article 309261 (2015)

,

,


Jeong CH, Choi GN, Kim JH, Kwak JH, Heo HJ, Shim KH, Cho BR, Bae YI, Choi JS.
In vitro antioxidative activities and phenolic composition of hot water extract from different parts of
Cudrania tricuspidata. J Food Sci Nutr, 14, 283-289 (2009)


Jia YW, Li X, Xie HT, Shen J, Luo J, Wang JS, Wang KDG, Liu QW, Kong LY. Analysis and pharmacokinetics studies of gastrodin and
p-hydroxybenzyl alcohol in dogs using ultra fast liquid chromatography-tandem mass spectrometry method. J Pharm Biomed Anal, 99, 83-88 (2014)

,


Kang DH, Kim JW, Youn KS. Antioxidant activities of extracts from fermented mulberry (
Cudrania tricuspidata) fruit, and inhibitory actions on elastase and tyrosinase. Korean J Food Preserv, 18, 236-243 (2011)


Kim BW, Koppula S, Kim JW, Lim HW, Hwag JW, Kim IS, Park PJ, Choi DK. Modulation of LPS-stimulated neuroinflammation in BV-2 microglia by
Gastrodia elata: 4-Hydroxybenzyl alcohol is the bioactive candidate. J Ethanopharm, 139, 549-557 (2012)

,


Kim DW. Bioactive constituents of
Maclura tricuspidata fruit and quality characteristics of fermented vinegar. Ph D Thesis, Jeonbuk National University, Korea, p 120-146 (2021)

Kim DW, Kim DH, Kim JK, Yeo SH, Choi HS, Kim YH, Kim MK. Comparison of volatile compounds in
Maclura tricuspidata fruit vinegar and commercial vinegars. Korean J Food Preserv, 27, 85-97 (2020)


Kim DW, Lee WJ, Gebru YA, Choi HS, Yeo SH, Jeong YJ, Kim S, Kim YH, Kim MK. Comparison of bioactive compounds and antioxidant activities of
Maclura tricuspidata fruit extracts at different maturity stages. Molecules, 24, 567 (2019)

,

,


Kim HJ, Hwang IK, Won MH. Vanillin, 4-hydroxyben aldehyde and 4-hydroxybenzyl alcohol prevent hippocampal CA1 cell death following global ischemia. Brain Res, 1181, 130-141 (2007)

,


Kim YC, Hur J, Sohn DH, Kim HS. Antibacterial compounds of the root barks of
Cudrania tricuspidata. Kor J Pharmacogn, 39, 246-248 (2008)

Kulikova N, Klein O, Stepanova E, Koroleva O. Use of basidiomycetes in industrial waste processing and utilization technologies: Fundamental and applied aspects (review). Appl Biochem Microbiol, 47, 565-579 (2011)


Lee YJ, Kim S, Lee SJ, Ham I, Whang WK. Antioxidant activities of new flavonoids from
Cudrania tricuspidata root bark. Arch Pharm Res, 32, 195-200 (2009)

,


Lim EJ, Kang H, Jung HJ, Park EH. Anti-aingiogenic, anti-inflammatory and anti-nociceptive activity of 4-hydroxybenzyl alcohol. J Pharm Pharmacol, 59, 1235-1240 (2007)

,


Martinkova L, Kotik M, Markova E, Homolka L. Biodegradation of phenolic compounds by
Basidiomycota and its phenol oxidases: A review. Chemosphere, 149, 373-382 (2016)

,


Morris SM. Enzymes of arginine metabolism. J Nutr, 134, 2743S-2747S (2004)

,


Oh PS, Lee HJ, Lim KT. Inhibitory effect of glycoprotein isolated from
Cudrania tricuspidata bureau on histamine release and COX-2 activity in PBL-2H3 cells. Korean J Food Sci Technol, 41, 405-412 (2009)

Olicon-Hernandez DR, Gonzalez-Lopez J, Aranda E. Overview on the biochemical potential of filamentous fungi to degrade pharmaceutical compounds. Front Microbiol, 8, Article 1972 (2017)

,

,


Park JC, Young HS, Choi JS. Constituents of
Cudrania tricuspidata in Korea. Yakhak Hoeji, 36, 40-45 (1992)

Park SE, Yeo SH, Kim S. The effect of
Cudrania tricuspidata fruit vinegar on LPS-induced inflammation in 3T3-L1 adipocytes. Korean J Food Preserv, 27, 809-816 (2020)


Seo EJ, Curtis-Long MJ, Lee BW, Kim HY, Ryu YB, Jeong TS, Lee WS, Park KH. Xanthones from
Cudrania tricuspidata displaying potent
α-glucosidase inhibition. Bioorg Med Chem Lett, 17, 6421-6424 (2007)

,


Singh AP, Singh T. Biotechnological applications of wood-rotting fungi: A review. Biomass Bioenergy, 62, 198-206 (2014)


Song YE, Lee IS, Song EJ, Choi MK, Han HA, Shin SH, Choi SR, Lee KK, Kim MK, Park SY. Changes of off-odor constituent and parishin derivatives of fermentation of
Gastrodia elata rhizome by lactic acid bacteria strains. Korean J Food Nutr, 30, 973-982 (2017)

Taguchi H, Yoshioka I, Yamasaki K, Kim IH. Studies on the constituents of
Gastrodia elata blume. Chem Pharm Bull, 29, 55-62 (1981)


Tang C, Wang L, Cheng M, Zhang X, Liu X, Xiao H. Rapid and sensitive analysis of parishin and its metabolites in rat plasma using ultra high performance liquid chromatography-fluorescence detection. J Chromatogr B, 973, 104-109 (2014)

,


Tian YH, Kim HC, Cui JM, Kim YC. Hepatoprotective constituents of
Cudrania tricuspidata. Arch Pharm Res, 28, 44-48 (2005)

,


Upadhyaya J. Biotransformation of major ginsenosides to rare ginsenosides, C-K, C-Mc, and C-Y by honey mushroom mycelia. Ph D Thesis, Jeonbuk National Unversity, Korea, p 22-136 (2015)

Vrabl P, Schinagl CW, Artmann DJ, Heiss B, Burgstaller W. Fungal growth in batch culture-What we could benefit if we start looking closer. Front Microbiol, 10, Article 2391 (2019)

,

,


Wang R, Sun JC, Lassabliere B, Yu B, Liu SQ. Biotransformation of green tea (
Camellia sinensis) by wine yeast
Saccharomyces cerevisiae. J Food Sci, 85, 306-315 (2020)

,


Xin LT, Yue SJ, Fan YC, Wu JS, Yan D, Guan HS, Wang CY.
Cudrania tricuspidata: An updated review on ethnomedicine, phytochemistry and pharmacology. RSC Adv, 7, 31807-31832 (2017)


Yang H, Zhang L. Changes in some components of soymilk during fermentation with the basidiomycete
Ganoderma lucidum. Food Chem, 112, 1-5 (2009)


Yim EJ, Jo SW, Lee ES, Park HS, Ryu MS, Uhm TB, Kim HY, Cho SH. Fermentation characteristics of mulberry (
Cudrania tricuspidata) fruit vinegar produced by acetic acid bacteria isolated from traditional fermented foods. Korean J Food Preserv, 22, 108-118 (2015)


Youn KS, Kim JW. Antioxidant and angiotensin converting enzyme I inhibitory activities of extracts from mulberry (
Cudrania tricuspidata) fruit subjected to different drying methods. J Korean Soc Food Sci Nutr, 41, 1388-1394 (2012)


Zhu HY, Zhang D, Zhang Q, Zhao Y, He ZM, Gao YG, Zhang LX. 4-Hydroxybenzyl alcohol derivatives and their sedative–hypnotic activities. RSC Adv, 8, 19539-19550 (2018)

,

,


Zou YS, Hou A, Hou AJ, Zhu GF. Isoprenylated xanthones and flavonoids from
Cudrania tricuspidata. Chem Biodiver, 2, 131-138 (2005)

,