1. 서론
염증반응은 외부의 물리적·화학적 자극뿐만 아니라 바이러스나 세균, 곰팡이와 같은 외부 병원체의 침입에 대한 내부 생체 조직의 방어기작으로 과도하게 발생하면 체내 조직 손상, 종양 성장 유도, 아토피성 피부염, 류마티스 관절염과 같은 다양한 염증성 질환을 유발하게 된다(Lebert과 Huttenlocher, 2014; Medzhitov, 2010; Zhou 등, 2016). 그람음성균의 세포외막에 존재하는 lipopolysaccharide(LPS)는 염증반응에 관여하는 대식세포의 막 수용체인 toll-like receptor 4(TLR4)를 자극하며 세포 내부로 신호를 전달하여 전사인자인 nuclear factor kappa-B(NF-κB)의 활성화를 유도한다(Sharif 등, 2007; Takeuchi과 Akira, 2010). 활성화된 NF-κB는 inhibitor kappa-B(IκB)와 분리된 후 핵 내로 이동하여 inducible nitric oxide synthase (iNOS)와 cyclooxygenase-2(COX-2)와 같은 효소의 발현 유도를 통해 nitric oxide (NO)와 prostaglandin E2(PGE2)와 같은 다양한 염증매개인자의 생성을 증가시킨다(Yoon 등, 2015). 또한, tumor necrosis factor-α(TNF-α), interleukin-1β (IL-1β)와 같은 염증성 사이토카인들의 생성을 증가시킨다(Surh 등, 2001). 이러한 염증매개인자들의 과도한 증가로 인해 염증반응이 지속되면, 만성 염증 질환의 원인으로 작용하며 NO나 PGE2, 염증성 사이토카인의 생성 억제는 염증 질환의 예방과 치료에 있어서 중요한 요소로 여겨지고 있다(Andreakos 등, 2004; Lee 등, 2019). 지금까지 널리 사용되고 있는 항염증제는 간 손상, 신장기능 저하, 위장관 출혈 및 궤양, 심혈관계 질환 등의 많은 부작용을 초래할 수 있다. 따라서 최근에는 부작용이 적으며 효과적으로 항염 효과를 나타낼 수 있는 천연물을 이용한 소재 개발을 위한 연구들이 진행되고 있다(Park과 Kim, 2011).
양배추(Brassica oleracea L var. capitata)는 십자화과 채소의 일종으로 phenolic acids, flavonols, anthocyanidins 등과 같은 페놀 화합물뿐만 아니라 glucosinolates, isothiocyanates와 같은 다양한 생리활성물질을 함유하고 있는 것으로 보고되었다(Conaway 등, 2001; Hwang과 Nhuan, 2015; Sang 등, 1984; Singh 등, 2006). 양배추 추출물이 대식세포에서 NO 생성 및 염증 관련 유전자의 발현을 조절하여 항염증 활성을 나타낸다고 보고되었다(Lee 등, 2018). 따라서, 본 연구에서는 염증에 효과가 있는 양배추를 L. plantarum과 L. acidophilus 복합배양을 통해 발효물을 제조하고 LPS로 유도된 Raw264.7 cell에서 NO, PGE2 및 염증성 사이토카인 생성에 미치는 영향과 염증매개인자의 생성에 중요한 역할을 하는 단백질 발현 및 NF-κB 활성화 여부를 조사하여 유산균 복합배양 양배추 발효물의 항염증 효능을 확인하고자 하였다.
2. 재료 및 방법
양배추 발효를 위한 균주는 국립농업과학원 씨앗은행(KACC)로부터 분양받은 Lactiplantibacillus plantarum ATCC14917(type strain)와 Lactobacillus acidophilus ATCC4356(type strain)를 사용하였다. 0.5 mm로 분쇄한 후 살균한 양배추에 L. plantarum와 L. acidophilus 균주를 동일한 비율로 혼합하여 양배추 중량당 0.5%로 접종하고 37°C에서 7일간 정치 배양하였다. 배양이 끝난 후 동결건조기(Ilshin Lab, Dongducheon, Korea)를 이용하여 건조하였고 건조된 양배추 발효물을 멀티밀(Dsml-370, Duksan korea)을 사용하여 100 mesh로 분쇄하여 −20°C에 보관하며 실험에 사용하였다.
Raw264.7 macrophage cell(40071, KCLB, Seoul, Korea)은 10% fetal bovine serum(FBS, Welgene, Gyeonsan-si, Korea)와 1X antibiotic-antimycotic를 함유하는 Dulbecco’s Modified Eagle’s Medium(DMEM) 배지를 이용하여 37°C, 5% CO2로 유지한 배양기에서 배양하였다. 배지는 2일마다 교체하였으며 cell confluency가 70-80%에 도달하였을 때 cell scraper를 이용하여 계대배양하였다.
Raw264.7 세포에 대한 혼합물의 세포 독성을 3-(4,5-dimethylthiazole-2-yl)-2,5-diphenyl-tetrazoliumbromide(MTT) 시약을 이용하여 측정하였다(Mosmann, 1983). 10% FBS, 1X antibiotic-antimycotic를 포함하는 DMEM를 이용하여 세포를 96-well plates에 분주한 뒤 12시간 동안 배양하였다. 배지로 희석한 시료를 농도별로 세포에 처리하고 24시간 동안 배양하였다. 배지를 제거하고 배지로 희석한 MTT 용액(최종농도: 0.5 mg/mL)을 각 well에 100 μL씩 처리하여 37°C에서 4시간 동안 반응시켰다. MTT가 포함된 배지를 제거하고 생성된 formazan을 녹이기 위해 100 μL의 dimethyl sulfoxide(DMSO)으로 10분 동안 상온에서 반응시켰다. 흡광도 측정을 위해 540 nm에서 microplate reader(Versamax, Molecular Devices, Sunnyvale, CA, USA)를 이용하여 측정하였다. 시료를 처리하지 않고 배지만 단독 처리한 대조군과 비교하여 세포 생존율을 %로 나타내었다.
생성된 NO 함량은 Nitric Oxide Assay Kit(Thermofisher, Waltham, MA, USA)를 이용하여 측정하였다. 세포를 6 well plate에 1×105 cells/well로 분주한 후 12시간 배양하였다. 3시간 동안 시료를 농도별로 전처리한 후, LPS(1 μg/mL) from Escherichia coli O55:B5(Sigma aldrich, St. Louis, MA, USA)를 처리하여 20시간 배양하였다. 배양 후 제조사의 mannual에 따라 실험을 진행하여 흡광도를 측정하고 Standard의 농도별 흡광도로 표준곡선을 이용하여 배지의 NO 농도를 결정하였다.
NO 생성량 측정과 동일한 농도로 시료와 LPS를 처리한 후 배지를 원심분리하여 상층액을 분리하고 실험에 사용하기 전까지 −70°C에 보관하였다. PGE2와 사이토카인 농도는 enzyme-linked immunosorbent assay(ELISA) kit (R&D Systems, Minneapolis, MN, USA)를 이용하여 흡광도를 측정하고 Standard의 농도별 흡광도로 표준곡선을 이용하여 배지의 사이토카인 농도를 결정하였다.
시료와 LPS를 처리한 후 phosphate buffered saline (PBS)로 세포를 세척하였다. RIPA buffer(50 mM Tris-HCl, pH 8.0, 150 mM NaCl, 1% NP-40, 0.5% Nadeoxycholate and 0.1% SDS)로 세포를 용해시킨 후 12,000 ×g, 4°C에서 20분간 원심분리하였다. 원심분리하여 얻은 상층액은 BCA protein assay kit(Thermofisher, Waltham, MA, USA)를 이용하여 단백질 농도를 측정하였다. 단백질 20 μg을 10% SDS-PAGE로 단백질을 분리하고 분리된 단백질은 PVDF membrane으로 옮긴 다음 실온에서 blocking buffer(Biorad, Hercules, CA, USA)를 이용하여 5분간 blocking 하였다. 1차 항체를 1:1,000-1:3,000으로 희석하여 4°C에서 overnight 시킨 후 TBS-T (10 mM Tris, 100 mM NaCl, 0.1% Tween20) 용액으로 membrane을 10분씩 3회 세척하였다. 2차 항체는 1:2,500으로 희석하여 상온에서 2시간 반응시킨 후 TBS-T로 membrane을 10분씩 3회 세척하였다. Membrane의 단백질 발현은 ECL detection kit(Thermofisher, Waltham, MA, USA)를 처리한 후 image reader(Microchemi 4.2, DNR, Neve Yamin, IS)를 이용하여 단백질 밴드 확인 및 정량하였다.
3. 결과 및 고찰
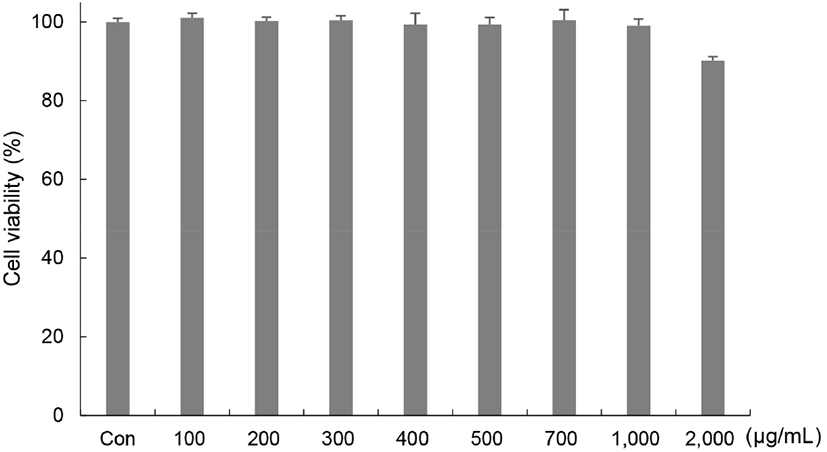
유산균 복합배양 양배추 발효물의 항염증 효과를 확인하기 위해 RAW264.7 세포에 독성을 미치지 않는 농도를 결정하기 위해 MTT assay를 수행하였다. RAW264.7 세포주에 유산균 복합배양 양배추 발효물을 농도별(100, 200, 300, 400, 500, 700, 1,000, 2,000 μg/mL)로 처리한 결과 유산균 복합배양 양배추 발효물 1,000 μg/mL 이하의 농도에서 99.05% 이상의 세포생존율을 나타내며, 2,000 μg/mL에서는 89.13%로 세포생존율이 감소함을 확인하였다. 따라서 RAW264.7 세포만 배양한 대조군에 비해 세포독성을 나타내지 않는 유산균 복합배양 양배추 발효물 1,000 μg/mL 이하로 설정하여 항염증 효과를 확인하였다(Fig. 1).
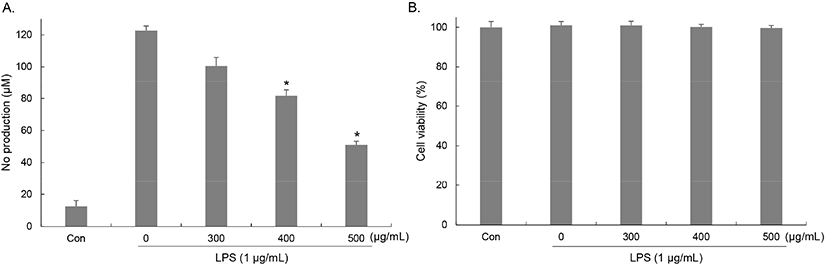
LPS에 의해 활성화된 대식세포는 NO나 염증성 사이토카인과 같은 염증 매개인자를 유리하여 외래인자를 제거하는 중요한 역할을 하지만 박테리아를 NO는 과도하게 생성되면 염증을 일으켜 체내 조직의 손상, 유전자 변이, 신경 손상 등을 일으키고, 여러 가지 유해물질을 생성하여 암의 형성과 진행에도 중요한 역할을 한다(Jung 등, 2010). RAW264.7에서 LPS에 의해 유도된 NO 생성에 대한 유산균 복합배양 양배추 발효물의 억제 효과를 griess 시약을 이용하여 측정하였다. RAW264.7 세포에 배지만 처리한 대조군에 비해 LPS를 단독 처리한 군에서는 NO의 생성이 12.51 μM에서 122.65 μM로 급격하게 증가하였다. 유산균 복합배양 양배추 발효물을 농도별(300, 400, 500 μg/mL)로 처리한 결과, NO 생성이 억제되어 100.51, 81.7, 51.01 μM로 감소하였으며 농도별로 각각 18.04, 33.38, 58.40%의 억제율을 나타냈다(Fig. 2(A)). 또한, 유산균 복합배양 양배추 발효물과 LPS 처리가 세포 생존율에 영향을 미치는지를 확인하기 위해 동일한 조건으로 처리 후 세포 생존율을 측정한 결과, 세포 생존율이 감소하지 않았으며 NO 생성 억제 효과가 세포생존율 감소에 의해 나타난 것이 아님을 확인하였다(Fig. 2(B)).
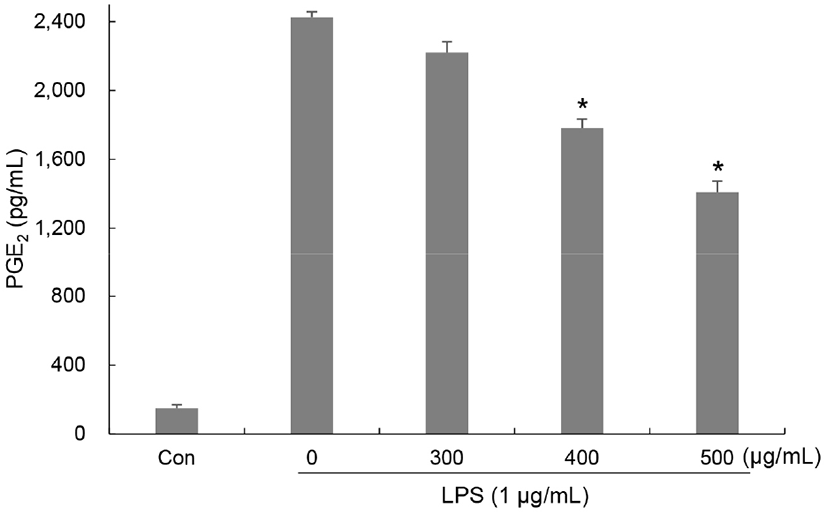
Arachidonic acid로부터 생성되는 prostaglandin은 염증반응을 유도하는 중요한 인자로 그 중 PGE2는 prostaglandin endoperoxide synthase 효소인 COX-2에 의해 합성되는 염증 유발인자로 염증부위로 면역세포의 이동 및 염증성 사이토카인의 생성을 유도한다. 과도하게 생성된 PGE2에 의해 통증, 발열을 일으키며 다양한 염증성 질환을 유발한다(Harris 등, 2002; Jang 등, 2006). RAW264.7에서 LPS에 의해 유도된 PGE2 생성에 대한 유산균 복합배양 양배추 발효물의 억제 효과를 ELISA를 이용하여 확인하였다. RAW264.7 세포에 배지만 처리한 대조군에 비해 LPS를 단독 처리한 군에서는 PGE2의 생성이 150.61 pg/mL에서 2,425.72 pg/mL로 급격하게 증가하였다. 유산균 복합배양 양배추 발효물을 농도별(300, 400, 500 μg/mL)로 처리한 군은 PGE2의 생성이 억제되어 2,220.89, 1,781.15, 1,409.26 pg/mL로 감소하였으며 농도별로 각각 8.43, 26.56, 41.90%의 억제율을 나타냈다(Fig. 3).
이 같은 결과를 통해서 유산균 복합배양 양배추 발효물이 LPS에 의해 유도된 과도한 NO와 PGE2 생성을 억제하여 염증반응 억제 효능을 나타냄을 의미한다. Park 등의 연구에 의하면 유산균 균주를 이용하여 발효한 층꽃나무 추출물이 RAW264.7 세포의 NO와 PGE2 생성을 억제한다고 보고하였으며 이는 본 연구결과와 일치하였다(Park 등, 2018).
염증반응 시 TNF-α, IL-1β와 같은 사이토카인들의 생성이 증가되고, 대식세포와 같은 면역세포에서 이들을 분비하여 다양한 염증반응을 매개하며 NO와 PGE2 생성을 유도한다. 그 중 IL-1β는 염증부위에 림프구와 호중구 등과 같은 세포의 침윤을 상승시키며 NO의 생성을 유도한다(Baek 등, 2012). TNF-α는 다른 염증성 사이토카인의 생성과 NO, PGE2의 생성을 유도하며 염증반응 초기에 염증 부위로 호중구를 유인하여 부종 유발 및 종양 형성에 관여한다고 알려져 있다(Kielian 등, 2004; Levine 등, 1990; Zhang 등, 1992). RAW264.7에서 LPS에 의해 유도된 IL-1β와 TNF-α 생성에 대한 유산균 복합배양 양배추 발효물의 억제 효과를 ELISA를 이용하여 확인하였다. IL-1β는 RAW264.7 세포에 배지만 처리한 대조군에 비해 LPS를 단독 처리한 군에서는 40.91 pg/mL에서 380.07 pg/mL로 급격하게 증가하였다. 유산균 복합배양 양배추 발효물을 농도별 (300, 400, 500 μg/mL)로 처리한 결과, IL-1β의 생성이 억제되어 350.63, 290.27, 190.99 pg/mL로 감소하였으며, 농도별로 각각 10.11, 25.58, 51.03%의 억제율을 나타냈다(Fig. 4(A)).
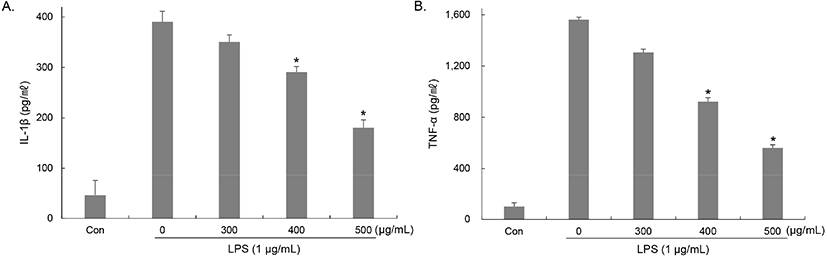
TNF-α는 RAW264.7 세포에 배지만 처리한 대조군에 비해 LPS를 단독 처리한 군에서는 100.07 pg/mL에서 1,561.12 pg/mL로 급격하게 증가하였다. 유산균 복합배양 양배추 발효물을 농도별(300, 400, 500 μg/mL)로 처리한 결과, TNF-α의 생성이 억제되어 1,306.60, 923.19, 562.37 pg/mL로 감소하였으며 농도별로 각각 16.30, 40.87, 64.04%의 억제율을 나타냈다(Fig. 4(B)). Choi 등(2020)은 황기 및 추출물이 LPS에 의해 염증반응이 유도된 대식세포에서 NO 및 PGE2뿐만 아니라 염증성 사이토카인 (IL-1β, IL-6, TNF-α)의 생성을 저해시켜 항염증 효과를 나타낸다고 보고하였다. 따라서 이러한 결과들은 유산균 복합배양 양배추 발효물이 IL-1β, TNF-α 생성 감소에 효과가 있음을 나타내는 것으로 NO와 PGE2 같은 염증매개인자뿐만 아니라 염증성 사이토카인의 생성을 억제하여 염증반응을 억제할 수 있음을 의미한다.
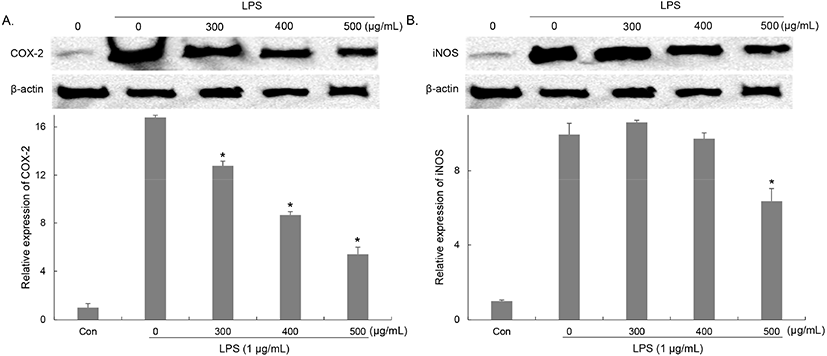
NO 생성에 관여하는 NO synthase(NOS) 중, iNOS는 대식세포에 작용하여 LPS, TNF-α 등에 의해 활성화되며, L-arginine으로부터 NO를 생성한다(Moncada 등, 1991). COX-2는 염증부위에서 arachidonic acid로부터 prostaglandins(PGs)을 합성하며 TNF-α, IL-1β와 같은 염증성 사이토카인의 생성을 증가시킨다(Liu와 Malik, 2006). LPS 처리에 의한 염증매개인자의 생성 증가에 관여하는 iNOS와 COX-2의 단백질 발현량을 NO와 사이토카인과 동일한 조건으로 세포를 처리한 후 western blot을 이용하여 확인하였다. COX-2의 경우, 배지만 처리한 대조군에 비해 LPS 단독처리한 군에서는 16.78배 발현이 증가하였고, 유산균 복합배양 양배추 발효물(300, 400, 500 μg/mL)을 처리한 군에서는, 23, 48, 67%의 감소하는 것을 확인하였다(Fig. 5(A)). iNOS의 경우, 배지만 처리한 대조군에 비해 LPS 단독처리에 의해 증가된 iNOS는 유산균 복합배양 양배추 발효물을 처리한 결과, 300, 400 μg/mL에서는 큰 변화가 나타나지 않았지만 500 μg/mL에서는 36.15% 감소하였다(Fig. 5(B)). Lee 등은 발효 추출물 처리에 의해 LPS로 염증반응을 유도한 RAW264.7 세포에 NO와 PGE2의 생성이 감소되었으며, 이는 iNOS와 COX-2의 발현조절에 의한 것임을 보고하였다(Lee 등, 2015). 따라서 유산균 복합배양 양배추 발효물이 NO, PGE2와 같은 염증매개인자의 생성을 유도하는 단백질의 발현을 조절하여 염증반응을 억제하는 효과를 나타냄을 확인하였다.
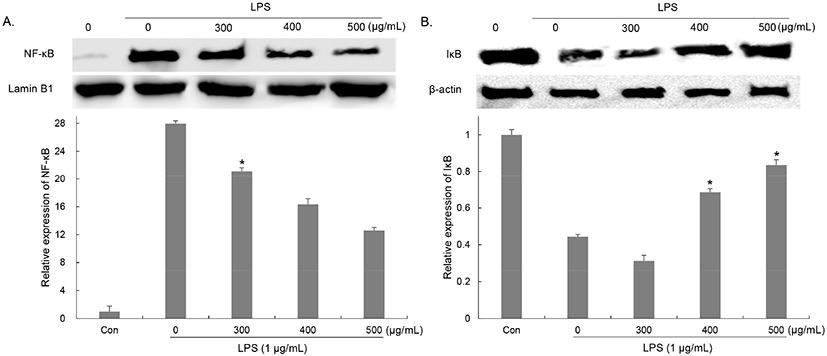
두 개의 subunit(p50, p65)으로 구성된 NF-κB는 정상적인 조건에서는 inhibitor-κB(IκB)와 결합되어 비활성 상태로 존재하지만 LPS와 같은 외부자극에 의해 염증반응이 발생하면 IκB는 IKKα/β에 의해 인산화 및 ubiquitination 되어 분해되고, IκB와 분리된 NK-κB는 활성화되어 핵 안으로 이동하여 염증매개인자의 발현을 유도한다(Surth 등, 2001). NF-κB의 활성화 및 핵 내 이동 억제는 염증반응 억제에 있어서 중요한 요소로 작용하므로 유산균 복합배양 양배추 발효물이 LPS 처리에 의한 NF-κB의 활성화 및 핵 내 이동을 억제할 수 있는지 western blot을 이용하여 확인하였다. 배지만 처리한 군에 비해 LPS 처리에 의한 NK-κB 단백질의 핵 내 이동 약 27.96배 증가하였지만 유산균 복합배양 양배추 발효물(300, 400, 500 μg/mL) 처리한 군은 LPS 단독 처리군 대비 핵으로 이동한 NK-κB 단백질 양이 각각 24.43, 41.55, 54.99%로 감소하는 것을 확인하였다(Fig. 6(A)). 또한 IκB의 분해를 확인한 결과, 배지만 처리한 군에 비해 LPS 처리에 의한 세포질 내 IκB는 약 0.4배로 감소하였지만, LPS 단독 처리군 대비 유산균 복합배양 양배추 발효물 (300, 400, 500 μg/mL) 처리한 군은 세포질에 존재하는 IκB 단백질 양이 70.36, 154.75, 188.51%로 증가하는 것을 확인하였다(Fig. 6(B)). Lee 등(2015)은 발효 추출물 처리에 의해 LPS로 염증반응을 유도한 RAW264.7 세포에서 NO와 PGE2뿐만 아니라 염증성 사이토카인과 같은 염증매개인자의 생성이 감소되었으며, 이는 NF-κB의 활성화 조절에 의한 것임을 보고하였다. 이러한 결과를 통해서 유산균 복합배양 양배추 발효물이 IκB 분해 및 NF-κB의 인산화를 저해함으로서 NF-κB의 핵 내 이동 및 iNOS 및 COX-2의 발현을 감소시켜 염증매개인자와 염증성 사이토카인의 생성을 억제시킴으로서 염증반응 억제 효과를 나타냄을 알 수 있었다.
따라서 염증반응을 억제할 수 있는 유산균 복합배양 양배추 발효물은 염증반응 조절을 위한 항염증 기능성 소재로 활용 가능할 것으로 사료된다.
