서 론
새싹채소는 싹채소, 어린 싹이라고도 불리며, 종자로부터 발아하여 모든 부위를 이용하거나 배축부를 절단하여 이용하는 채소이다. 새싹채소의 경우, 성장을 위해 영양소를 생합성함으로 성장한 채소에 비해 영양성분이나 생리활성 효과가 우수하다는 보고가 있다. 이에 평상시 미네랄 및 비타민 등을 쉽게 섭취할 수 있는 장점이 있다(Kim과 Lee, 2010). 인삼의 잎을 이용하기 위해서 재배를 하게 되면 밭에서 재배되고 있는 인삼은 더 성장할 수 없게 되어 뿌리와 잎 모두 사용하기 어렵게 된다. 또한 인삼의 잎은 경화되어 있을 뿐 아니라, 쓴맛이 너무 강하여 쌈 채소로 이용하기엔 어려움이 크다. 따라서, 묘삼을 이용하여 새싹인삼을 만들어 인삼의 모든 부위를 다 식용으로 사용할 수 있도록 하여 소비자들에게 제공되고 있다(Seong 등, 2019).
인삼은 현재 뿌리만 사용되는데 이전 연구에 따르면 잎에도 많은 진세노사이드가 함유되었다는 보고가 있다(Kim 등, 2010). 삼 종류의 주요 성분 중의 하나인 ginsenoside는 ginseng과 glucoside의 합성어로 triterpenoid의 dammarane계의 인삼속의 식물에만 존재하는 특유 사포닌이다. C-3, C-6 또는 C-20번 위치에 glucose, xylose와 rhamnose 등의 당을 결합하는 일반적인 소수성 스테로이드 형태의 구조를 가지며, 이들은 protopanaxadiol(PD), protopanaxatriol(PT), oleanolic acid 및 octillol 계로 나눠진다(Park 등, 2017). PD계 ginsenoside는 Rb1와 Rb2, Rb3, Rc, Rd 등이 있고, PT계는 Re와 Rf, Rg1 등이 있다(Park 등, 2005). 한편, 잎에는 지하부에 함유되어 있지 않은 ginsenoside F1과 F3 등과 같은 성분 등이 존재한다(Lee 등, 2004).
인삼과 같은 식물체는 특유의 쓴맛이 있어 생으로 섭취하기에 어려움이 있다. 식품의 가공 공정 중 하나로 볶음 공정은 쓴맛을 지닌 식품의 갈변반응을 촉진하며, 향기성분을 생성함으로써 쓴맛을 감소시켜 기호성을 높여 주는 것으로 보고되어 있다(Cho and Joo, 2012). 침출차에 대한 대중의 관심이 높아지면서 여주(Ahn 등, 2015), 옥수수(Lee 등, 2017) 및 옻씨(Jin 등, 2017) 등과 같이 다양한 식물체를 온도와 시간에 따른 볶음 처리 연구가 진행되었고 이러한 공정은 항산화 활성과 총 폴리페놀 함량 등에 영향을 주는 것으로 보고되었다. 이러한 천연 재료를 볶음 처리하여 기호성과 상품성을 증진시키는 다양한 연구가 진행되고 있다. 따라서, 본 연구에서는 새싹인삼의 볶음 횟수가 증가함에 따라 변화되는 이화학적 특성, 총 phenolics와 총 flavonoids, 갈변물질, ginsenosides, phenolic acids, flavonols 함량 및 항산화 활성 등의 최적 조건을 분석하였다.
재료 및 방법
새싹인삼은 경상남도 사천시 서포면 소재 농업회사법인 드림팜의 식물공장에서 재배된 것을 공급받아 사용하였다. 온도 17±2°C, 습도 95±2%, 및 LED 광원(적색, 청색과 백색 혼합 광원) 400±200 lx로 자동 제어된 식물공장에서 30일간 재배된 새싹인삼을 공급받아 사용하였다. 공급받은 새싹인삼은 큰 줄기에서 두 줄기로 나누어져 각각 줄기에서 잎이 5개 생성되었고, 지상부(잎과 줄기)와 지하부(뿌리)의 평균 길이는 각각 19.52 cm와 13.11 cm였고 평균 무게는 각각 1.4 g과 0.9 g이었다. 21 종의 ginsenosides 표준품(Rb1, Re, Ro, Rg2, Rg3, Rb2, Rd, F2 및 compound K 등)은 KOC바이오텍(Daejeon, Korea)에서 구입하였다. Phenolic acids 표준품(gallic acid, chlorogenic acid, protocatechuic acid, vanillic acid, ferulic acid 및 ventaric acid)과 flavonols 표준품(epigallocatechin, catechin, vanilin, rutin, catechin gallate, quercetin 및 formonoetin)은 Sigma-Aldrich 사에서 구입하였다. 총 phenolics 측정에 사용된 Folin-Cicalteu phenol과 총 flavonoids 함량 측정에 사용된 diethyleneglycol은 Sigma-Aldrich(St. Louis, MO, USA)에서 구입하여 사용하였다. 항산화 활성에 사용된 2,2'-diphenyl-1-picrylhydrazyl(DPPH), 2,4,6-azino-bis(3-ethylbenzothiazoline-6-sulphnoic acid) diammonium salt(ABTS), thiobarbituric acid(TBA) 및 trichloroacetic acid(TCA) 역시 Sigma-Aldrich Co.에서 구입하여 사용하였다. HPLC-grad water, acetonitrile 및 methanol은 Fisher Scientific(Fairlawn, NJ, USA)에서 구입하였고, 이외 분석에 사용된 시약은 1급으로 구입하여 실험에 사용하였다.
새싹인삼은 3회 세척하고 물기를 제거하고 지상부(잎과 줄기)와 지하부(뿌리)로 구분한 후 100°C에서 10분간 증자하였다. 지상부는 150°C에서 5분간 1, 2 및 3회 볶음 처리하였고, 지하부는 200°C에서 5분간 1, 2 및 3회 볶음 처리하였다(Fig. 1). 볶음 처리한 시료는 분쇄 후 사용 전까지 −20°C에서 보관하였다.
pH는 분쇄한 부위별 및 횟수별 시료 1 g을 증류수로 10배 진탕하여 pH meter(MP 200 pH meter, Schwerzenbach, UK)를 사용하여 측정하였다. 산도는 각각의 시료 1 g에 증류수 50 mL를 가하여 현탁 시킨 후 그 상등액을 0.1 N NaOH로 pH 8.20까지 적정하여 그 소모량을 젖산량으로 환산하여 %로 나타내었다.
F: factor of 0.1 N NaOH
환원당 함량은 각각의 시료 1 g에 10배의 증류수를 가한 것을 사용하였다. 즉, 각각의 시료 현탁물 0.1 mL에 DNS (dinitro salictlic acid) 시약 1 mL를 가하여 100°C에서 20분간 발색시키고, 냉각시킨 후 570 nm에서 흡광도를 측정하였다. 환원당 표준 물질은 glucose를 사용하여 작성된 표준 검량곡선으로부터 값을 산출하였다.
지방산 분석은 Cho 등(2017)의 방법을 약간 변형하여 gas chromatograph(GC, Agilent 7890A system, Agilent Technologies Inc., Wilmington, DE, USA)를 사용하여 측정하였다. 시료 1 g을 시험관에 정확히 칭량하고 0.5 N 메탄올성 NaOH를 3 mL 분주한 후 100°C에서 10분간 열처리하여 지방산과 글리세롤 가수분해한 후 삼불화붕소(BF3) 2 mL를 첨가하고 교반한 후 다시 30분간 열처리하여 지방산의 메틸에스테르화를 진행하였다. 메틸에스테르화 반응이 끝난 후 이소옥탄 1 mL를 첨가하고, 혼합 및 방치시켜 이소옥탄층만을 회수하여 무수황산나트륨과 함께 탈수한 뒤 0.45 μm membrane filter로 여과하여 GC로 분석하였다. 이동상은 질소 가스를 사용하였으며, 속도는 1 mL/min으로 유지하였다. 오븐의 온도는 140°C에서 5분간 유지한 후 1분당 20°C만큼 상승시켜 180°C에서 2분간 유지하였고, 5°C만큼 상승시켜 230°C까지 온도를 올려 35분간 유지하였다. Injector 온도는 220°C로 하였고, FID detector의 온도는 240°C로 하였다.
유리아미노산 분석은 시료 1 g에 증류수 4 mL를 가하여 교반하였다. 60 °C에서 1시간 가수분해한 후 10% 5-sulfosalicylic acid 1 mL를 첨가하여 4°C에서 2시간 방치시켜 단백질을 침전시킨다. 3분간 원심분리하여 얻은 상등액을 0.45 μm membrane filter(Dismic-25CS, Toyoroshikaisha Ltd., Tokyo, Japan)로 1차 여과시켜 60°C에서 감압 농축하였다. 농축된 시료는 lithium citrate buffer(pH 2.2) 2 mL에 용해 후 0.45 μm membrane filter로 여과한 여액을 아미노산 자동분석기(L-8900, Hitachi High-Technologies Corp., Tokyo, Japan)를 이용하여 분석하였다.
무기질 분석은 시료 0.5 g을 시험관에 칭량하고, 여기에 70% 질산 용액을 10 mL 첨가하여 microwave high pressure digestion system(Ultrawave 2.0, Milestone, Bergamo, Italy)로 분해하였다. 분해 후 최종 부피가 50 mL가 되도록 증류수로 정용하여 liquid chromatography-inductively coupled plasma mass spectrometer(NexION 350 ICP MS, PerkinElmer Inc., Waltham, USA)로 분석하였다.
총 phenolics와 총 flavonoids 함량 분석을 위한 추출은 분쇄한 시료 1 g에 50% 발효 주정(I1-San Trading Co., Ltd., Haman, Korea) 10 mL를 분주하여 상온에서 12시간 동안 추출하여 원심분리한 후 상등액을 0.45 μm membrane filter (Dismic-25CS, Toyotoshikaisha Ltd., Tokyo, Japan)로 여과하여 추출물을 제조하였다. 총 phenolics 함량은 희석된 시료와 25% Na2CO3 용액을 각각 0.5 mL씩 시험관에 분주하여 3분간 정치시킨 후 2 N Folin-Ciocalteu phenol 시약 0.25 mL 첨가 후 흔들어 30°C에서 1시간 발색시킨 후 분광 광도계(UV-1800 240V, Shimadzu Corp., Kyoto, Japan)를 사용하여 750 nm에서 측정하였고 gallic acid를 이용하여 작성된 표준 검량곡선에 대입하여 값을 계산하였다. 총 flavonoids 함량은 추출물 0.5 mL를 시험관에 분주하고, diethylene glycol 용액 1 mL와 1 N NaOH 0.01 mL를 첨가한 후 수욕상(37°C)에서 1시간 반응시킨 후 420 nm(UV-1800 240V, Shimadzu Corp.)로 측정하였으며, Rutin을 이용하여 작성된 표준 검량곡선으로부터 함량을 계산하였다. 갈변물질은 시료 1 g에 증류수를 10 mL 가한 후 1시간 동안 교반한 후 원심분리하여 상등액을 취하여 420 nm(UV-1800 240V, Shimadzu Corp.)에서 측정하였다.
Ginsenosides 유도체 분석은 Jin 등(2012)의 방법을 약간 변형하여 high performance liquid chromatography(HPLC, Agilent 1260 system, Agilent Technologies Inc., Waldbronn, Germany)를 이용하여 실시하였다. 분쇄된 시료 1 g에 HPLC water 20 mL를 가하여 항온수조(70°C)에서 1시간 추출하였고, 이를 원심분리하여 0.45 μm membrane filter로 여과하였다. 이를 2회 반복하여 얻은 추출물을 60°C에서 감압농축 후 HPLC water 2 mL로 용해하여 0.45 μm membrane filter로 여과한 여액을 분석 시료로 사용하였다. 시료 주입량은 10 μL, 유속은 1.0 mL/min을 유지하였고, 칼럼은 TSKgel ODS-100Z를 사용하였다. 이동상 용매는 HPLC water(A 용매)와 HPLC acetonitrile(B 용매)로 사용하였으며, 분석 조건은 A 용매 기준으로 10 min-81%, 15 min-80%, 40 min-77%, 75 min-65%, 90 min-10% 105 min-81%를 바탕으로 하여 203 nm에서 분석하였다.
Phenolic acids 및 flavonols 유도체 분석은 Hwang 등(2017)의 방법을 약간 변형하여 HPLC(Agilent 1260 system, Agilent Technologies Inc.)로 분석하였다. XBridge™ C18 칼럼을 사용하였고, 칼럼 온도는 30°C, 시료 주입량은 10 μL, 유속은 분당 1 mL를 유지하였다. 분석용매는 0.2% acetic acid in HPLC water(A용매) 및 0.2% acetic acid in acetonitrile(B용매)를 사용하였으며 이동상 조건은 B 용매 기준으로 0 min-0%, 3 min-3%, 5 min-5%, 8 min-10%, 10 min-15%, 15 min-5%, 17 min-8%, 19 min-10%, 20 min-15%, 22 min-20%, 26 min-15%, 27 min-20%, 28 min-30%, 32 min-40%, 36 min-60%, 37 min-30%, 38 min 40%, 40 min-50%, 45 min-60%, 55 min-80%, 60 min-90% 및 65 min-100%로 유지하였다. 한편, 각각 phenolic acids 유도체는 280 nm 및 flavonols 유도체는 270 nm에서 분석하였다.
DPPH 라디칼 소거활성은 Hwang 등(2013)의 방법에 따라 측정하였다. DPPH 용액 0.8 mL를 시험관에 분주하고 적당히 희석한 시료 0.2 mL를 가하여 10초간 교반한 후 실온에서 30분간 반응시킨 후 분광광도계를 이용하여 525 nm(UV-1800 240V, Shimadzu Corp.)에서 측정하였다. ABTS 라디칼 소거활성 역시 Hwang 등(2013)의 방법에 따라 측정하였다. 7 mM ABTS 용액과 2.45 mM potassuim persulfate 용액을 1:1로 섞어 실온 암실에서 12-16시간 반응하여 ABTS·+ radical을 형성시킨 후 732 nm(UV-1800 240V, Shimadzu Corp.)에서 흡광도 값이 0.7±0.02가 되도록 메탄올로 희석하였고, 희석된 ABTS 용액 0.9 mL와 시료 0.1 mL를 시험관에 분주하여 정확히 3분 후에 측정하였다. Hydroxyl 라디칼 소거활성은 Ahn 등(2015)의 방법에 따라 측정하였다. 10 mM H2O2, 10 mM FeSO4·7H2O-EDTA, 및 10 mM 2-deoxyribose 0.2 mL를 시험관에 분주하고, 시료 1.4 mL를 가하여 37°C에서 4시간 동안 반응시켰다. 이후 1% TBA와 2.8% TCA 1 mL를 분주하고 100°C에서 20분 발색한 후 520 nm(UV-1800 240V, Shimadzu Corp.)에서 측정하였다. 음성대조구는 시료 대신 PBS 완충용액을 사용하였으며, 시료 첨가구와 무첨가구 사이의 차이를 백분율(%)로 나타내었다.
FRAP 환원력 측정은 Hwang 등(2014)의 방법을 조금 변형하여 측정하였다. 30 mM acetate buffer(pH 3.6), 10 mM TPTZ 시약(40 mM HCl) 및 20 mM FeCl3 용액을 10:1:1 (v/v/v)의 비율로 혼합하여 FRAP 측정 시약을 조제하였다. 시료 50 μL와 37°C 항온기에서 15분 예비 반응한 FRAP 시약 950 μL를 시험관에 분주하여 37°C에서 15분 반응시키고, 분광 광도계를 사용하여 593 nm(UV-1800 240V, Shimadzu Corp.)에서 흡광도를 측정하였다. 각 실험은 3회 반복하여 평균±표준편차로 나타내었다.
결과 및 고찰
새싹인삼의 볶음 처리에 따른 이화학적 특성은 Table 1과 같았다. 지상부의 원료에서 pH는 5.72로 나타났으며, 볶음 처리 시간이 증가할수록 pH는 낮아져 15분 볶음 처리하였을 때 5.50로 나타났다. 또한 지하부의 pH의 변화는 원료 5.81에서 15분 볶음 처리하였을 때 5.55로 낮아졌다. 산도는 지상부의 원료에서 3.78%로 가장 높게 나타났으며 볶음 처리하였을 때 산도가 낮아졌으나, 볶음 시간이 증가할수록 산도 또한 증가하였다. 지하부의 산도는 원료에서 3.22%로 높은 수치를 나타냈으며, 15분 볶음 처리하였을 때 2.43%로 가장 낮게 나타났다. 지상부의 환원당은 원료일 때보다 볶음 처리 시간이 5분, 10분 및 15분으로 증가할수록 함량은 각각 3.40 mg/g에서 4.80, 4.55 및 9.56 mg/g으로 원료에 비해 증가하였다. 지하부의 경우 원료에서 9.44 mg/g에서 5분 볶음 처리하였을 때 8.33 mg/g으로 약간 감소하였으나, 볶음 처리 시간이 10분 및 15분으로 증가할수록 함량 또한 16.57 mg/g 및 14.23 mg/g으로 증가하였다. Park 등(1993)은 온도 변화에 따라 인삼을 볶음 처리하여 비교하였을 때 원료에서 5.36에서 4.67로 pH가 낮아졌다고 보고하였다. 또한, 볶음처리와 같은 원료에 가열을 하였을 때 pH가 저하되는 원인은 비효소적 갈변 반응이 발생될 때 생성되는 전구물질인 carbonyl compounds의 작용에 의해 생성되는 유기산에 의한 것이라 판단하였다.
새싹인삼의 볶음 처리에 따른 지방산 함량 비교는 Table 2와 같았다. 지상부의 포화지방산 중 palmitic acid(C16:0), stearic acid(C18:0) 및 myristic acid(C14:0)의 함량이 높았다. 볶음 처리 시간이 증가할수록 palmitic acid의 함량은 원료일 때 261.8 mg/100 g에서 15분간 볶음 처리하였을 때 191.4 mg/100 g으로 함량이 감소하는 것을 보였다. Stearic acid 또한 원료일 때 96.7 mg/100 g으로 나타났으나, 15분 볶음 처리 시 86.0 mg/100 g으로 함량이 감소하였다. Lignoceric acid (C24:0)의 경우 0분 처리 시 검출되지 않았으나, 볶음 처리가 진행됨에 따라 4.3 mg/100 g, 6.4 mg/100 g 및 7.9 mg/100 g으로 증가하였다. 불포화지방산 중 linoleic acid(C18:2c)의 함량이 가장 높았으며, 볶음 처리에 따라 큰 차이를 보이지 않았다. Palmitoleic acid(C16:1)의 경우, 볶음 처리 시간이 증가할수록 7.4 mg/100 g, 8.3 mg/100 g, 10.2 mg/100 g 및 12.3 mg/100 g으로 함량이 증가하였다. α-Linolenic acid (C18:3n3)의 경우, 0분 처리 시 186.0 mg/100 g의 함량을 보였으나, 볶음 처리가 진행되면서 295.9 mg/100 g, 278.1 mg/100 g 및 257.8 mg/100 g으로 함량이 증가하였으며, 볶음 처리에 따른 큰 차이는 없었다. 지하부의 경우 myristic acid는 검출되지 않았으며, palmitic acid의 경우 볶음 처리 시간이 증가하여도 큰 차이를 보이지 않았으나, 볶음 처리를 15분간 진행되었을 때 166.5 mg/100 g으로 가장 낮은 함량을 보였다. Arachidic acid(C20:4n6)는 지하부에선 검출되었으며, 볶음 처리에 따라 6.1 mg/100 g, 6.3 mg/100 g, 7.0 mg/100 g 및 5.4 mg/100 g으로 큰 차이는 보이지 않았다. 불포화지방산 중 linoleic acid는 볶음 처리 시간이 증가함에 따라 0분(291.7 mg/100 g), 5분(297.8 mg/100 g), 10분(302.2 mg/100 g) 및 15분(312.8 mg/100 g)으로 함량 역시 증가하였다. Ecosadienoic acid(C20:2)는 10분간 볶음 처리 시 5.5 mg/100 g으로 가장 높은 함량을 보였으나 유의적 차이를 보이지 않았다.
Jang 등(2018)은 햄프씨드의 가열 처리에 따른 지방산 함량을 분석하였다. 그 결과, 포화지방산의 함량은 2,935.60 mg%의 함량에서 볶음 처리하였을 때 3,164.29 mg/%로 증가하였고, 불포화지방산의 함량은 원료 39,437.51 mg%에서 40,733.91 mg%로 증가하는 것을 보였다. 이에 다른 시료들과 볶음 처리와 비교하였을 때 지방산 함량과 조성은 시료와 시료의 지방산의 조성에 따라 차이가 있는 것으로 예상하였으며, 이에 따른 함량의 증감 차이가 있다고 보고하였다. 본 연구에서는 포화지방산의 함량은 볶음 처리하였을 때 원료에 비해 낮아졌고, 불포화지방산의 함량은 증가하여 시료에 따른 지방산 조성의 차이가 있는 것으로 판단된다.
새싹인삼의 볶음 처리에 따른 지상부 및 지하부의 유리아미노산은 Table 3과 같았다. 지상부의 경우, aspartic acid의 함량은 5분 볶음 처리하였을 때 162.26 mg/100 g으로 가장 높게 나타났으며, 15분 볶음 처리하였을 때 119.34 mg/100 g으로 가장 낮은 함량을 보였다. Glutamic acid 또한 5분 볶았을 때 107.55 mg/100 g의 함량으로 가장 높았으며, 10분 볶음 처리하였을 때는 100.01 mg/100 g으로 큰 차이를 보이지 않았다. γ-Aminobutyric acid 및 대부분의 비필수 유리아미노산의 경우, 볶음 시간이 증가할수록 함량이 감소하는 것으로 나타났다. 필수 아미노산의 경우에도 원료일 때보다 볶음 시간이 증가함에 따라 함량이 감소하는 것으로 나타났다. 지하부의 경우 aspartic acid의 함량이 원료일 때 89.29 mg/100 g의 함량을 보였으며, 15분 볶았을 때 136.69 mg/100 g으로 볶음 처리를 하였을 때 함량이 증가하였다. Alanine의 경우, 볶음 처리를 하지 않았을 때 106.76 mg/100 g의 함량을 보였으나, 15분간 볶음 처리하였을 때 31.11 mg/100 g으로 함량이 감소하는 것을 보였다. 또한 기타 비 필수 아미노산의 경우, 볶음 처리 시간이 증가할수록 함량이 감소하는 것을 보였다. 또한 threonine, valine, isoleucine 및 lysine 등의 모든 필수 아미노산이 함량은 볶음 시간이 길어질수록 함량이 감소하였다.
Kim 등(2019)은 열처리나 증숙 과정 중에 amino carbonyl 반응 중 갈변 반응에 의해 유리아미노산의 함량이 크게 감소한다고 보고하였다. 또한 Van Voekel(2006)은 arginine과 lysine이 amino carbonyl 반응에 가장 먼저 관여하며, 이후 나머지 아미노산들이 반응하여 결국 아미노산의 함량이 크게 감소한다고 보고하여 이는 본 연구와 동일하였다.
새싹인삼의 볶음 처리에 따른 지상부 및 지하부 무기질 함량 비교는 Table 4와 같았다. 지상부 및 지하부 모두 칼륨의 함량이 가장 높았다. 지상부의 칼륨 함량은 0분, 5분, 10분 및 15분 볶음 처리를 하였을 때 34.67 mg/100 g, 34.85 mg/100 g, 33.14 mg/100 g 및 34.11 mg/100 g으로 큰 차이를 보이지 않았다. 지하부 역시 23.06 mg/100 g, 22.96 mg/100 g, 21.32 mg/100 g 및 23.59 mg/100 g으로 볶음 처리에 따른 큰 차이를 보이지 않았다. 인의 함량이 두 번째로 가장 높았으며, 지상부의 경우 0분 및 15분 볶음 처리시 4.20 mg/100 g 및 3.61 mg/100 g으로 15분 볶음 처리 시 가장 낮은 함량을 보였다. 지하부의 경우에도 인이 두 번째로 높은 함량을 나타냈으며, 0분 및 15분 볶음 처리하였을 때 4.26 mg/100 g 및 4.97 mg/100 g으로 큰 차이를 보이지 않았다. 구리, 아연 및 망간은 미량 검출되었으며, 나트륨 또한 평균 2.57 mg/100 g의 함량으로 시료에 열처리를 하여도 무기질의 함량에는 유의적인 차이를 보이지 않았다.
새싹인삼의 볶음 처리에 따른 총 phenolics, 총 flavonoids 및 갈변물질 함량은 Fig. 2와 같았다. 지상부의 총 phenolics 함량은 볶음 시간이 증가할수록 함량이 증가하였으며 원료일 때 5.71 GAE/g에서 15분 볶음 처리 시 7.84 GAE/g으로 나타났다. 지하부 역시 시간이 증가할수록 함량이 증가하였으며, 각 볶음시간 별로 1.37 GAE/g, 2.47 GAE/g, 3.13 GAE/g 및 3.57 GAE/g으로 나타났다(Fig. 2A). 총 flavonoids 함량은 Fig. 2B와 같았으며, 지상부 및 지하부 모두 볶음 시간이 증가할수록 함량이 증가하였다. 지상부의 경우, 원료일 때 7.43 RE/g에서 5분 볶음 처리하였을 때 8.43 RE/g, 10분 볶았을 때 9.80 RE/g 및 15분 볶았을 때 9.95 RE/g으로 증가하였으며, 지하부 또한 원료일 때 1.49 RE/g에서 15분 볶음 처리 시 4.36 RE/g으로 함량이 증가하였다. 지상부의 갈변물질은 원료일 때 2.635 OD420 nm에서 15분 볶음 처리 시 3.022 OD420 nm로 큰 차이를 보이지 않았으며, 지하부의 경우 2.316 OD420 nm에서 2.987 OD420 nm로 유의적 차이를 보이진 않았다(Fig. 2C).
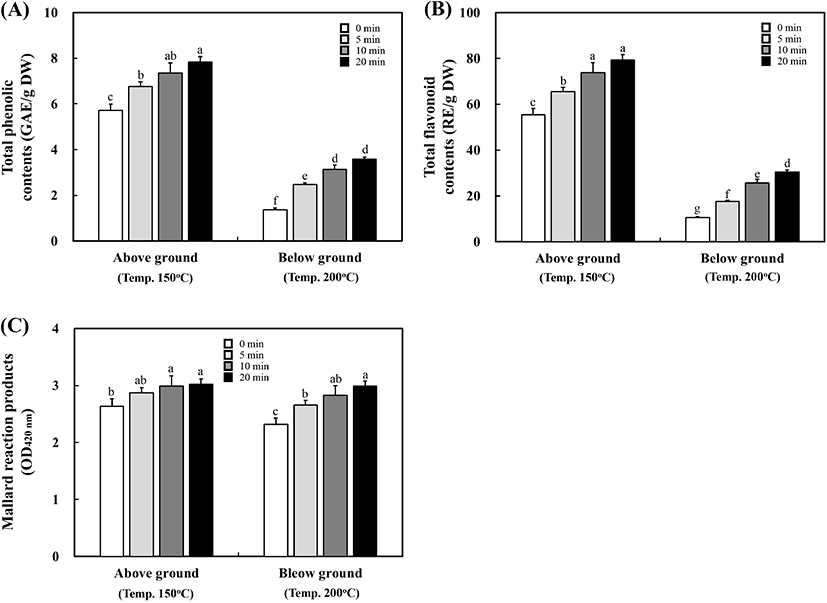
Lee 등(2013)은 결명자의 볶음 처리에 따른 총 phenolics 함량을 비교하였다. 175°C와 200°C에 원료일 때 7.15 mg TAE/g의 함량을 보였으나, 5분 볶음 처리하였을 때 각각 10.95 mg TAE/g 및 11.45 mg TAE/g으로 증가하였으며, 10분 볶음 처리하였을 때 역시 11.34 mg TAE/g 및 12.69 mg TAE/g으로 함량이 증가하였다. 한편, 치커리(Hong 등, 1998), 감국(Kang 등, 2002) 등에서는 볶음처리 하였을 때 총 폴리페놀의 함량이 증가된다고 보고하였다. Kwon 등(1997)은 둥굴레의 볶음 처리에 따라 갈변반응이 증가한다고 보고하였다. 이는 당 및 아미노산 등이 갈변반응이 진행시키는 요인이 되어 둥굴레의 볶음 처리의 결과와 유사하게 새싹인삼에서도 적용된 것으로 판단된다.
새싹인삼의 볶음 처리에 따른 ginsenoside 함량은 Table 5및 Fig. 3과 같았다. 지상부의 ginsenoside Re의 경우, 볶음 시간이 증가할수록 32.67 mg/g에서 21.02 mg/g, 19.97 mg/g 및 19.40 mg/g으로 함량이 감소하는 것으로 나타났으며, Rf의 경우 약 0.32 mg/g으로 큰 차이를 보이지 않았다. Rg2의 경우, 원료일 때 2.34 mg/g에서 15분 볶았을 때 3.13 mg/g으로 함량이 증가하였다. Rd2 또한 원료일 때 3.09 mg/g에서 5분일 때 7.54 mg/g, 10분일 때 8.52 mg/g, 15분 볶았을 때 11.37 mg/g으로 약 4배 증가하였다. F2 및 Rg3 또한 원료일 때 각각 5.23 mg/g 및 0.85 mg/g에서 15분 볶았을 때 7.55 mg/g 및 1.42 mg/g으로 함량이 증가하였다. Compound K는 원료일 때 0.63 mg/g에서 5분 볶았을 때 0.81 mg/g, 10분 볶았을 때 0.98 mg/g에서 15분 볶았을 때 1.81 mg/g으로 함량이 증가하였다. 지하부의 ginsenoside Rg1은 볶음 시간이 증가할수록 함량이 원료일 때 2.31 mg/g에서 15분 볶았을 때 1.92 mg/g으로 감소하였다. Ginsenoside F3, F1 및 protopanaxtriol 화합물은 검출되지 않았다. Ginsenoside Rb1 또한 원료일 때 10.14 mg/g, 5분 볶았을 때 9.02 mg/g, 10분 볶았을 때 8.57 mg/g 및 복음 시간이 15분 볶았을 때 7.07 mg/g으로 함량이 감소하였다. Rc 또한 4.85 mg/g에서 4.18 mg/g, 3.91 mg/g, 15분 볶았을 때 3.26 mg/g으로 감소하였다. Rg3 및 compound K의 경우 10분 볶았을 때 1.77 mg/g 및 1.24 mg/g으로 가장 높았으며, 15분 볶았을 때 0.96 mg/g 및 0.92 mg/g으로 두 번째로 높은 함량을 보였다.
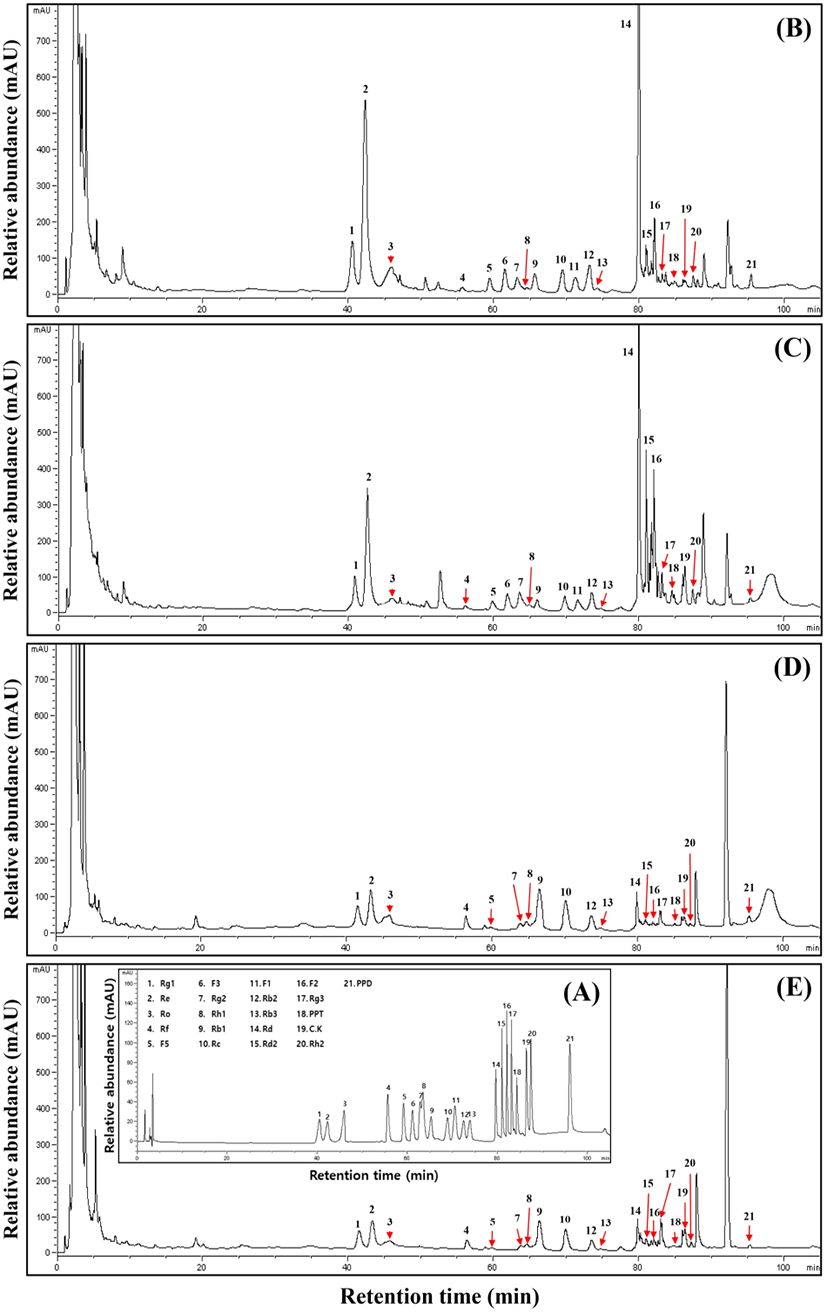
Park 등(1996)은 인삼 박의 볶음 처리에 따른 ginsenosides 함량을 비교하였으며, 이중 ginsenosides Rb1와 Re, Rg1의 함량이 감소하는 것으로 보고하였다. 또한 이는 진세노사이드의 C-20 위치에 결합되어 있는 당이 열이나 산에 의해 쉽게 분해되기 때문이라고 보고하였다. 본 연구에서도 Rb1와 Re 등은 볶음 시간이 증가함에 따라 함량이 감소하였으며, 당이 떨어지면서 기존 화합물의 구조에서 당이 하나씩 떨어진 다른 화합물로 전화되었을 것으로 판단된다.
새싹인삼의 볶음 처리에 따른 지상부 및 지하부의 phenolic acids 및 flavonols 함량은 Table 6과 같았다. 지상부의 gallic acid 함량은 원료일 때 12.26 mg/100 g에서 15분 볶았을 때 33.58 mg/100 g으로 볶음 시간이 증가할수록 함량이 증가하였다. Chlorogenic acid 및 ferulic acid의 함량 역시 볶음 시간이 증가할수록 함량이 증가하였다. 이에 총 phenolic acid 함량 역시 원료일 때 205.74 mg/100 g에서 5분(265.34 mg/100 g), 10분(345.11 mg/100 g), 15분 볶음 처리하였을 때 388.34 mg/100 g으로 증가하였다. Flavonols 화합물 중 epigallocatechin의 함량이 높게 나타났으며, 원료일 때 110.17 mg/100 g, 5분일 때 204.00 mg/100 g, 10분일 때 397.13 mg/100 g, 15분일 때 408.14 mg/100 g으로 함량이 증가하였다. Quercetin 화합물은 15분 볶음 처리하였을 때 307.98 mg/100 g으로 볶음 처리 시간이 증가할수록 함량이 증가하였고, 총 flavonols 함량도 15분 볶음 처리 시 813.01 mg/100 g으로 가장 높았다. 지하부의 경우 protocatechuic acid의 함량이 볶음 시간이 증가함에 따라 각각 2.28 mg/100 g, 4.00 mg/100 g, 5.62 mg/100 g 및 6.39 mg/100 g으로 함량 또한 증가하는 것을 보였다. Ferulic acid의 함량은 원료일 때 5.09 mg/100 g에서 15분 볶았을 때 9.82 mg/100 g으로 증가하였다. 반면, t-cinnamic acid의 경우 볶음 시간이 증가할수록 원료일 때 3.42 mg/100 g에서 15분 볶았을 때 0.41 mg/100 g으로 함량이 감소하였다. 그러나, 총 phenoilc acids 함량은 원료에서 133.01 mg/100 g, 5분 볶았을 때 144.02 mg/100 g, 10분 볶았을 때 196.92 mg/100 g 및 15분 볶았을 때 206.97 mg/100 g으로 함량이 증가하였다. Flavonols 중 rutin의 함량은 새싹인삼 원료일 때 0.80 mg/100 g에서 15분 볶았을 때 5.46 mg/100 g으로 증가하였다. 또한, quercetin 함량은 53.44 mg/100 g에서 206.67 mg/100 g으로 15분 볶았을 때 볶음 처리를 하지 않았을 때보다 약 4배 높은 함량을 보였다.
Cho와 Joo(2012)는 원료에 비해 볶음 처리를 하였을 때 gallic acid와 chlorogenic acid 등의 함량이 증가한다고 하였고, 이는 볶음처리에 의해 ester 결합된 polyphenol 성분이 유리형 phenolics으로 변환되어 함량이 증가한 것으로 보고하였다. 본 연구의 결과도 볶음 시간이 증가함에 따라 함량이 증가하였고, 이에 항산화 활성이 증가될 것으로 추정된다. Choi 등(2012)은 여주를 부위별로 볶음 처리하여 phenolics 화합물을 분석하였는데, 본 연구결과와 유사하게 gallic acid와 chlorogenic acid, ferulic acid 등이 증가한다고 보고하였다. 또한 이중 gallic acid 및 기타 phenolic acid는 항산화 및 항암에 효과가 있다고 보고하였다.
새싹인삼의 볶음 처리에 따른 항산화 활성은 Fig. 4와 같았다. DPPH 라디칼 소거활성의 경우, 지상부 및 지하부 모두 볶음 시간이 증가할수록 활성이 증가하는 것으로 나타났다. 원료일 때 지상부 및 지하부 각각 47.36% 및 25.32%의 활성을 보였으며, 15분 볶음 처리하였을 때 80.05% 및 43.89%의 활성을 보였다(Fig. 4A). ABTS 라디칼 소거활성 또한 각 볶음 시간에 따라 지상부의 경우 원료일 때 54.81%, 5분 볶음 처리하였을 때 67.72%, 10분 볶았을 때 74.63% 및 15분 볶음 처리하였을 때 82.73%의 활성을 보였고, 지하부 역시 각각 30.62%, 42.78%, 51.23% 및 59.81%로 15분 볶았을 때 높은 활성을 보였다(Fig. 4B). Hydroxyl 라디칼 소거활성 또한 앞선 두 라디칼 소거활성과 동일하게 지상부 및 지하부 각각 82.81% 및 61.51%로 15분 볶음 처리하였을 때 가장 높은 활성을 보였다(Fig. 4C). FRAP 환원력은 지상부에서 원료일 때 0.724 OD593 nm로 나타났으며, 15분 볶음 처리하였을 때 1.082 OD593 nm로 나타났다. 지하부 또한 볶음 처리하였을 때 0.353 OD593 nm에서 15분 볶음 처리하였을 때 0.715 OD593 nm로 증가하였다(Fig. 4D).
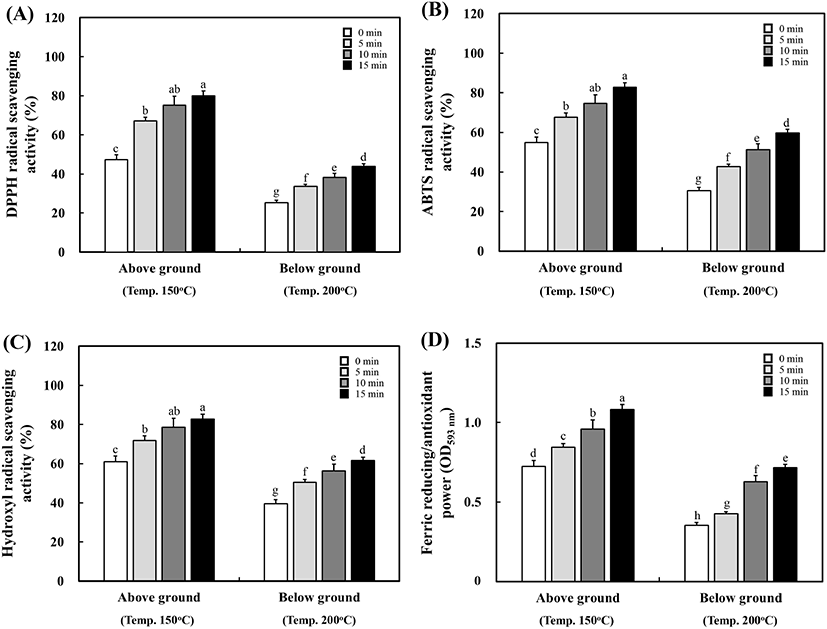
Kim 등(2018b)은 백하수오를 120°C와 180°C에서 원료 및 1-4분간 볶음 처리하여 DPPH 및 ABTS 라디칼 소거능을 비교하였다. 원료일 때 496.77 mg/mL의 IC50 값을 보였으나, 볶음처리 시간이 증가할수록 DPPH 활성이 높게 나타났다. 4분간 볶음 처리하였을 때 IC50 값이 온도별로 각각 264.05 mg/mL 및 107.25 mg/mL로 나타났다. Kwon 등(2014)은 볶음 처리에 따른 우엉차의 ABTS 라디칼 소거능을 비교하였으며 볶음 처리로 인해 75.13%의 활성에서 85.66%로 활성이 증가하였고 FRAP 환원력 역시 증가한다고 보고하였으며, 본 연구와 유사한 결과를 보고하였다. 총 phnolics 및 총 flavonoids의 함량이 볶음 처리하였을 때 증가하였으며, 이에 유사하게 항산화활성 또한 증가하는 것을 보였다. 이는 총 phenolics 및 총 flavonoids와 같은 polyphenol성 화합물이 항산화 활성에 영향을 준다고 판단된다(Kwon 등, 2014).

