Article
Rhizopus oligosporus ‘Koji’의 효소활성 및 향미성분
전성희
1
, 윤영
1, 정도연
2, 김영수
3,*
Enzyme activities and volatile compounds of Rhizopus oligosporus ‘Koji’
Sung-Hee Jeon
1
, Young Youn
1, Do-Youn Jeong
2, Young-Soo Kim
3,*
1Food Research and Development Team, Imsil Cheese and Food Research Institute, Imsil 55918, Korea
2Microbial Institute for Fermentation Industry (MIFI), Sunchang 56048, Korea
3Department of Food Science and Technology, Jeonbuk National University, Jeonju 54896, Korea
*Corresponding author. E-mail:
ykim@jbnu.ac.kr, Phone:+82-63-270-2569, Fax:+82-63-270-2572
Copyright © The Korean Society of Food Preservation. This is an Open-Access article distributed under the terms of the
Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/4.0/) which permits
unrestricted non-commercial use, distribution, and reproduction in any
medium, provided the original work is properly cited.
Received: Jan 17, 2020; Revised: Feb 10, 2020; Accepted: Feb 10, 2020
Published Online: Jun 30, 2020
요 약
본 연구에서는 R. oligosporus 코지의 제조 가능성을 확인하기 위하여 R. oligosporus의 기질에 따른 효소 활성과 향미 성분을 조사하였다. R. oligosporus의 온도와 NaCl 농도에 따른 생육환경을 조사한 결과, 빠른 생육을 하는 것을 확인하였으며, 최적온도는 30°C, NaCl의 농도는 5% 이내가 적절할 것으로 판단되나, 저온(4°C)에서도 원활한 생육이 진행되었다. 기질에 따른 생육환경은 대두 기질 또는 혼합기질에서 배양하였을 때 가장 적합하였고, 효소 활성도 측정 결과, 혼합기질에서 배양하였을 경우 가장 좋은 활성을 가졌다. 이러한 결과를 토대로 혼합기질에서의 향미 성분을 동정한 결과, isoamyl alcohol을 포함한 alcohol류를 비롯하여 ketone류, ester류, aldehyde류 및 pyrazine류 등이 검출되었다. 결과적으로 R. oligosporus는 단기발효에 적합한 생육환경과 효소 활성을 가지고 있었으며, 혼합기질을 사용한 코지에서 향미 성분 또한 다양하게 나타나, 이를 이용한 속성장 제조에 적합할 뿐만 아니라, 관능적 요인에 도움이 될 것으로 기대된다.
Abstract
This study was performed to verify the possibility of manufacturing Rhizopus oligosporus ‘Koji’, which is cultured using a range of different substrates. The growth characteristics of R. oligosporus were therefore investigated for the preparation of R. oligosporus ‘Koji’, and the optimal incubation conditions were determined to be 30 °C for 24 h, with an optimal NaCl concentration were 5%. Based on these results, R. oligosporus was incubated using three substrates, namely beans, rice and a mixture of beans and rice, for 6 d, and the enzyme activities and volatile compounds of the fermentation products were investigated. On the fourth day of incubation, the α-amylase activities of the rice and the mixed substrates were 155 and 42 unit/mL, respectively, while on the fifth day of incubation, the neutral protease activities of the beans and the mixed substrate were 14 and 15 unit/mL, respectively. In terms of the lipase activity, the mixed substrate resulted in a higher activity than the other substrates. Various volatile flavor compounds, including alcohols, ketones, esters, aldehydes, and pyrazines, were identified in R. oligosporus ‘Koji’ cultured using the mixed substrate.
Keywords: Rhizopus oligosporus; Koji; growth characteristics; enzyme activity; volatile compound
서 론
콩은 우리나라 식생활에서 중요한 식물성 단백질원으로서 두부, 콩나물, 콩밥, 두유 등으로 가공하여 섭취하거나 고추장, 된장, 간장 등과 같은 전통발효식품의 소재로 이용되어왔다. 그중 대두는 타 작물에 비하여 단백질 및 지방 함량이 높을 뿐만 아니라, isoflavone, trypsin inhibitor, saponin 등의 생리활성물질을 함유하고 있어 영양학적인 가치가 높은 것으로 알려져 있다. 일반적으로 대두에 glycosides 형태로 0.1–3.0% 함유된 isoflavone은 체내에서 aglycone으로 가수분해되면 체내 이용률이 높아져 생리활성이 더욱 증가되는 것으로 알려져 있으며(Choi 등, 1996; Izumi 등, 2000), 항암, 저밀도 지질단백질의 감소, 골다공증 예방 및 억제 등과 같은 많은 생리기능을 가지고 있는 것으로 보고되었다(Maskarinec 등, 1998; Taku 등, 2007; Sehmisch 등, 2010). 특히, 대두를 이용하여 제조한 청국장이나 된장 등의 발효식품은 발효기간 중 발효균주의 작용으로 대두 isoflavone의 체내 이용률을 높일 수 있다.
발효식품의 제조에 사용되는 균주 중 하나인 Rhizopus oligosporus(R. oligosporus)는 인도네시아의 대두 발효식품인 Tempeh의 주요 발효균주로 발효 시 대두에 함유된 isoflavone glycosides를 aglycone 형태로 분해하여 isoflavone의 체내 흡수율을 높여 생체이용률 향상에 영향을 미친다(Wang 등, 1974; Yoo 등, 2014). 또한, 발효 중 R. oligosporus에서 생성되는 lipase, protease, phytase 및 carbohydrase와 같은 다양한 효소의 활성으로 tempeh의 조직감을 높이고, riboflavin, niacin 등의 비타민과 항산화 활성을 가진 물질들을 생성하여 영양적 가치와 소화흡수율을 높인다(Roelofsen과 Talens, 1964; Liem 등, 1977; Shurtleff와 Aoyagi, 1979; Kim 등, 1990). 이는 식품으로서의 가치를 증가시킬 뿐만 아니라, 항균 활성을 갖는 화합물을 생산하여 박테리아의 성장을 억제한다고 알려진 바 있다(Wang 등, 1969). 이외에도 R. oligosporus는 발효 중 phytase를 생성하여 대두에 존재하는 phytic acid의 함량을 감소시켜 대두의 체내 이용률 향상에 도움을 준다(Sudarnadji와 Markakis, 1977; Wang 등, 1980; Fardiaz와 Markakis, 1981).
현재까지 국내에서 R. oligosporus를 이용한 연구는 캡슐형 메주의 제조 및 품질 특성에 관한 연구(Choi 등, 2002), chitosan의 생산에 관한 연구(Park과 Lee, 1997), 대두 발효물질의 대퇴골 손실 감소에 관한 연구(Yoo 등, 2014), 상업용 rennet에 관한 연구(Chen 등, 2010), 사과 탄저균에 대한 항균성에 관한 연구(Bajpai 등, 2010), 혼합곡물의 Tempeh 발효에 관한 연구(Kim 등, 1990), 발효두부의 품질 특성에 관한 연구(Lee 등, 2001), 균주를 달리하여 제조한 귤피 속성장의 특성에 관한 연구(Youn 등, 2016) 등이 있다. 그러나 이와 같은 연구는 대부분 기능성 물질이나 항균성에 관한 연구가 주를 이루고, R. oligosporus를 이용한 식품에의 적용 및 발효특성에 관한 연구는 미비한 실정이다. 따라서 본 연구에서는 여러 가지 영양학적 특성 및 다양한 효소 활성을 가지는 R. oligosporus가 속성장의 제조에 유리한 조건을 가지고 있다고 판단하였고, 이에 R. oligosporus 코지를 활용한 속성장 제조를 위한 가능성을 확인하고자 R. oligosporus의 기질에 따른 효소 활성 및 향미 성분을 분석하여 이를 이용한 속성장 제조에 적용하기 위한 기초자료로 활용하고자 하였다.
재료 및 방법
재료 및 종균
본 연구에 사용된 균주는 한국미생물보존센터에서 분양받은 Rhizopus oligosprus(R. oligosporus) KCCM 11275를 사용하였다. 대두는 태광(백태) 품종, 쌀은 신동진 품종을 대형마트에서 구입하여 사용하였다.
온도 및 NaCl 농도에 따른 균주의 생육환경 조사
R. oligosporus의 생육을 측정하기 위하여 30°C에서 전배양한 균주를 10 mL PDB(Potato dextrose broth, Difco., Detroit, MI, USA)에 1%(v/v) 접종하고 4°C와 30°C에서 배양하면서 6시간 간격으로 건조 균체량을 측정하여 균주의 생육량을 측정하였다. NaCl 농도에 따른 균주의 생육환경을 조사하기 위해 0%(w/v), 5%(w/v), 10%(w/v), 15%(w/v) 및 20%(w/v)로 NaCl(Junsei Chemical Co., Ltd., Tokyo, Japan)을 첨가한 PDB에 30°C에서 전배양한 균주를 1%(v/v) 접종한 후, 30°C에서 24시간 간격으로 건조 균체량을 측정하여 균주의 생육량을 측정하였다.
기질에 따른 미생물 배양
기질은 일반적인 코지 제조 시 이용되는 대두와 쌀을 이용하였다. 대두는 정제수로 3회 세척하여 12시간 수침한 후 121°C에서 30분간 증자하고, 쌀은 정제수로 5회 세척하여 3시간 수침한 후 1시간 동안 증자하여 사용하였다. 각각의 대두와 쌀 및 대두와 쌀을 1:1의 비율로 섞은 혼합물을 각 petri dish에 50 g씩 담고 균주 배양액을 1%(v/w) 접종하여 30°C에서 배양하며 1일 간격으로 채취하여 분석시료로 사용하였다.
효소활성 측정
조효소액은 시료 5 g에 증류수 25 mL를 넣고 진탕교반하여 추출 후 50 mL로 정용하고, 여과지(Advantec 2, Toyo Roshi Kaisha, Ltd., Tokyo, Japan)를 사용하여 여과한 다음 syringe filter(0.22 μm pore size, Futecs Co., Ltd., Daejeon, Korea)를 사용하여 재여과한 것을 조효소액으로 사용하였다.
α-Amylase 활성 측정을 위해서 1% 전분용액과 조효소액 1 mL를 20°C에서 3분간 반응시킨 후 3,5-dinitrosalicylic acid 1 mL를 넣고 95°C 이상의 항온수조에서 15분간 반응시켰다. 이후 실온으로 냉각하고 증류수를 혼합한 후 540 nm에서 흡광도를 측정하였다. 조효소액 1 mL에 의해 분해되는 전분의 mg 수를 효소 활성단위 1 unit으로 하여 시료 1 mL당 환산하여 표시하였으며, 표준곡선은 maltose를 이용하였다(Bernfeld, 1955).
Protease 활성 측정을 위해서 pH 7로 조정한 0.6% casein 용액 5 mL에 조효소액 1 mL를 혼합하여 30°C에서 10분간 반응시켰다. 이후 0.4 M trichloracetic acid 5 mL를 혼합하고 30°C에서 30분간 반응시킨 다음 여과하였다. 여액 2 mL에 0.4 M sodium carbonate 5 mL와 Folin reagent 용액 1 mL를 혼합하여 30°C에서 30분간 발색한 후 660 nm에서 흡광도를 측정하였다. 조효소액 1 mL에서 1분간 1 μg의 tyrosine을 유리할 때 1 unit로 하여 시료 1 mL당 환산하여 표시하였으며, 표준곡선은 L-tyrosine을 이용하여 작성하였다(Jung 등, 2012).
Lipase 활성 측정을 위해서 대두유와 염을 첨가한 50 mM phosphate buffer(pH 6.0) 0.9 mL에 0.1 mL의 조효소액을 혼합한 후 30°C에서 1시간 동안 반응시켰다. 이후 Copper regent 2 mL와 extraction solvent 6 mL를 혼합하여 30분간 진탕 교반하였다. 반응액을 12,000 ×g에서 원심분리하여 상등액 3 mL에 colour regent 0.25 mL를 혼합하여 발색시킨 후 440 nm에서 흡광도를 측정하였다. 1분당 1 μmole의 지방산 생성량을 시료 1 mL당 1 unit로 환산하여 표시하였으며, 표준곡선은 linoleic acid를 이용하여 나타내었다(Kim 등, 1984).
기질별 휘발성 향미 성분 분석
향미 성분의 포집을 위하여 AQ-200 liquid sampler(Japan Analytical Industry, Tokyo, Japan)를 사용하였다. 시료관의 온도는 40°C로 설정하였고, 시료를 50 mL/min로 bubbling하여 Tenax GR 흡착관(Japan Analytical Industry, Tokyo, Japan)에 30분간 흡착시켰다. 흡착된 시료는 Purge & Trap sampler(JTD-505Ⅲ, Japan Analytical Industry, Tokyo, Japan)-GC/MS QP 2010 plus(Shimadzu, Kyoto, Japan)를 사용하여 분석하였다. 흡착된 시료를 탈착(280°C, 30분)시킴과 동시에 Curio pointer(–40°C)에서 재흡착하였고, 재흡착이 끝난 후 280°C로 pyrolysis시켜 시료를 컬럼에 주입하였다. 그 외 Transfer-line temperature 280°C, needle heater 200°C, cold-trap heater 86 MPa, head press 1.0 mL/min, column flow 1/100, split ratio의 조건으로 분석하였다. 시료는 GC/MS QP 2010 plus(Shimadzu, Kyoto, Japan)를 사용하여 분석하였고, 컬럼은 DB-624 column(30 m×0.251 mm×1.40 mm; Agilent Technologies, Wilmington, DE, USA)를 사용하였다. Oven temperature program은 40°C for 3 min hold, 10 mL/min up to 260°C, 5 min hold의 조건으로 분석하였다. 질량분석기의 ion source 온도는 200°C, transfer line은 250°C, 그리고 EM voltage는 70 eV를 사용하였다. Database는 NIST database(Wiley 9.1 Version)를 이용하여 정성분석하였다(Youn 등, 2016).
통계처리
실험은 3회 이상 반복 실시하여 평균(mean)±표준편차(standard deviation, SD)로 나타내었고, 시료 간 차이는 SPSS package program(Ver. 12.0K, SPSS Inc., Chicago, IL, USA)를 이용하여 p<0.05 수준에서 one-way ANOVA 분석을 하였고, Ducan’s multiple range test로 그 유의성을 검증하였다.
결과 및 고찰
온도 및 NaCl 농도에 따른 균주의 생육 환경
속성장은 대개 1개월 이내의 발효를 통해 제조되며, NaCl 함량이 낮은 특징을 가진다(Youn 등, 2016). 이러한 낮은 NaCl의 함량은 건강을 생각하는 현대인들의 입맛에 부합하는 부분이나, 낮은 식염 함량은 속성장의 저장성에 영향을 준다. 이에 본 연구에서는 R. oligosporus의 온도에 따른 균주 활성을 측정하여 속성장 제조 시 발효온도 설정에 적용하고자 하였다. 이와 함께 속성장 제조 시 첨가되는 최적 NaCl의 농도를 정하고자 NaCl의 농도에 따른 균주의 생육 영향성을 확인하고자 하였다.
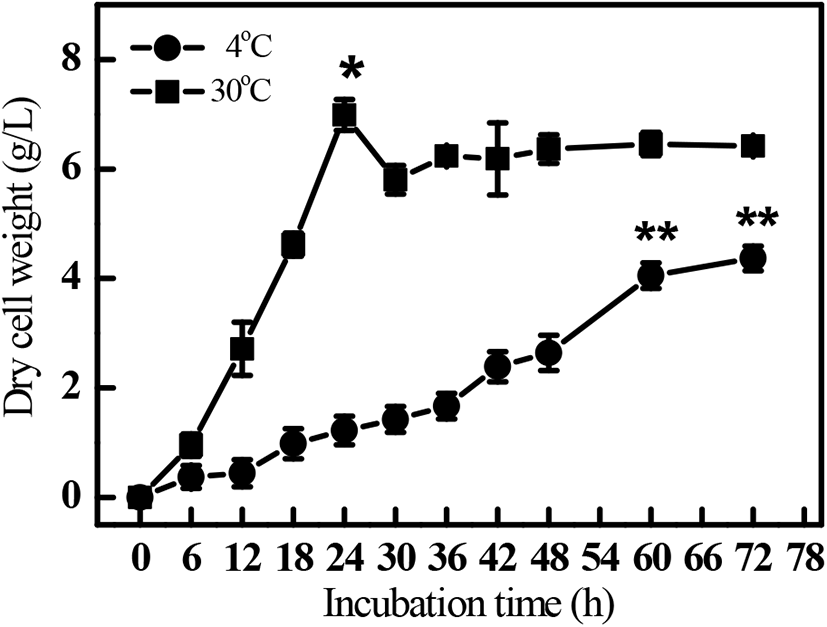
R. oligosporus의 생육에 대한 배양온도의 영향을 조사하기 위하여 4°C 및 30°C에서 배양한 결과(Fig. 1), 각각의 배양온도에서 배양시간에 따라 균체의 생육이 증가하였다. 배양온도 30°C의 경우, 배양 24시간까지 급격히 증가하여 유의적으로 높은 생육을 나타내었으나, 배양온도 4°C의 경우에는 48시간까지는 점진적으로 증가하였고, 그 이후에는 급격하게 증가하여 72시간에서 높은 생육을 나타내었다. 따라서 R. oligosporus의 배양온도는 30°C가 적절하다고 판단되나, 저온에서도 배양시간에 차이가 있을 뿐 생육에는 큰 영향을 주지 않았다. 이 결과는 한국 전통발효식품에 주로 사용되는 A. oryzae의 경우에 25°C에서 배양 72시간째 0.5 g/200 mL 생장하였다고 보고한 연구(Na, 1995)와 비교할 때, R. oligosporus의 생장 속도가 빠르며, 생육온도의 범위 또한 더 넓어 R. oligosporus 코지를 이용할 경우 속성장을 제조하는데 매우 적합할 것이라 판단된다.
Fig. 1.
The growth curve of R. oligosporus ‘Koji’ on different temperatures.
*,**p<0.05 versus 6 h of each microorganisms.
Download Original Figure
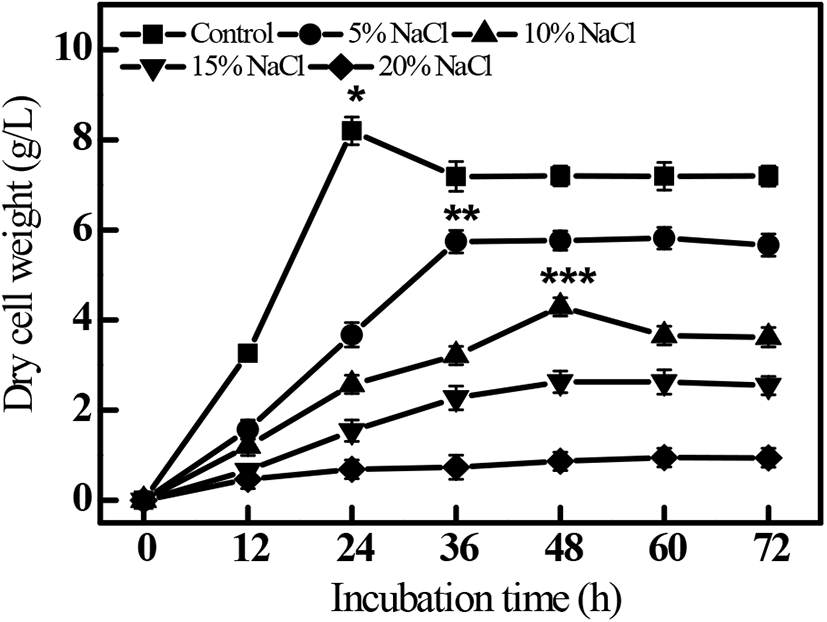
R. oligosporus의 생육에 대한 배양환경 내 NaCl 농도의 영향을 조사하기 위하여 0–20%(w/v) NaCl을 첨가하여 30°C에서 배양한 결과는 Fig. 2와 같다. 0% NaCl에서 배양된 R. oligosporus는 배양 24시간까지 급격하게 증가하여 최대 균체를 생성하였으나, 그 이후에는 배양시간에 따른 증가는 나타나지 않았다. 5% 및 10% NaCl에서 배양된 R. oligosporus는 각각 배양 36시간과 48시간까지 유의적으로 증가하였고, 그 이후에는 유의적인 차이를 나타내지 않았다. 또한, 15% NaCl에서 배양된 R. oligosporus는 미약하게나마 증가하는 경향을 보인 반면, 20% NaCl에서 배양된 R. oligosporus는 72시간 동안 균의 증식이 일어나지 않았다. 결과적으로 R. oligosporus는 NaCl의 농도에 따라 균주의 생육 최대치 및 배양시간이 다르게 나타났으며, NaCl 농도 0–20%까지 생육이 가능하였으나, 15%와 20%에서는 생육이 느리게 진행되었다. 이는 NaCl의 농도가 균의 생육에 중요한 요인으로 작용하기 때문에 R. oligosporus를 이용하여 속성장을 제조할 경우, NaCl 첨가량에 따라 균의 생육이 저해 받을 수 있을 것이라 판단된다. 따라서 R. oligosporus의 배양 시 NaCl의 농도가 생육에 영향을 미치기 때문에 최적 NaCl의 농도를 5% 이내로 하는 것이 적절할 것으로 판단된다.
Fig. 2.
The growth curve of R. oligosporus ‘Koji’ on different NaCl concentrations.
*,**,***p<0.05 versus 12 h of each microorganisms.
Download Original Figure
기질에 대한 생육 환경 및 효소 활성
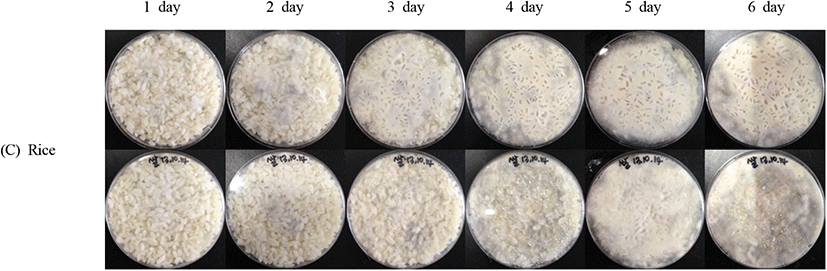
기질에 대한 R. oligosporus의 생육 적합성을 확인하기 위하여 기질로 사용할 대두, 혼합물(대두+쌀) 및 쌀에 R. oligosporus를 접종시킨 후 30°C에서 6일 동안 배양하여 균의 생육 정도를 확인하였다(Fig. 3). 대두를 기질로 하여 배양한 R. oligosporus는 배양 3일째 균의 균사가 대두의 표면을 완전히 감싸 생육이 잘 되었음을 확인하였으며, 이때 plate 내의 냄새는 상큼한 향을 내었다. 혼합물의 경우, 배양 4일째에 plate 내의 균사가 잘 뻗어있는 것을 확인하였으나, 이와 함께 쿰쿰한 냄새를 발생하여 불쾌취를 나타내었다. 쌀을 기질로 배양한 경우에는 배양 4일째 배양이 잘 이루어졌으나, 이후 배양시간이 증가함에 따라 기질 표면의 수분이 감소하여 R. oligosporus의 생육에 영향을 미치는 것으로 판단되었다. 결과적으로 R. oligosporus의 최적 기질로 대두와 혼합물이 생육에 우수하여 코지 제조에 적합할 것으로 보이며, 쌀 기질을 이용할 경우 배양시간이나 배양방법의 변형이 필요할 것으로 판단된다.
Fig. 3.
The growth effect of R. oligosporus ‘Koji’ on three types of substrates.
R. oligosporus were cultured by substrates of three types at 30°C for 6 days.
(A), cultured R. oligosporus in beans; (B), cultured R. oligosporus in mixed substrates [bean+rice, 1:1(w/w)]; (C), cultured R. oligosporus in rice.
Download Original Figure
Download Original Figure
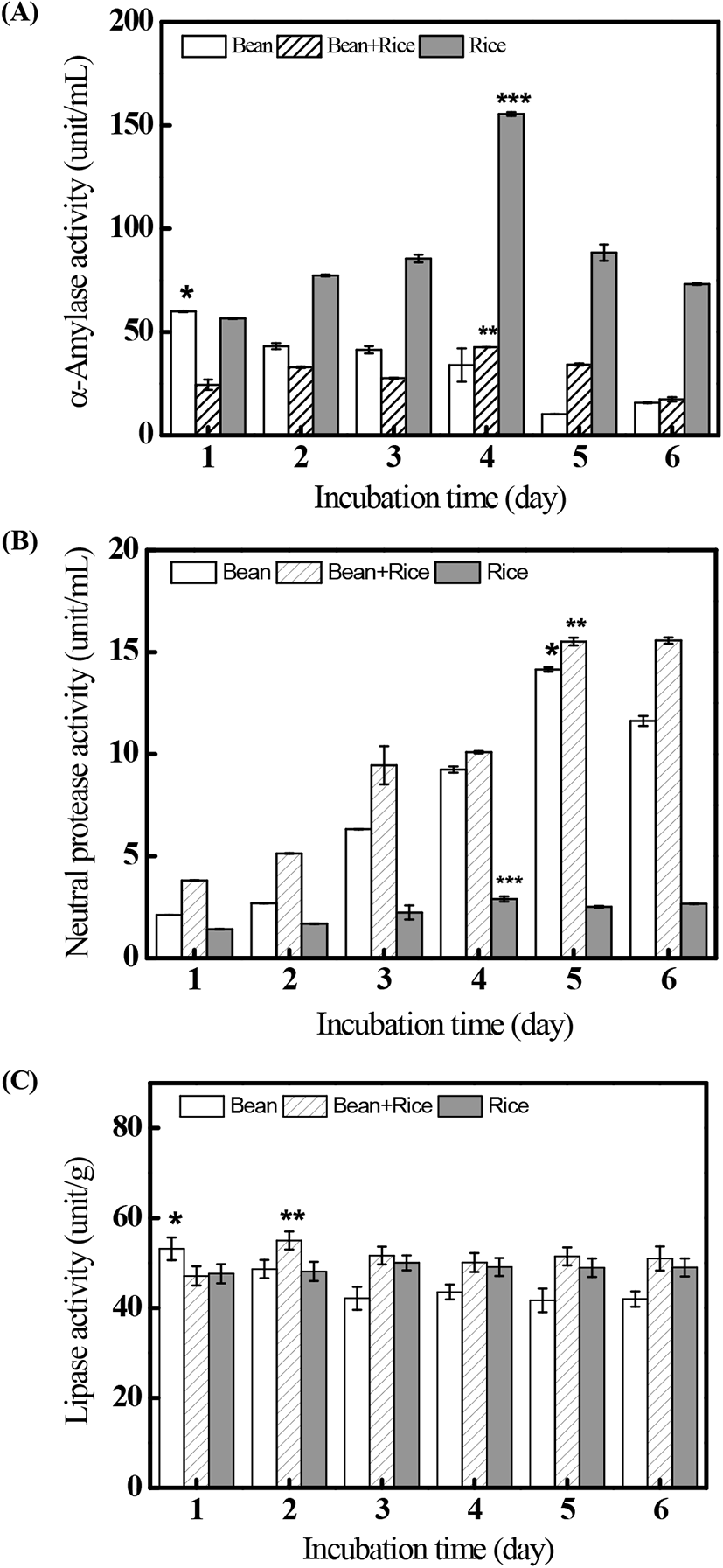
대두, 혼합물(대두+쌀) 및 쌀에서 배양하여 추출한 R. oligosporus의 조효소액의 α-amylase 활성도를 측정한 결과는 Fig. 4와 같다. 대두에서 배양된 R. oligosporus의 α-amylase의 활성도(Fig. 4A)는 배양 1일째 59 unit/mL로 배양기간 동안 유의적으로 높은 활성을 나타냈지만, 혼합물의 경우 배양 4일째 42 unit/mL로 유의적으로 높은 활성을 나타내었다. 특히, 쌀에서 배양된 경우, 다른 기질보다 상대적으로 높은 활성을 나타내었으며, 배양 4일째에 155 unit/mL로 유의적으로 가장 높은 활성을 나타내었다. 이는 쌀이 다른 기질에 비해 상대적으로 많은 양의 전분질을 함유하여 α-amylase의 생성이 많았기 때문으로 추정된다. 결과적으로 R. oligosporus의 α-amylase 활성은 쌀을 기질로 사용할 경우, 다른 기질보다 상대적으로 높은 α-amylase의 활성을 나타내었다.
Fig. 4.
The enzyme activities of R. oligosporus ‘Koji’ on three types of substrates concentrations.
(A) is the alpha amylase activity of R. oligosporus in each substrates, (B) is neutral protease activity of R. oligosporus in each substrates, (C) is lipase activity of R. oligosporus in each substrates.
*,**,***p<0.05 versus 1 day of each substrates.
Download Original Figure
대두, 혼합물(대두+쌀) 및 쌀에서 배양하여 추출한 R. oligosporus의 조효소액의 protease 활성도를 측정한 결과(Fig. 4B), 대두에서 배양한 경우 배양 5일째 약 14 unit/mL로 유의적으로 높은 활성을 나타내었으며, 혼합물 또한 배양 5일째 약 15 unit/mL로 높은 활성을 나타내었다. 그러나 쌀에서 배양한 경우 약 1–3 unit/mL로 활성이 매우 낮게 나타났다. 이는 배양에 사용된 대두의 단백질 함량이 다른 기질에 비해 상대적으로 풍부하여 protease의 생성이 높았기 때문으로 판단된다. 특히, 혼합물의 경우, 혼합물 내의 서로 작용하는 효소들에 의해 R. oligosporus가 이용하기 쉽도록 분해되어 단일 기질을 이용하였을 때보다 효소의 생성량이 많은 것으로 추정된다.
대두, 혼합물(대두+쌀) 및 쌀에서 배양하여 추출한 R. oligosporus의 조효소액의 lipase 활성도를 측정한 결과(Fig. 4C), 대두에서 배양된 경우, 배양 1일째 약 53 unit/mL로 배양기간 동안 유의적으로 높은 활성을 나타낸 반면, 혼합물에서 배양된 경우 배양 2일째 약 55 unit/mL로 유의적으로 높은 활성을 나타내었다. 또한, 쌀에서 배양된 경우, 배양 3일째 약 50 unit/mL로 배양 3일째 유의적으로 높은 활성을 나타내었다. 특히, 대두가 포함된 기질(대두 및 혼합물)에서 배양한 R. oligosporus가 높은 lipase의 활성을 나타내었다. 이는 Wang 등(1980)이 대두에서 배양된 lipase 활성(37°C, 26시간)이 25.4 unit의 활성을 갖는다고 보고한 결과와 비교하여 수행한 세 가지 기질 모두에서 높은 활성을 갖는 것으로 나타났다. 따라서 효소 활성의 결과를 토대로 R. oligosporus 코지 제조를 위하여 기질을 선택할 경우, 혼합물을 사용한다면 우수한 효소 활성을 가질 것으로 추정된다.
향미 성분 분석
R. oligosporus의 생육특성 조사결과, 배양 후 72시간째 가장 왕성한 활성이 나타났으며, 기질에 따른 효소 활성을 비교한 결과, R. oligosprus의 기질로 혼합물을 사용하였을 때 가장 우수한 활성을 가지는 것으로 확인되었다. 이러한 결과를 토대로 R. oligosprus를 혼합기질에 접종한 후 30°C에서 3일간 배양하여 휘발성 향미 성분을 확인한 결과는 Table 1과 같다. 혼합기질에서 동정된 향기성분은 총 40여개로 isoamyl alcohol 등을 포함한 alcohol류가 9가지, ketone류가 13가지, ester류 5가지, aldehyde류 6가지, pyrazine류 4가지 및 기타 3가지가 확인되었다. 주로 과일과 꽃의 향을 내는 isoamyl alcohol과 1-propanol, ethyl acetate 등이 검출되어, 생육 적합성을 위한 배양 시 발생하는 냄새와 대부분 일치하였다. 이 중 46.08%의 높은 면적을 차지하는 isoamyl alcohol은 퓨젤유 성분으로 바나나향을 내는 것으로 알려져 있으며(Choi와 Lee, 2003), 이러한 퓨젤유 성분은 미량만으로도 풍미에 크게 영향을 미친다(Lee 등, 2014). 그 다음으로는 22.2%의 함량을 가진 ethyl alcohol이 검출되어 두 번째로 넓은 면적을 차지하였으나, 실질적으로 발현되는 향의 기여도는 ester류와 aldehyde류보다 낮아 향의 강도가 세지 않았다. Ester류 중 가장 넓은 면적을 차지한 ethyl acetate는 과일 에센스, 과즙, 주류, 과자 등의 향료로 널리 이용되는 과실향으로 알려져 있으며, 맥주의 주요 ester 성분으로 달콤하고 신선한 배향의 특성을 가진 isoamyl acetate는 좋은 향을 내는 것으로 보고된 바 있다(Steffen, 1969; Yuda, 1976).
Table 1.
Volatile compounds from R. oligosporus ‘Koji’ cultured in mixed substratea
|
Compounds |
Peak area (%) |
|
Mixed (bean+rice) |
|
Esters |
|
Ethyl acetate |
3.14 |
|
Propanoic acid, ethyl ester |
0.44 |
|
Butanoic acid, 2-methyl-, ethyl ester |
0.77 |
|
Butanoic acid, 3-methyl-, ethyl ester |
0.45 |
|
Isoamyl acetate |
0.23 |
|
Aldehydes |
|
Acetaldehyde |
0.23 |
|
Isobutyraldehyde |
0.19 |
|
3-Methylbutanal |
0.81 |
|
Crotonaldehyde |
0.81 |
|
2-Methyl-2-butenal |
0.39 |
|
Heptaaldehyde |
0.42 |
|
Ketones |
|
2-Propane |
1.55 |
|
2,3-Butanedion |
1.58 |
|
Methyl ethyl ketone |
3.07 |
|
Pentaborane |
0.16 |
|
Methyl propyl ketone |
0.62 |
|
3-Methyl-2-pentanone |
0.11 |
|
3-Hexanone |
0.16 |
|
2-Hexanone |
0.28 |
|
3-Heptanone |
0.44 |
|
2-Heptanone |
0.36 |
|
5-Methyl-2-heptanone |
0.12 |
|
3-Octanone |
0.27 |
|
2-Octane |
0.15 |
|
Alcohols |
|
Ethyl alcohol |
22.2 |
|
1-Propanol |
1.50 |
|
2-Butanol |
1.13 |
|
Isobutyl alcohol |
7.87 |
|
1-Butanol |
1.55 |
|
3-Methyl-2-butanol |
0.10 |
|
Isoamyl alcohol |
46.08 |
|
Dipheyl tetrahydro eriostanol |
0.17 |
|
1-Hexanol |
0.11 |
|
Pyrazines |
|
2,5-Dimethylpyrazine |
0.16 |
|
Trimethylpyrazine |
0.42 |
|
3-Ethyl-2,5-dimethylpyrazine |
0.32 |
|
Tetramethylpyrazine |
0.72 |
|
Others |
|
Methyl propyl ether |
0.17 |
|
Methyl cyanide |
0.16 |
|
9-Borabicyclo[3,3,1]nonane,9-ethyl |
0.56 |
|
Total |
100 |
Download Excel Table
기존의 연구(Youn 등, 2016)에서 Aspergillus oryzae 코지를 사용하여 제조한 속성장에서는 주로 hydrocarbon류, alcohol류, ketone류 등의 성분들이 검출되었지만, R. oligosporus 코지를 사용할 경우 alcohol류 및 ketone류가 주로 검출되었고 또한, A. oryzae 코지를 사용한 속성장에 비해 검출된 성분이 적다고 보고된 바 있다. 특히, 된장의 주요 향기성분 중 쿰쿰한 불쾌취와 고린 향의 냄새성분으로 알려진 butanoic acid와 benzenacetaldehyde 등이 R. oligosporus를 사용한 혼합기질에서는 검출되지 않아 이를 활용한 속성장에서는 일반적인 된장의 향미 성분과 다를 것으로 생각된다.
결과적으로 R. oligosporus를 단기발효 균주로 활용할 시 발효 기간이 짧음에도 충분한 향미와 활성을 가지고 있음을 알 수 있었고, 이를 이용한 코지 제조 시 속성장 발효에 적합할 것이라 판단된다.
감사의 글
본 연구는 (재)발효미생물산업진흥원 지역 농식품선도클러스터 육성사업(제목: 동부권 연계 제품개발(쌈장, 토마토된장 및 고추장 관련 응용제품)에 의해 수행되었으며, 이에 감사드립니다.
References
Bajpai VK, Choi SW, Kang SC. Antifungal properties of
Rhizopus oligosporus against apple anthracnose fungi. Korean J Environ Agric, 29, 86-91 (2010)


Bernfeld P. Amylases α and β. In: Methods, Enzymol, Academic Press, Cambridge, MA, USA, p 149-158 (1955)


Chen MT, Lu YY, Weng TM. Comparison of milk-clotting activity of proteinase produced by
Bacillus subtilis var.
natto and
Rhizopus oligosporus with commercial rennet. Asian-Aust J Anim Sci, 23, 1369-1379 (2010)


Choi JH, Kim MH, Shon MY, Park SK, Choi SD, U H. Production and quality properties of capsule type
Meju prepared with
Rhizopus oligosporus. Korean J Food Preserv, 9, 315-320 (2002)

Choi JS, Kwon TW, Kim JS. Isoflavone contents in some varieties of soybean. Food Sci Biotechnol, 5, 167-169 (1996)

Choi JY, Lee TS. Characteristics of volatile flavor compounds in
Kochujang prepared with commercial enzyme during fermentations. J Korean Soc Agric Chem Biotechnol, 46, 207-213 (2003)

Fardiaz D, Markakis P. Degradation of phytic acid in oncom (fermented peanut press cake). J Food Sci, 46, 523-525 (1981)

,


Izumi T, Piskula MK, Osawa S, Obata A, Tobe K, Saito M, Kataoka S, Kubota Y, Kikuchi M. Soy isoflavone aglycones are absorbed faster and in higher amounts than their glucosides in humans. J Nutr, 130, 1695-1699 (2000)

,


Jung JB, Choi SK, Jeong DY, Kim YS, Kim YS. Effects of germination time of soybean on quality characteristics of
Cheonggukjang fermented with an isolated bacterial strain. Korean J Food Sci Technol, 44, 69-75 (2012)


Kim CJ, Cheigh HS, Byun SM. A simple and modified photometric method for measuring lipase activity. Korean J Food Sci Technol, 16, 251-253 (1984)

Kim CT, Kim CJ, Kim DC, Kwon TW. Tempeh fermentation from a mixture of soybean and sorghum grain. Korean J Food Sci Technol, 22, 668-674 (1990)

Lee DH, Lee YS, Cho CH, Park IT, Kim JH, Ahn BH. The qualities of liquor distilled from
Ipkuk (koji) or
Nuruk under reduced or atmospheric pressure. Korean J Food Sci Technol, 46, 25-32 (2014)


Lee SH, Kim YT, Son MY, Sung CK, Park SK. Quality properties of fermented tofu prepared with different molds and coagulants. J Korean Soc Food Sci Nutr, 30, 617-622 (2001)

Liem IT, Steinkeraus KH, Cronk TC. Production of vitamin B-12 in tempeh, a fermented soybean food. Appl Environ Microbiol, 34, 773-776 (1977)


Maskarinec G, Singh S, Meng L, Franke AA. Dietary soy intake and urinary isoflavone excretion among women from a multiethnic population. Cancer Epidemiol Biomarkers Prev, 7, 613-619 (1998)

Na HJ. Effect of
Artemisia asiatica Nakai extract on the growth and enzyme activity of
Aspergillus oryzae. MS Thesis, Kon-kuk University, Korea, p 9-14 (1995)

Park HK, Lee KH. Production of the microbial chitosan from
Rhizopus oligosporus ATCC 22959. Korean J Food Nutr, 10, 491-496 (1997)

Roelofsen PA, Talens A. Changes in some B vitamins during molding of soybeans by
Rhizopus oryzae in the production of tempeh kedelee. J Food Sci, 29, 224-226 (1964)


Sehmisch S, Uffenorde J, Maehlmeyer S, Tezval M, Jarry H, Stuermer KM, Sutermer EK. Evaluation of bone quality and quantity in osteoporotic mice - The effects of genistein and equol. Phytomedicine, 17, 424-430 (2010)

,


Shurtleff W, Aoyagi A. The Book of Tempeh. 2nd ed, Ten Speed Press. California, MO, USA, p 34-36 (1979)

So MH, Lee YS, Han SH, Noh WS. Analysis of major flavor compounds in Takju mash brewed with a modified Nuruk. Korean J Food Nutr, 12, 421-426 (1999)

Steffen A. Perfume and Flavor Chemicals: Aroma Chemicals. Newark NJ (Consultant), Allured Publishing Corp, Carol Stream, IL, USA, p 60-61 (1969)

Sudarnadji S, Markakis P. The phytate and phytase of soybean tempeh. J Sci Food Agric, 28, 381-383 (1977)


Taku K, Umegaki K, Sato Y, Taki Y, Endoh K, Watanabe S. Soy isoflavones lower serum total and LDL cholesterol in humans: A meta-analysis of 11 randomized controlled trials. Am J Clin Nutr, 85, 1148-1156 (2007)

,


Wang HL, Ruttle DI, Hesseltine CW. Antibacterial compound from a soybean product fermented by
Rhizopus oligosporus. Proc Soc Exp Biol Med, 131, 579-583 (1969)

,


Wang HL, Swain EW, Hesseltine CW. Phytase of molds used in oriental food fermentation. J Food Sci, 45, 1262-1266 (1980)


Wang HL, Vespa JB, Hesseltine CW. Acid protease production by fungi used in soybean food fermentation. Appl Environ Microbiol, 27, 906-911 (1974)


Yoo HW, Chang MJ, Kim SH. Fermented soybeans by
Rhizopus oligosporus reduce femoral bone loss in ovariectomized rats. Nutr Res Pract, 8, 539-543 (2014)

,

,


Youn Y, Jeon SH, Yoo JH, Jeong DY, Kim YS. Quality characteristics of tangerine peel
Soksungjang prepared from different Koji strains. Korean J Food Preserv, 23, 117-126 (2016)


Yuda J. Volatile compounds from beer fermentation. J Soc Brew Jpn, 71, 819-830 (1976)