서 론
인류가 농경을 시작하면서 각 문명은 자연스럽게 그 지 역에서 얻기 쉬운 농작물로 술을 만들기 시작하였다. 메소 포타미아와 이집트에서는 보리를 싹 틔워 쓰거나 포도, 사 과 등을 이용하였고 잉카는 옥수수나 사탕수수를 사용하였 다(1). 반면 한국, 중국, 일본, 인도네시아, 인도, 네팔 등 아시아권에서는 쌀과 잡곡에 누룩을 첨가하는 양조법으로 발전되어 왔다(2). 발효주에 증류기술이 적용되면서 위스 키, 브랜디, 꼬냑, 럼, 보드카 등의 다양한 증류주가 만들어 지기 시작하였고 우리나라와 중국, 일본은 각각 소주(燒酒), 백주(白酒, báijiǔ), 쇼추(燒酎, shochu)로 분류하였으며(2) 현재까지도 널리 음용되고 있다.
우리나라의 주류시장에서 소주가 차지하는 비중은 2015 년 출고금액기준, 희석식 소주가 3조 4,666억 원으로 전체 주류의 37%를 차지하고 있으나 증류식 소주는 195억 원으 로 0.21%에 불과하다(3). 우리나라에서 증류식 소주가 쇠퇴 한 이유는 일제강점기 시대 주세법에 따른 다양성의 축소와 한국전쟁으로 경제가 어려워지면서 값싼 술을 찾을 수밖에 없었던 역사적 배경을 들 수 있다. 이외에 쌀을 주류제조에 사용하지 못하게 하는 양곡관리법 등의 조치가 이어지면서 1976년 증류식 소주 제조장은 국내에서 완전히 사라지게 되고 희석식 소주는 꾸준히 성장하게 된다(4). 이후 1990년 쌀 사용이 허용되면서 증류식 소주도 다시 생산되기 시작하 였고 2015년 국내에 55개 제조장이 운영 중이다(4,5).
그러나 제품경쟁력이 외국산 증류주에 밀리면서 2015년 31,402 kL(2,683억원)의 증류주가 수입되었다(6). 2015년 국내 증류식 소주 생산량이 954 kL(6)이므로 국내생산량의 33배가량이 수입되었다. 주류의 수입은 단순히 무역수지 악화로 끝나는 문제가 아니라 주류를 만드는 농산물을 포함 한 일자리 및 문화 등이 국내에 유입되는 의미도 가지고 있다. 1 L의 위스키를 생산하는데 약 1.13 kg의 곡물이 사용 되므로(7) 2015년 수입된 16,963 kL(6)의 위스키는 술과 더불어 2만톤의 보리가 국내로 유입된 것이다.
이러한 문제를 극복하기 위해서는 다양한 노력이 필요하 겠지만 품질경쟁력 확보가 시급한 문제로 판단된다. 증류 주 제조에 필요한 기술은 원료처리, 누룩제조, 발효, 증류, 숙성, 폐수처리 및 기계설비 제작기술 등을 꼽을 수 있다. 현재까지의 연구를 살펴보면, 원료영역에 있어서는 쌀(8), 고구마(9), 감자(10), 잡곡(11) 등이 소재로 이용되었고, 누 룩제조 분야에서는 누룩 미생물의 분포 및 특성(12-14), 제 조법 최적화(15) 등의 연구가 있고, 발효기술연구로는 누룩 과 국균의 종류에 따른 특성의 변화(16,17), 가수량(18), 미 생물 혼합배양(19), 유기산 첨가(20) 등이 시도되었다. 증류 분야에서는 유기산 에스테르화(21) 및 증류방법에 따른 품 질변화 조사(22) 등이 있으며 숙성, 폐수처리, 기계설비에 대한 연구는 찾아보기 어려운 실정이다. 증류식 소주의 품 질을 높이기 위해서는 보다 근본적이고 제조현장에 부합한 체계적인 연구가 시급하다.
우리나라와 일본의 증류식 소주는 산 생성이 높은 백국 균(Aspergillus luchuensis)을 사용하기 때문에(23) 산도가 높은 환경에서 안정적인 발효를 할 수 있는 효모가 필요하 다. 그러나 국내에서는 증류식 소주용 효모가 판매되고 있 지 않기 때문에 많은 양조장에서 막걸리용 효모나 수입 빵효모를 사용하고 있는 실정이다. 본 연구팀은 국내 10개 지역에서 수집한 누룩으로부터 내산성이 높은 효모 2종을 분리하였고(24,25) 증류식 소주 제조특성에 대하여 조사하 였기에 보고하는 바이다.
재료 및 방법
효모는 재래누룩에서 분리한 N4(KACC93224P), N9 (KACC93234P) 및 국내 증류식 소주 양조장에서 사용되고 있는 효모를 사용하였다. 건조효모는 ㈜충무발효(Ulsan, Korea)에서 생산하고 있는 충무 종효모(CM)와 빵효모(La Parisienne, S.I. Leasaffre Co., Marcq-en-Baroeul, France; LP) 를 구매한 후 순수 분리한 다음 사용하였다. 대조구로는 일본의 증류식 소주용 효모 C4(26)를 사용하였다. 종국은 ㈜충무발효의 백국을 사용하였다. 쌀은 한아름 품종을 시중 에서 구입하여 이용하였다.
전배양은 YPD 배지(Difco-BD, Sparks, MD, USA)에서 수행하였다. 삼각플라스크에 배지 10 mL를 분주하고 1백 금이를 접종한 뒤 30℃, 150 rpm에서 24시간 배양하였다.
쌀 3 kg을 세척시간을 합쳐 60분간 수침하고 60분간 물빼 기 한 뒤 60분간 증자하였다. 증자미를 40℃까지 냉각시키 고 종국 0.3 g을 접종한 다음 제국기(Mini-15, Yaegaki Food Co., Hyogo, Japan)에서 43시간동안 배양시켰다. 배양시간 19, 24, 28시간째 뒤집기를 하여 외부의 공기를 주입시키고 곰팡이가 고루 자라도록 하였으며 품온은 38℃로 유지시켰 다. 배양 28시간 이후에는 품온을 35℃로 낮추어 산 생성이 증가되도록 하고(27) 배양 43시간 째 회수하여 -20℃에 보 관하면서 사용하였다.
밑술은 물 480 mL에 효모 전배양액 8.8 mL를 넣은 다음 입국 400 g을 첨가하고 30℃ 수욕 상에서 5일간 발효하여 제조하였다. 본 발효는 밑술에 백미 800 g 상당량의 증자미 와 물 1,920 mL를 첨가한 다음 30℃ 수욕 상에서 발효시켰 다. 발효기간은 전날과의 무게 차이가 0.5 g이하로 될 때까 지 하였다. 이때 첨가된 입국과 백미의 무게는 수분 12.5% 일 때의 무게로 제국 및 증자과정에서 흡수되는 수분량은 첨가되는 물 양에서 제외하였다. 전체적으로는 입국사용량 은 전분질 원료의 1/3, 급수비율은 160% 모델을 사용하였 다. 발효경과는 매일 무게를 측정하여 그 변화량으로 산출 하였다.
증류는 상압증류를 수행하였다. 술덧 700 g을 유리용기 에 넣고 스팀발생기에서 생성된 증기가 술덧에 직접 주입 되도록 제작된 기구를 이용하였다(28). 증류 종말점은 받아 진 증류액(원주)의 알코올 농도가 41%가 될 때로 하였다.
수분은 적외선 수분측정기(MX-50, A&D Co., Ltd., Tokyo, Japan)를 사용하였으며 조지방, 조단백질, 조회분 및 탄수화물 함량은 식품공전(29)에 준하여 실시하였다.
한아름 품종 백미 50 g을 밖으로 이탈되지 않도록 거즈로 잘 감싸고 증류수가 담겨있는 250 mL 비이커에 수침시킨 다음 10분 단위로 꺼내 세게 흔들어 쌀에 붙어 있는 수분을 잘 제거한 다음 무게를 측정하였다. 수분흡수율은 원료에 대한 무게 증가율로 나타내었다. 이때 물 양은 쌀이 충분히 잠길 만큼 조절하여 실시하였다.
산도 측정을 위해 입국 20 g에 물 100 mL를 첨가하고 20℃에서 3시간 추출하였다. 추출물을 여과(Filter paper No. 2, Whatman International Ltd., Maidstone, England)한 뒤 10 mL를 취해 0.1 N NaOH로 적정하고 그 mL수를 산도로 표시하였다. 효소활성 측정을 위한 조효소액은 입국 20 g에 0.5% NaCl함유 10 mM acetate buffer(pH 5.0) 100 mL로 추출한 뒤 여과하여 제조하였다. 추출조건과 여과조건은 산도측정용 시료 제작과 동일하게 하였다. 당화력, α -amylase, gluco-amylase, α-glucosidase 및acidic carboxypeptidase 는 양조용 효소 측정 kit(Kikkoman Co., Tokyo, Japan)를 사용하였다.
당화력은 기질인 4-nitro-phenyl-β-maltoside(G2-β-PNP) 를 4-nitro-phenyl-β-glucoside(G1-β-PNP)로 분해시키는 활 성으로 구하였다. 기질에 조효소액을 반응시킨 후 분해된 G1-β-PNP에 β-glucosidase를 작용시켜 유리된 4-nitrophenol (PNP)를 440 nm에 측정한 후 제조사가 제시하는 계산식으 로 산출하였다(30).
조효소액이 2-chloro-4-nitrophenyl 65-azido-65-deoxy-β -maltopentaoside(N3-G5-β-CNP)를 2-chloro-4-nitrophenyl β-maltotrioside(G3-β-CNP)와 2-chloro-4-nitrophenyl β -maltoside(G2-β-CNP)로 분해시키는 활성으로 하였다. 기 질용액에 조효소액을 첨가하여 반응을 개시시키고 동시에 gluco-amylase와 β-glucosidase를 첨가하여 분해생성물인 G3-β-CNP와 G2-β-CNP로부터 2-chloro-4-nitrophenol(CNP) 를 유리시켰다. 최종 생성된 CNP의 400 nm에서 정량하여 α-amylase의 활성으로 환산하였다(31).
α-Glucosidase는 4-nitro-phenyl-α-glucoside(PNPG)에서 glucose를 분해시켜 PNP를 생성시키는 활성으로 하였고 gluco-amylase는 당화력과 α-glucosidase의 반응속도와 활 성차이로 산출하였다(32).
Carbobenzoxy-L-tyrosyl-L-alanine(Cbz-Tyr-Ala)에서 L-alanine을 분해시키는 활성으로 측정하였다(33).
기질용액(1 mM p-nitrophenol-β-D-glucoside/50 mM sodium acetate buffer, pH 5.0) 0.5 mL를 37℃에서 5분간 예열한 후 조효소액 50 μL를 첨가하였다. 이 후 37℃에서 10분간 반응시킨 다음 200 mM Na2CO3용액 1 mL를 첨가하여 반응 을 정지시키고 410 nm에서 흡광도를 측정하여 유리된 p-nitrophenol을 측정하였다. β-Glucosidase 활성은 PNPG에 서 37℃, 1분간에 1 nmol의 p-nitrophenol을 만드는 활성을 1 unit로 하였다.
효모수는 methylene blue(0.01% w/v methylene blue, 2% w/v sodium citrate)로 염색한 후 현미경으로 계수하였고(34) 알코올, 산도, pH, 휘발산도, 환원당, 총당 함량은 주류분석 규정을 따랐다(35).
증류된 알코올 농도 41% 원주에 증류수를 첨가하여 알코 올 농도를 25%로 조절한 후 4℃에서 3일간 방치하여 불용 성 성분의 석출을 유도하였다. Membrane filter(5 μm, Whatman International Ltd.)로 여과하여 불용성 물질을 제 거한 후 유리병에 담고 호일로 감싼 다음 15℃ 암소에서 1달 동안 숙성시켜 소주를 제조하였다. 소주 10 mL와 10 mg/ L(25% EtOH)농도로 제조된 methyl tridecanoate (internal standard) 100 μL를 vial에 넣었다. 이후 polydimethylsiloxane(PDMS)이 0.5 mm 코팅된 15 mm twister(Gerstel Co., Tokyo, Japan)를 넣고 실온에서 1,200 rpm으로 1시간 동안 교반시켜 twister에 향기성분이 흡착되 도록 하였다. 그런 다음 twister를 꺼내어 증류수로 세척하 여 불순물을 제거시키고 여분의 물은 종이 타올로 닦아내었 다. 가열탈착장치(GERSTEL TDS3, CIS4)에 장착한 후 흡 착된 성분을 260℃로 탈착시켰다(36). 성분분석은 GC-MS (Agilent Technologies, Santa Clara, CA, USA)로 분석하였 다. 분리용 컬럼은 DB-WAX(60 m×0.25 mm I.D., 0.25 μm film thickness, Agilent Technologies Inc.)를 사용하였고 헬 륨을 1.0 mL/min의 속도로 흘려주면서 분석하였다. 컬럼오 븐은 40℃에서 5분 동안 유지시킨 다음 분당 3℃씩 240℃까 지 승온시켰다. 성분확인은 NIST05a MS spectral library data 및 AromaOffice(Nishikawa Keisoku Co., Ltd., Tokyo, Japan) database에 수록된 retention index를 참고하여 수행하 였다. 정량은 각 성분의 peak area값을 internal standard의 area값으로 나누어 internal standard 농도에 대한 상대농도 로 나타내었다.
결과 및 고찰
한아름 품종(백미)의 일반성분은 Table 1에 제시한 바와 같이 수분 14.7, 조단백질 6.8, 조지방 0.9, 조회분 0.4, 탄수 화물 76.5 g/100 g으로 Park 등(37)의 조사결과와 유사하였 다. 한편 일반 멥쌀 백미의 조성은 각각 13.4, 6.4, 0.4, 0.4, 79.5%(38)로 한아름벼는 일반미에 비해 단백질, 회분, 탄수 화물의 함량은 유사하였으나 지질의 함량이 2배 정도 높은 것으로 나타났다.
| Composition (g/100 g, fresh weight) | ||||
|---|---|---|---|---|
| Moisture | Crude | Carbohydrate | ||
| Protein | Lipid | Ash | ||
| 14.7±0.11) | 6.8±0.1 | 0.9±0.0 | 0.4±0.0 | 76.5±0.1 |
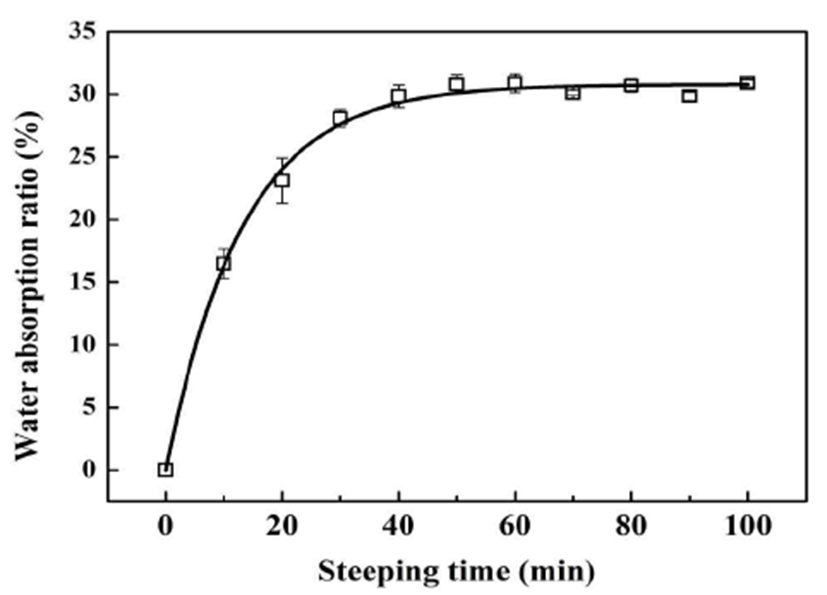
쌀의 흡수특성은 백미의 수분함량, 도정율, 품종, 수침온 도 등에 영향을 받으며, 수침시간이 짧으면 쌀 내부까지 수분이 흡수되지 않고, 장시간 수침할 경우 쌀에 있는 인(P) 이 유출되어 곰팡이 생육에 좋지 않은 영향을 미치게 되기 때문에(40) 수침시간 결정은 제국에서 중요한 요소이다.
한아름 품종의 수침시간에 따른 수분흡수율은 Fig. 1과 같다. 제국시 증자미의 적정 수분 함량은 쌀이 서로 엉겨 붙지 않으면서 곰팡이 생육에 영향을 받지 않고 효소활성을 확보할 수 있는 35-38%로 조정하는 것이 일반적이다(39). 한아름 품종의 수침시간에 따른 수분흡수율은 10분에 17.5%로 급격하게 증가한 후 20분부터는 완만해지기 시작 하여 60분에 30.1%로 최대 흡수량에 도달하였다. 수침 60분 후 수분함량은 33.6%이었고 증자 후 수분함량은 35.2% (data not shown)로 제국에 적절한 수분함량에 도달하였다. 따라서 한아름 품종의 적정 수침시간은 60분이 적절할 것 으로 판단되었다.
한아름 품종으로 제조한 입국의 산도는 7.80으로서 구연 산 함량으로 환산하면 2.92 g/100 g dry base 상당량이 함유 되어 있었다. 효소활성에 있어 당화력은 926.72, α-amylase 는 52.40, gluco-amylase는 887.71, α-glucosidase는 0.14, acidic carboxypeptidase는 17,335.73, β-glucosidase는 174.46 U/g dry base로 조사되었다(Table 2). 일본의 소주제 조용 코지의 평균 효소활성은 α-amylase 159, gluco-amylase 282, acidic carboxypeptidase 9,224 U/g dry base로서(41) α -amylase 활성은 3.0배 낮은 반면, gluco-amylase의 활성은 3.1배, acidic carboxypeptidase의 활성은 1.9배 높은 것으로 나타나 일본 입국과는 차이가 있었다. 국내에서 유통되는 백국균은 수원발효에서 생산되는 SW201과 ㈜충무발효에 서 판매하고 있는 CF1005 두 종뿐이며 Aspergillus luchuensis(또는A. luchuensis mut. kawachii)이다(42). 본 균 주는A. niger의 변종으로 동아시아에 많이 분포하고 있고 산 생성능력이 높아 한국과 일본에서 증류식 소주나 막걸리 제조에 사용되어 왔으나(23), 제조사에 따라 효소활성의 차이가 있는 것으로 알려져 있다. 일본에서 유통되고 있는 8종의 백국균을 대상으로 효소활성을 분석한 결과 최대활 성과 최소활성의 차이가 α-amylase는 2.6배, gluco-amylase 1.9배, α-glucosidase 2.1배, acidic carboxypeptidase 1.3배 나 타나는 것으로 확인되었다(43). 또한 동일 제조사의 제품도 원료곡의 품종과 도정율에 따라서 효소활성의 차이가 나타 났다(44). 한국과 일본 입국의 효소활성 차이는 균주 개량 등의 영향과 품종의 차이가 복합적으로 작용되었을 가능성 이 있다.
발효가 완료된 술덧을 분석한 결과(Table 3) 산도는 10.95-11.70, pH는 3.59-3.79 범위로 효모별로 큰 차이를 보이지 않았다. 그러나 알코올 함량은 N9(16.58%), C4(15.98%), N4(15.37%), LP(13.19%), CM(12.33%)순으로 누룩에서 분리한 N4, N9 효모 및 일본 증류식 소주용 효모 인 C4의 알코올 생산량은 유사하였고, 국내 상업용 효모는 누룩분리 효모에 비해 16.7-36.0% 낮은 것으로 확인되었다. 이러한 이유는 세 가지 원인을 먼저 생각해 볼 수 있다. 첫째는 발효기간 입국의 효소활성 저하로 쌀의 전분이 분해 되지 못하면서 알코올 생산이 낮아지는 경우이다. 발효 종 료 후 각 효모별 술덧의 당화력은 225.32-258.39 U/mL이고 α-amylase의 활성은 7.85-9.84 U/mL로 충분한 활성을 가지 고 있었기 때문에 효소활성 저하에 따른 당화불량이 원인은 아니라고 판단된다. 둘째는 발효에 충분한 효모수가 확보 되지 못한 경우이다. 술덧에 포함된 효모의 총균수는 누룩 분리 효모가 8.98-11.08, 상업용 효모가 7.06-8.34×107 cells/mL로 통계적 유의성이 없었다. 생균수는 각각 1.52-3.15, 1.81-4.55×107 cells/mL이었으며 생존율은 각각 28.3-39.2%, 23.7-64.2%로 상업용 효모가 높았다. 발효가 정상적인 술덧에 포함된 효모수는 107-108 cells/mL로(45) 각 처리구별로 발효에 충분한 효모수가 확보되었기 때문에 효모 개체수에 대한 영향도 아닌 것으로 판단된다. 셋째는 효모의 당 이용률이 낮아 알코올 생산량이 떨어지는 경우이 다. 각 효모별 술덧의 환원당 함량은 각각 N9 2.04, C4 2.88 N4 3.92, LP 7.92, CM 8.78 g/100 mL 순으로 알코올 생산량 과 반비례하며 환원당과 알코올 함량과의 상관계수(r)가 0.997(data not shown)로 매우 높게 나타났다. 결론적으로 동일조건에서 누룩분리 효모가 상업용 효모에 비해 술덧의 당을 보다 많이 이용함으로써 알코올 생산이 증가된 것으로 이해된다.
이러한 현상은 술덧의 발효경과(Fig. 2)에서도 관찰된다. 누룩에서 분리한 N4, N9 효모는 발효 11일에 CO2발생이 완만해지고 19일에 발효가 종료되는 반면 상업용 효모는 발효 9일에 CO2발생이 완만해진 다음 누룩분리 효모보다 2일 빠른 17일에 발효가 종료되었다. 발효종료일 누적 CO2 발생량은 N4와 N9이 각각 418.9, 452.1 g/mash로 상업용 효모 LP와 CM의 345.3, 327.6 g/mash에 비하여 21.3-38.0% 높은 것으로 확인되었다. 발효가 완만해지는 시기의 누적 CO2생산량은 누룩분리효모가 333.0-350.5 g/mash, 국내상 업용 효모가 256.5-250.4 g/mash로 모든 CO2생산량이 알코 올 대사과정에서 만들어졌다고 가정하면 알코올 생산량은 각각 394.7-407.8, 268.0-261.7 g/mash로 예측할 수 있다. 이때의 술덧양은 각각 3,926.9-3,939.5, 4,001.2-4,005.0 g/mash이므로 술덧의 알코올 농도는 11.2-11.8, 8.3-8.5% (v/v)로 계산된다.
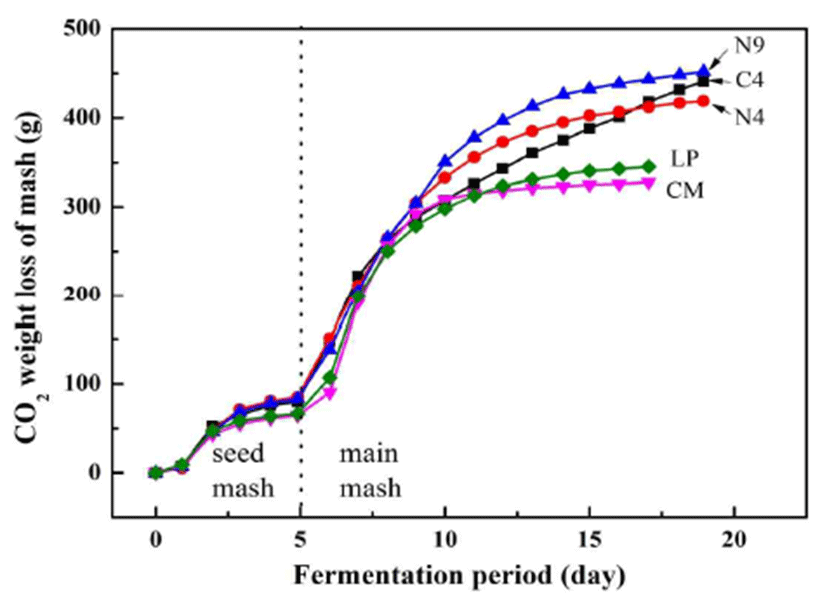
한편, 입국의 산 함량은 건물량으로 2.92%(Table 2)이고 쌀을 물에 넣었을 때 용적의 변화를 나타낸 원료계수가 1.15(46)이므로 입국 100 g(수분함량 12.5%)에 물 120 mL를 첨가하였다면 부피는 235 mL(100×1.15+120)가 되며 밑술 의 산 함량은 1.24%가 된다. 이때 pH(citric acid의 PKa1=3.13) 는 3.0-3.3 범위가 일반적이다. 이러한 환경에서 시험에 이 용된 효모는 발효에 충분한 개체수를 확보하였으나(Table 3) 국내상업용 효모는 술덧의 알코올 농도 8.3-8.5% 부근에 서 효모 세포내로 당 흡수가 저하되면서 지속적인 발효로 이어지지 못하고 CO2 발생량(Fig. 2)과 알코올 함량이 낮게 나타난 것으로 해석된다.
각 효모별 총당의 함량은 3.10-9.92 g/100 mL범위로 환원 당 함량 2.04-8.78 g/100 mL를 제외하면 1.06-1.19 g/100 mL의 전분이 분해되지 않은 난분해성으로 남아있는 것으 로 나타났다. 백미 사용량 등을 고려하여 계산하면 한아름 품종은 본 시험 조건에서 4.0%가량의 난분해성 전분을 함 유한 것으로 나타났다.
각 효모별 증류액(원주)의 알코올 함량은 41.05-41.29% 로 유사하게 증류되었으며 증류수율은 누룩 분리균이 93.2-94.5%, 국내상업용 효모가 86.3-84.2%로 누룩분리 효 모로 제조한 술덧이 7.9-12.2% 높은 것으로 조사되었다. 증류효율은 술덧에 함유된 알코올 함량에 대한 원주의 알코 올 함량비로 수율이 낮을수록 술덧에 증류되지 못한 알코올 이 많이 남아있다는 의미이다. 이로 인해 획득된 원주의 양은 누룩분리 효모가 242.23-265.55 mL이었던 반면 상업 용 효모는 173.81-193.43 mL로 25.2-52.7%가량 낮게 나타 났다.
증류식 소주에 있어 알코올 생산량은 생산비용과 직결되 어 있기 때문에 매우 중요한 요소로 여겨진다. 동일한 쌀 양에 대해 누룩분리효모가 일반적으로 사용되고 있는 상업 용 효모보다 알코올 생산량이 최대 36% 높게 나타났고 증류효율도 최대 12.2%까지 높은 결과로 원주의 생산량을 25.2-52.7%까지 증가시켰기 때문에 제품의 생산비용을 낮 출 수 있을 것으로 기대된다.
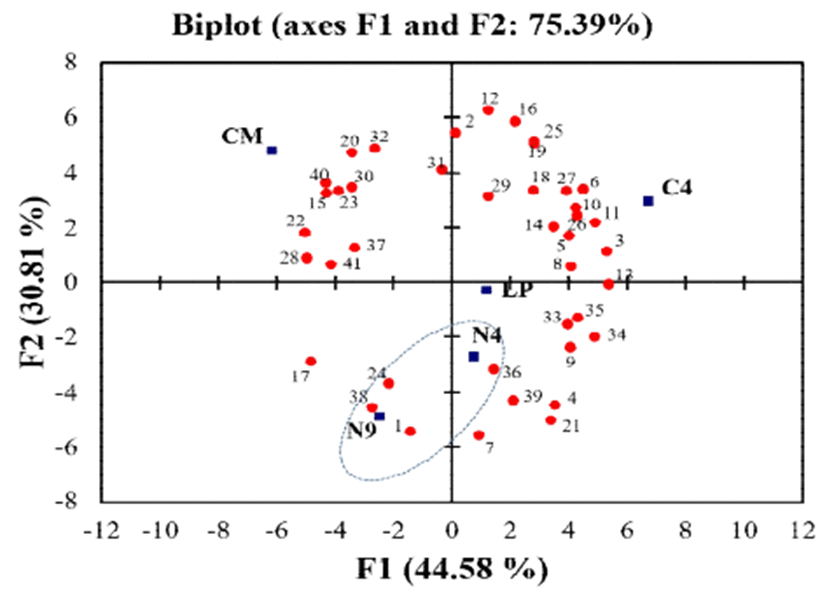
원주에 물을 첨가하여 25%로 조절한 후 1달 동안 숙성시 킨 각 쌀 증류식 소주의 향기성분은 Table 4에 나타내었고, 주성분분석 결과는 Fig. 3에 나타내었다.
각 효모 N4, N9, C4, LP, CM의 알코올류 성분의 합은 각각 26.76, 23.07, 33.33, 20.79, 27.86×100 μg/L로 C4에서 다소 높게 나타났다. 알코류 중 butanol 및 isoamyl alcohol은 양적으로 많이 존재하고 있지만 약한 알코올 향 이외에 특별한 향이 없고 분별역치 값도 50-600 mg/L로 높아 관능 에는 많은 영향을 미치지 못한다(47). 반면, phenethyl alcohol은 장미향을 가지고 있으며 역치 값도 40-70 mg/L로 비교적 낮아 증류식 소주에서 중요한 성분이다(47). 각 소주 별 phenethyl alcohol 함량은 누룩분리 효모가 1.17-1.51×100 μg/L로 상업용 효모의 0.75-1.06보다 1.1-2.0배 높은 함량을 나타내었다.
에스테르류는 과일향, 꽃향 등의 화려한 향을 가지고 있 고 역치가 낮아 소량으로도 소주의 향기에 많은 영향을 줄 수 있는 성분이다. 각 효모별 분포를 살펴보면 양적으로 많이 함유된 성분은 ethyl acetate(과일향) 6.25-12.35, isoamyl acetate(바나나향) 4.22-16.59, ethyl caproate(사과향) 4.29-6.28, ethyl caprylate(과일향) 37.20-44.71, ethyl caprate (포도주향, 꼬냑향, 장미향) 11.55-12.08, phenylethyl acetate(장미향) 1.14-6.77×100 μg/L 등으로 나타났다. Table 3에서 술덧의 휘발산도가 N4 4.95, N9 6.83, C4 2.30, LP6.13, CM 5.85로 N9과 LP에서 높게 나타났다. 휘발산의 주성분 은 acetic acid로서(47) N9과 LP가 acetic acid 생산력이 높았 다고 추정되며 이들 효모로 제조된 소주에서 ethyl acetate의 함량이 다소 높았던 이유로 판단된다. Isoamyl acetate는 isoamyl alcohol이 acetyl CoA와 alcohol acetyltransferase의 작용에 의해 생성되는 성분으로서 isoamyl alcohol의 농도 에 의존적이다(48). Isoamyl alcohol의 농도가 높았던 N4와 LP소주에서 isoamyl acetate의 함량이 높은 이유로 생각된 다. 지방산 에스테르 화합물인 ethyl caproate, ethyl caprylate, ethyl caprate는 효모별로 큰 차이를 보이지 않는 것으로 확인되었다.
에스테르 성분 중 ethyl acetate, isobutyl acetate, ethyl caproate 등의 저비점 성분은 마시기 전 술향에 기여하고 고비점 성분인 phenethyl acetate, ethyl caprylate, ethyl laurate 등은 마신 후 입안에 남는 잔향으로 작용한다(47).
각 소주에 함유된 알데히드류는 nonanal 0.05-0.08, furfural 0.14-0.19, decanal 0.04-0.09, 2-nonenal 0.04-0.05 ×100 μg/L범위로 양적으로는 furfural의 함량이 높았다. Furfural은 탄내(49)를 가지고 있기 때문에 그 함량이 많을 경우 증류식 소주에 좋지 않은 영향을 미치게 된다. 발효과 정 중에는 거의 생성되지 않고 증류 시 술덧에 함유된 당류 가 열을 받아 아미노카르보닐 반응을 거쳐 생성된다(50). Table 3에 나타낸 바와 같이 상업용 효모인 LP와 CM효모로 제조한 술덧의 환원당 함량은 각각 7.92, 8.78 g/100 mL로 누룩분리 효모로 제조한 술덧의 함량 2.04-3.92 g/100 mL보 다 높았기 때문에 furfural의 함량도 높을 것으로 예상했으 나 큰 차이를 보이지 않았다. Pentose는 산성조건에서 가열 되면 3분자의 물이 탈수되어 furfural이 생성되지만 hexose 는 동일 조건에서 3-deoxy glucosone을 거쳐 hydroxy methyl furfural(HMF)이 되고 더욱 가열되면 levulinic acid, formic acid로 분해되는 과정에서 중간생성물로 소량 만들어 진다 (51). 이외에 증류방법 및 증류기 금속의 종류, 술덧에 함유 된 유기산 종류, pH의 영향과 더불어 잔당의 종류와 양에 의해서 그 생성이 다른 것으로 알려져 있다(47). 효모별 술덧의 pH 및 산도는 유사하고(Table 3) 증류방법 및 증류기 의 종류는 동일하므로 술덧을 구성하고 있는 당의 종류에 많은 영향을 받을 수 있다. 술덧을 구성하고 있는 당은 원료 인 쌀의 분해 산물이며 glucose, maltose, isomaltose 및 polysaccharide가 주성분이고 pentose 성분은 쌀의 hemicellulose가 분해되어 생성된 xylose, arabinose가 소량 함유되어 있다(52,53). 누룩 분리 효모를 포함한 일반적인 효모는 xylose와 arabinose를 이용하지 못하므로(53) 술덧에 함유된 pentose양은 유사할 것으로 추측되고 furfural의 생 성에는 주로 hexose가 작용할 것으로 생각된다. 본 증류조 건인 술덧에 스팀을 주입하는 상압증류방식은 술덧의 최대 온도가 100℃를 초과하지 못하므로 각 hexose의 furfural변 환이 높지 않았기 때문에(54) 각 효모별로 furfural의 함량 차이가 적은 것으로 이해된다. 다만, 시중에 유통되고 있는 제품의 탄내는 직화방식의 증류식 소주에서 불꽃이 닫는 부분의 온도가 비교적 높기 때문에 hexose가 furfural로 많이 변환되었을 것으로 추측된다. 상업용 효모를 사용한 술덧 을 직화방식으로 증류할 경우 누룩분리 효모를 사용한 술덧 에 비해 탄내가 높을 가능성이 있다.
4-vinylguaiacol의 함량은 0.05-0.07×100 μg/L로 높지 않 았으며, 효모별로도 큰 차이를 나타내지 않았다. 4-vinylguaiacol은 술덧에 함유된 ferulic acid의 일부가 증류 중 산 및 열에 의해 4-vinylguaiacol로 변환되어 유출되고 저장 중에 산화되어 바닐라향을 가지고 있는 vanillin 및 vanillic acid로 바뀌게 된다(49).
주성분 분석(Fig. 3)은 전체 분산의 75.39%를 설명하고 있으므로 비교적 적합한 모델로 나타났다. 전체 분산의 44.58%를 설명하고 있는 제 1주성분(F1)의 각 효모별 적재 값은 N4, N9, C4, LP, CM가 각각 0.025, 0.162, 0.773, 0.617, 0.056으로 일본 상업용 효모인 C4와 국내 상업용 효모인 CM이 변동을 이끌었다. 전체의 30.81%를 설명하고 있는 제 2주성분(F2)은 N9의 적재값이 0.628을 가지면서 다른 효모의 적재 값 0.03-0.321보다 높게 나타났다. 즉, 시험에 사용된 5종의 효모 중 C4와 CM소주의 향기성분 차이가 가장 많았고 다음은 N9과 다른 4종의 효모의 분포차이가 큰 것으로 해석된다. 누룩에서 분리한 N4, N9 효모로 만든 증류식 소주가 다른 상업용 효모와 차이가 나는 성분은 1번(i-BuOH), 38번(isobutanal diethyl acetal), 24번(ethyl caprate), 36번(tetradecanoic acid) 성분으로 나타났다.
이외에 C4소주에는 ethyl isovalerate, isoamyl acetate, diethyl succinate 등의 향기성분이 다른 소주에 비해 2.3-9.3 배 높게 나타나(Table 4, Fig. 3) C4소주의 특징을 줄 수 있는 성분으로 판단되었다. 이 중 사과향을 가지고 있는 ethyl isovalerate의 역치는 3 μg/L(55)이고 isoamyl acetate의 역치값 역시 1.6 mg/L(47)로 낮은 편에 속하므로 너무 과도 할 경우 전체적인 향의 균형을 깰 수 있다. CM은 phenylacetaldehyde diethyl acetal과 propyl caproate 등의 성 분이 주요하게 다른 소주와 차이가 있는 것으로 나타났다 (Fig. 3). Acetal 성분은 aldehyde 성분이 알코올과 반응하여 생성되는 물질로 부드럽고 고급스러운 향을 부여하고(47), propyl caproate는 파인애플향을 가지고 있으나(56) isobutyl caprylate, ethyl laurate 등의 고비점 에스테르 성분함량 등도 높아 마시고 난 후 입안에 잔여감이 오래 머물면서 맛에 있어 좋지 않은 영향을 미칠 수 있다.
누룩분리한 효모인 N4와 N9은 알코올 생산수율을 증대 시켜 제품의 생산비용을 감소시킬 수 있으며 향기성분에 있어서도 적정한 균형을 이루고 있기 때문에 산업용으로 검토해 볼 가치가 있다고 판단된다.
요 약
재래누룩에서 분리한 효모인 N4와 N9에 대해 쌀 증류식 소주제조 특성을 살펴보았다. 원료 쌀(한아름 품종)의 일반 성분은 수분 14.7, 조단백질 6.8, 조지방 0.9, 조회분 0.4, 탄수화물 76.5 g/100 g이었다. 제조된 입국의 총산 함량은 2.92%(citric acid, dry base)였으며 효소활성에 있어 당화력 은 926.72, α-amylase 52.40, gluco-amylase 887.71, α -glucosidase 0.14, acidic carboxypeptidase 17,335.73, β -glucosidase 174.46 U/g dry base로 나타났다. 술덧의 알코올 함량은 재래누룩 분리 효모가 15.37-16.58%로 상업용 효모 12.33-13.19%보다 16.7-36.0% 높은 것으로 나타났다. 반면, 환원당 함량은 각각 2.04-3.92, 7.92-8.78 g/100 mL로 상업용 효모의 당 이용률이 누룩분리 효모보다 낮았다. 이러한 결 과로 증류 후 원주의 획득량이 누룩분리 효모에서 25.2-52.7% 높았다. 쌀 증류식 소주(알코올 25%)에서 41개 의 휘발성 성분이 검출되었으며, 주성분 분석 결과 누룩분 리 효모와 상업용 효모는 i-BuOH, isobutanal diethyl acetal, ethyl caprate, tetradecanoic acid 성분의 함량 차이가 있는 것으로 나타났다.