1. 서론
비만은 에너지 섭취와 소비 사이에 균형이 깨질 때 발생하는 질환의 일종으로, 당뇨병, 고혈압, 고지혈증 등 다양한 질병들과의 연관성이 밝혀져 왔다. 일반적으로 비만의 분류는 체질량지수(body mass index, BMI)를 사용하며, WHO에 따르면 성인의 경우 BMI 30 kg/m2 이상일 때 비만으로 분류한다(Kang 등, 2020). 국내에서는 대한비만학회의 기준에 따르면 25 kg/m2 이상 30 kg/m2 미만일 때 1단계 비만, 30 kg/m2 이상 35 kg/m2 미만일 때 2단계 비만, 35 kg/m2 이상은 3단계 비만으로 분류한다(Kim, 2021). 비만 인구는 전 세계적으로 급증하고 있으며(Tucci 등, 2010), 국내에서도 성별과 관련 없이 남 ․ 녀 모두에서 증가하고 있다(Oh, 2017). 비만과 식생활의 상관관계를 분석한 결과, 여성의 경우 비만 집단이 정상 집단에 비해 총섭취 열량 대비 탄수화물 비율이 높고 지방 비율이 낮게 나타났으며(Bang과 Hyeon, 2018), 비만 집단이 정상 집단에 비해 정제된 탄수화물 섭취량이 높은 것으로 확인되었다(Han 등, 2017). 이러한 결과를 바탕으로 비만과 과도한 정제 탄수화물 섭취 사이의 유의미한 상관관계 를 확인할 수 있다.
비만과 유사하게 제 2형 당뇨병(T2DM)도 우리나라에서 급격하게 증가하고 있는 질환 중의 하나로 고혈당증을 동반하는 특성을 나타낸다(Chong과 Han, 2022). 제 2형 당뇨병의 치료방법으로 체내 탄수화물 대사에 관여함으로써 공복 혈당 및 식후 혈당을 개선시키는 약물 치료제를 주로 사용하며, 이러한 치료제로 당 신생과정 억제제, α-glucosidase 억제제 등이 사용된다(Lee 등, 2022). 현재 주로 사용되고 있는 당뇨치료제 및 혈당강하제는 합성 및 화학적 치료제로 설사, 구역질, 메스꺼움과 같은 위장장애 등의 부작용이 나타나는 것으로 알려져 있다(Kim 등, 2015). 따라서 부작용이 없는 새로운 α-amylase와 α-glucosidase 활성 저해 물질을 찾아낼 필요가 있으며, 이와 관련하여 프로바이오틱스의 α-amylase와 α-glucosidase에 대한 활성 저해 효능에 대한 연구가 진행되고 있다(Kumari 등, 2022; Wang과 Li, 2022).
프로바이오틱스는 적정량 섭취 시 인간의 건강에 유익한 영향을 가지는 살아있는 미생물로, 장내 유익균 증식시키고 유해균을 억제하여 장내 미생물 균총을 안정화시켜 질병을 예방하는 등 이로운 효과를 야기한다(Seo 등, 2019). 그러나 프로바이오틱스 경구투여로 인한 설사, 피부 발진 및 두드러기와 같은 주요 부작용 사례가 보고됨에 따라 그 안전성에 대한 연구가 필요하다(Seo 등, 2019). 또한, 외부로부터 유입된 유전자에 의해 항생제 내성을 나타내는 미생물의 경우, 장 내 미생물로 항생제 내성 유전자를 전달할 수 있는 위험을 가지게 된다(Blair 등, 2015). 따라서, 국내에서는 식품의약품안전평가원이 프로바이오틱스 안전성 평가 가이드를 제시하였으며, 이 가이드에 따르면 프로바이오틱스 섭취 시 인체에 유해한 결과를 가져올 수 있는 항생제 내성 평가, 용혈활성 평가 및 독소 생성 여부 등의 평가를 권장한다(식품의약품안전처, 2022).
따라서, 본 연구에서는 국내 프로바이오틱스 안전성 평가기준에 따라 단일 균주들의 안전성을 평가하여 프로바이오틱스 섭취 안전성을 확인하고, 단일과 혼합 프로바이오틱스로서 탄수화물 소화효소(α-amylase와 α-glucosidase)에 대한 억제 가능성을 연구하였다. 2. 재료 및 방법
2. 재료 및 방법
본 연구에는 Lactobacillus acidophilus PBS066(DSM 24936), Lactiplantibacillus plantarum(이전 Lactobacillus plantarum) PBS067(DSM 24937), Limosilactobacillus reuteri(이전 Lactobacillus reuteri ) PBS072(DSM 25175)가 동일한 비율로 구성되어 있는 probiotics mixture를 SynBalance Srl(Via Celeste Milani, Origgio VA, Italy)로부터 제공받아 사용하였다. Presti 등(2015)에 따르면, 이 probiotics mixture를 구성하고 있는 각 균주들은 건강한 인체의 분변으로부터 분리되었으며, 내산성과 담즙산 내성이 확인되어 프로바이오틱스로 사용할 수 있음이 확인되었다. Probiotics mixture를 구성하는 각 단일 균주를 실험에 사용하기 위해 deMan Rogosa and Sharpe(MRS) 고체 배지(BD Difco, Franklin Lakes, NJ, USA)에 도말하여 37°C, 24시간, 혐기조건으로 배양하였으며, 단일 콜로니를 선별하여 16S rRNA 분석을 통해 각 콜로니를 분리 및 동정하였다. 동정이 완료된 각 균주를 MRS 액체 배지(BD Difco, Franklin Lakes, NJ, USA)에 2회 계대 배양하였으며, 배양액을 원심분리하여 배양액과 균주를 분리하였고, 균주는 phosphate buffered saline(PBS)(Dyne Bio Inc., Gyeonggi-do, Korea)를 이용하여 세척한 후 실험에 사용하였다.
Probiotics mixture의 항생제 내성평가는 European Food Safety Authority(EFSA) 기준을 따라 진행되었다. 항생제 내성평가에는 9가지 유형의 항생제 스트립(E-TEST®, BioMérieux, Marcy l’Etoile, France)이 사용되었다. LSM 고체배지(90% Isosensitest broth, 10% MRS broth, 1.5% bacto agar)를 제조한 후, probiotics mixture의 각 균주 3×108 CFU/mL를 멸균된 면봉에 충분히 적셔 LSM 고체배지에 도말한다. 도말한 균주가 배지에 잘 스며든 후 멸균 포셉을 이용해 각각 항생제 종류별 스트립을 LSM 고체배지에 올려 놓고, 37°C, 48시간 혐기조건으로 배양 후 각 항생제별 최소억제농도를 확인하였다. 최소억제농도는 균이 자라지 않는 스트립 부위의 가장 밑 부분으로 확정하였다.
각각의 균주를 MRS 액체배지에 접종하여 37°C, 24시간 혐기조건으로 배양하였고, 배양액의 일부를 혈액고체배지(Sheep blood agar)(KisanBio, Seoul, Korea)에 선상도말평판법으로 도말하여 37°C, 48시간 배양한 후, 콜로니 주위에 생기는 환을 관찰하여 용혈활성을 확인하였다(식품의약품안전처, 2022).
Probiotics mixture의 단일 균주의 세포 독성 평가에는 Dyne LDH PLUS Cytotoxicity Assay Kit(Dyne Bio Inc., Gyeonggi-do, Korea)가 사용되었다. Caco-2 세포(대장암 세포주) 1×104 cells를 Dulbecco’s modified Eagle’s medium(DMEM)(Corning®, Glendale, Arizona, USA), 10% Fetal bovine serum(FBS)(Gibco, Carlsbad, CA, USA), 1% penicillin/streptomycin(v/v)(Gibco, Carlsbad, CA, USA) 배지에 접종하고, 5% CO2, 37°C 환경에서 24시간 배양하였다. 배양 후, probiotics mixture의 단일 균주를 균수별로(107, 108, 109 CFU/well) Caco-2 세포에 접종하고 같은 환경조건에서 배양하였다. 양성 비교군으로는 lysate 용액을 사용하였으며, 음성 비교군으로는 균주가 들어있지 않은 DMEM 배지를 사용하였다. 비교군으로는 세계적으로 가장 많이 연구된 프로바이오틱스 균종 중 하나인 Lacticaseibacillus rhamnosus(이전 Lactobacillus rhamnosus) GG(LGG)를 사용하였다. 다음과 같은 공식에 따라 cytotoxicity(%)를 계산하였다.
α-Amylase 저해 활성은 Gowri 등(2007)의 방법을 변형하여 이용하였다. α-Amylase 저해 활성 실험에는 20 mM sodium phosphate buffer, 6.7 mM NaCl, pH 6.9로 조정된 용액을 사용하였고, 이 용액을 이용하여 1 U/mL α-amylase(Sigma-Aldrich Co., St. Louis, MO, USA) 효소 희석액과 각 시험군의 균주 1×109 CFU가 함유된 균질화 용액을 조제하였다. 조제한 효소 희석액 1 mL와 균주 함유 균질화 용액 1 mL를 혼합하였고, 25°C에서 30분 동안 정치시켰다. 혼합액에 1% starch 용액을 1 mL 첨가하여 25°C에서 15분 동안 반응시켰고, DNS 용액(96 nM 3, 5-dinitrosalicylic acid, 5.31 M sodium potassium tartrate, 2 M NaOH, deionized water) 1 mL를 가하여 85°C에서 약 15분간 발색시킨 후, 9 mL의 증류수를 첨가하고 microplate reader (BioTek, Winooski, VT, USA)로 540 nm에서 흡광도를 측정하였다. 음성대조군으로는 균주가 들어있지 않은 20 mM sodium phosphate buffer, 6.7 mM NaCl, pH 6.9로 조정된 용액을 사용하였으며, 양성대조군으로는 acarbose(Alfa Aesar, Tewksbury MA, USA)를 사용하였다. 다음과 같은 공식에 따라 α-amylase inhibitory activity(%)를 계산하였다.
α-Glucosidase 저해 활성 측정을 위해 α-Glucosidase Activity Assay kit(Sigma-Aldrich Co.)를 사용하였다. 효모, Saccharomyces cerevisiae로부터 얻어진 α-glucosidase(Sigma-Aldrich Co.)를 50 mM phosphate buffer, pH 7.0 용액으로 희석하였다. 0.5 U/mL α-glucosidase 5 μL와 각 시험군의 균주 1×109 CFU가 함유된 균질화 용액 20 μL를 혼합하였다. 혼합액에 50 mM phosphate buffer, pH 7.0 용액 200 μL와 α-NPG Substrate 5 μL가 혼합된 master reaction mix 200 μL를 첨가하여 섞어 주고, 20분 동안 실온에서 반응시킨 후에 microplate reader(BioTek)로 504 nm에서 흡광도를 측정하였다. 음성대조군으로는 균주가 들어있지 않은 50 mM phosphate buffer, pH 7.0 용액을 사용하였으며, 양성대조군으로는 acarbose(Alfa Aesar)를 사용하였다. 다음과 같은 공식에 따라 α-glucosidase inhibitory activity(%)를 계산하였다.
3. 결과 및 고찰
본 실험에 사용한 probiotics mixture의 균주 3종의 항생제 9종 ampicillin, vancomycin, gentamycin, streptomycin, erythromycin, clindamycin, tetracycline, chloramphenicol에 대한 최소 생육 저해농도를 평가하여 항생제 내성을 확인하였다. EFSA에서 제시한 L. acidophilus, L. plantarum 및 L. reuteri의 cut off value를 참고하였으며[EFSA Panel on Additives and Products or Substances used in Animal Feed(FEEDAP) 등, 2018], 그 결과 항생제 9종에 대한 3종의 균주 모두 EFSA가 제시한 cut off value보다 낮은 최소 생육 저해농도가 확인되었다(Table 1).
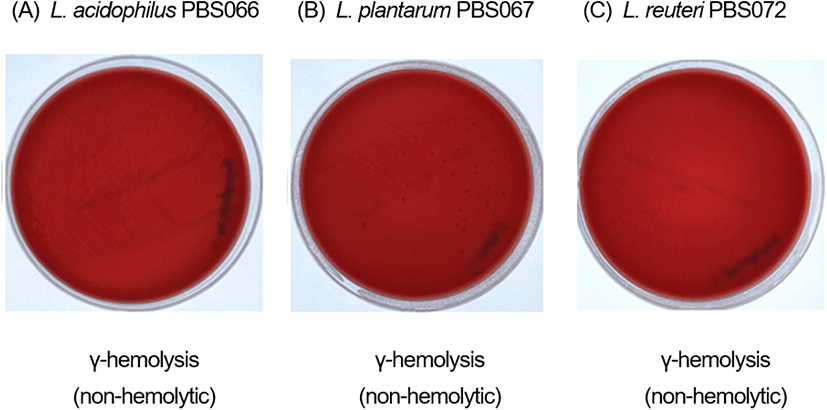
프로바이오틱스의 용혈활성은 혈액고체배지에 배양 시, 적혈구의 용해에 의한 혈액고체배지의 색상 변화를 통해 측정할 수 있다. 프로바이오틱스의 용혈활성은 적혈구의 불완전 용해로 콜로니 주위 녹색의 환을 생성하는 α-hemolysis, 적혈구의 완전 용해로 흰색 또는 노란색 환을 생성하는 β-hemolysis 그리고 용혈활성이 없어 환을 생성하지 않는 γ-hemolysis로 구별된다(Halder 등, 2017; Kim 등, 2018). 본 실험에 사용한 3종의 균주는 혈액고체배지에서 배양한 결과, 용혈 활성을 나타내지 않음이 확인되었다(Fig. 1).
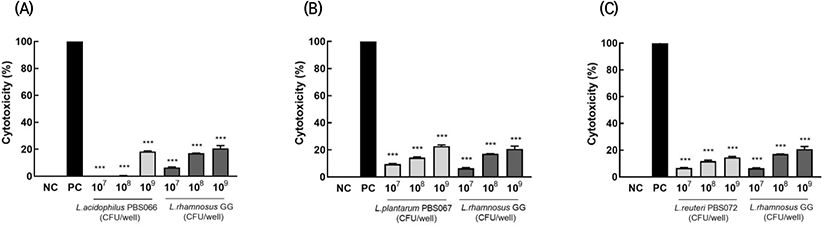
Lactate dehydrogenase(LDH) assay는 독소에 의해 사멸한 세포로부터 세포배양액으로 방출되는 LDH의 활성을 측정하는 방법으로, 프로바이오틱스와 프로바이오틱스의 균수에 의해 Caco-2의 세포막 손상 정도를 평가하는 데 사용된다(Chen 등, 2017). 본 실험에서 사용한 probiotics mixture 균주 3종의 세포독성 확인 결과, 양성대조군 대비 단일 균주에 의해 Caco-2 세포로부터 방출되는 LDH의 활성이 유의적으로 낮게 나타났으며(p<0.001, Fig. 2), 균주의 균수가 높을수록 Caco-2 세포의 세포막을 손상시켜 LDH 방출을 증가시켰다. 이 결과는 다양한 식품 및 보충제로 사용되어 섭취 경험이 많은 비교균주 LGG와 유사한 경향과 수치로 확인되었으며, 따라서 본 실험에 사용한 L. acidophilus PBS066, L. plantarum PBS067 및 L. reuteri PBS072는 비교균주 LGG만큼 섭취에 안전할 것으로 판단된다.
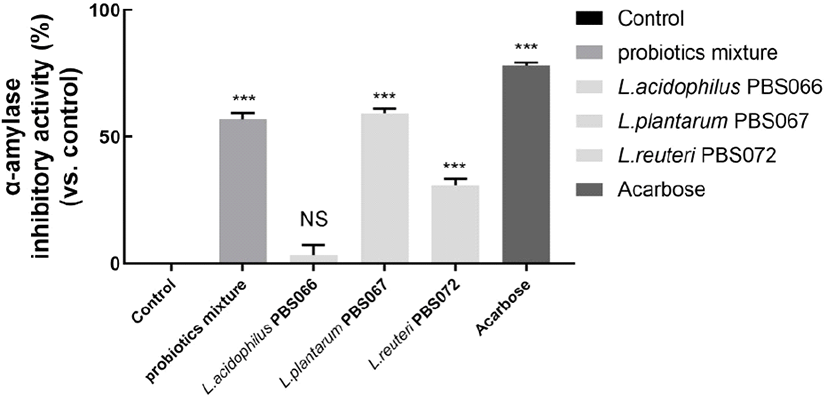
Probiotics mixture의 균주 3종 및 probiotics mixture의 α-amylase 저해 활성을 측정하였다. 음성대조군 대비 α-amylase 저해 활성은 acarbose(78.0±1.30%), L. plantarum PBS067(59.49±1.68%), probiotics mixture (56.79±2.75%), L. reuteri PBS072(30.91±2.64%) 그리고 L. acidophilus PBS066(3.49±3.81%) 순으로 저해 활성이 확인되었으며, L. acidophilus PBS066을 제외하고 모든 시험군에서 음성대조군 대비 유의적으로 저해 활성이 높게 나타나는 것을 확인하였다(p<0.001, Fig. 3). α-Amylase는 포도당의 중합체인 전분 및 이의 올리고당류인 아밀로오즈를 분해하는 효소로, 인체에서 효소의 활성이 저해될 경우 탄수화물의 소화 및 흡수속도를 감소시킨다고 알려져 있다(Park 등, 2009; Shivanna 등, 2015). 따라서, 단일 균주 L. plantarum PBS067, L. reuteri PBS072와 probiotics mixture는 음성대조군 대비 높은 α-amylase 저해 활성이 확인되어, 탄수화물 소화 및 흡수 저해효과가 있을 것으로 판단된다.
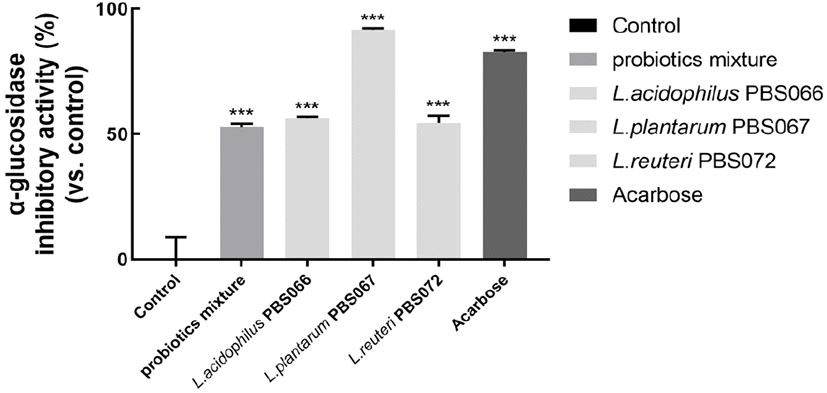
Probiotics mixture의 균주 3종 및 probiotics mixture의 α-glucosidase 저해 활성을 측정하였다. 그 결과 L. plantarum PBS067(91.70±0.55%), acarbose(82.73± 0.65%), L. acidophilus PBS066(56.47±0.55%), L. reuteri PBS072(54.42±3.02%) 및 probiotics mixture(52.91± 1.23%) 순으로 저해 활성이 확인되었으며, 모든 시험군에서 α-glucosidase 저해 활성이 음성대조군 대비 유의적으로 높게 나타나는 것을 확인하였다(p<0.001, Fig. 4). α-Glucosidase는 포도당 중합체를 포도당으로 분해하는 효소로, 인체에서의 효소 활성이 저해될 경우 소장점막에서 탄수화물 흡수를 지연시키는 역할을 하며, 탄수화물 섭취 후 혈당상승을 억제할 수 있다고 알려져 있다(Kim 등, 2015). 따라서, 모든 단일 균주와 probiotics mixture는 음성대조군 대비 높은 α-glucosidase 저해 활성이 확인되어, 탄수화물 흡수 지연 및 혈당상승 억제효과가 있을 것으로 판단된다.
4. 요약
본 연구는 probiotics mixture(Lactobacillus acidophilus PBS066(DSM 24936), Lactiplantibacillus plantarum PBS067(DSM 24937), Limosilactobacillus reuteri PBS072(DSM 25175))의 안전성 및 탄수화물 소화 효소 저해 효과를 in vitro로 평가하는 것을 목적으로 한다. 모든 균주는 유럽식품안전처(EFSA) 지침에서 권장하는 항생제 내성 프로필을 충족시켰으며, 모든 균주는 용혈 활성 및 세포 독성을 나타내지 않았다. Probiotics mixture, L. plantarum PBS067 그리고 L. reuteri PBS072는 α-amylase 활성을 억제하는 것으로 나타났으며, probiotics mixture와 이의 균주 3종 모두 α-glucosidase 활성을 억제하는 것으로 나타났다. 이로써 본 연구에 사용한 probiotics mixture 및 이의 단일 균주 3종의 안전성과 탄수화물 소화 억제 효과를 확인하였으며, 따라서 probiotics mixture 이의 단일 균주 3종은 섭취하여도 안전하며 섭취 시 체내 탄수화물 대사를 잠재적으로 조절하는 것을 확인하였다.